이성화
Isomerization화학에서 이성질화 또는 이성질화는 분자, 이온 또는 분자 조각이 다른 화학 [1]구조를 가진 이성질체로 변환되는 과정이다.엔올라이제이션은 이성질화(tautomerization)[2]의 한 예이다.이성질화가 분자 내에서 일어나는 것을 재배열 반응이라고 [citation needed]할 수 있다.
이성화 반응을 위한 활성화 에너지가 충분히 작을 때, 두 이성체는 서로 온도 의존적인 평형 상태로 존재할 것이다.표준 자유 에너지 차이 값인 Gδ {\ G의 많은 [3]값이 관측 데이터와 계산된 데이터 간에 잘 일치하여 계산되었습니다.
예와 응용 프로그램
알칸스
골격 이성질화는 석유화학 산업에서 사용되는 분해 공정에서 발생합니다.평균 체인 길이를 줄일 뿐만 아니라, 이 과정에서 직쇄 탄화수소가 분기 이성질체로 전환되는데, 이는 다음과 같은 [citation needed]반응을 나타낸다.
- 3 2 2 3 → 3 3 (3) 3 (i-butane
분기형 탄화수소를 함유한 연료는 옥탄 등급이 [4]더 높기 때문에 내연기관으로 선호됩니다.
알케네스
말단 알켄은 금속 촉매의 존재 하에서 내부 알켄으로 이성화된다.이 과정은 쉘 상위 올레핀 공정에서 알파 올레핀을 내부 올레핀으로 변환하는 데 사용되며, 올레핀 메타세시스를 따릅니다.특정 종류의 알켄 중합 반응에서 체인 워킹은 가지를 성장 중인 [citation needed]폴리머에 도입하는 이성질화 과정이다.
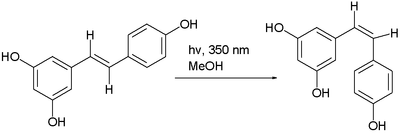
레스베라트롤의 트랜스 이성질체는 광화학 [5]반응에서 시스 이성질체로 전환될 수 있다.
아줄렌과 나프탈렌의 열적 재배열이 [citation needed]관찰되었다.
기타 예
알도스-케토스 이성질체, 일명 로브리 드 브루인-반 에켄슈타인 변환은 당류 [citation needed]화학의 예를 제공한다.
유기금속 이성질화의 예로는 데카페닐페로센[(γ-CPh555)2Fe]의 결합 [6][7]이성질체로부터 제조하는 것이 있다.
「 」를 참조해 주세요.
레퍼런스
- ^ IUPAC, 화학 용어집, 제2판('골드북') (1997).온라인 수정판: (2006–) "이성화".doi:10.1351/goldbook.I03295
- ^ Antonov L (2016). Tautomerism: Concepts and Applications in Science and Technology (1st ed.). Weinheim, Germany: Wiley-VCH. ISBN 978-3-527-33995-2.
- ^ 양자화학적 방법 Stefan Grimme, Marc Steinmetz, Martin Korth J. Org를 사용하여 유기분자의 이성화 에너지를 계산하는 방법 화학; 2007; 72(6) 페이지 2118 - 2126; (조) doi:10.1021/jo062446p
- ^ Karl Griesbaum, Arno Behr, Dieter Biedenkapp, Heinz-Werner Voges, Dorothea Garbe, Christian Paetz, Gerd Collin, Dieter Mayer, Hartmut Höke (2002). "Hydrocarbons". Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002/14356007.a13_227.
{{cite encyclopedia}}: CS1 maint: 작성자 파라미터 사용(링크) - ^ 레스베라트롤 광이성화: 통합가이드-문의실험 Elyse Bernard, Philip Britz-McKibin, Nicholas Gernigon Vol. 84 No.7 2007 화학교육 저널 1159.
- ^ Brown, K. N.; Field, L. D.; Lay, P. A.; Lindall, C. M.; Masters, A. F. (1990). "(η5-Pentaphenylcyclopentadienyl){1-(η6-phenyl)-2,3,4,5-tetraphenylcyclopentadienyl}iron(II), [Fe(η5-C5Ph5){(η6-C6H5)C5Ph4}], a linkage isomer of decaphenylferrocene". J. Chem. Soc., Chem. Commun. (5): 408–410. doi:10.1039/C39900000408.
- ^ Field, L. D.; Hambley, T. W.; Humphrey, P. A.; Lindall, C. M.; Gainsford, G. J.; Masters, A. F.; Stpierre, T. G.; Webb, J. (1995). "Decaphenylferrocene". Aust. J. Chem. 48 (4): 851–860. doi:10.1071/CH9950851.