십이지장자리 지아목
Giardia duodenalis| 십이지장자리 지아목 | |
|---|---|
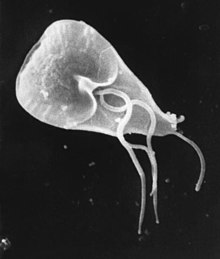 | |
| 지아디아 람리아 세포, SEM | |
| 과학적 분류 | |
| 도메인: | 에우카리오타 |
| 망울: | 메타모나다 |
| 주문: | 증서나다목 |
| 가족: | 헥사미티과 |
| 지누스: | 자르디아 |
| 종: | 십이지장자리 G. |
| 이항식 이름 | |
| 십이지장자리 지아목 스타일즈, 1902년 | |
| 동의어 | |
지아디아 십이지장은 소장에서 결장하여 번식하는 편평한 기생 미생물로, 지아디아시스(Giardia angelis), 지아디아스(Giardia lamlia)라고도 한다.[1][2][3]기생충은 복강접착판이나 흡충기에 의해 상피에 부착되며, 이항분열을 통해 번식한다.[4]지아디아시스(Giardiasis)는 혈류를 통해 퍼지는 것도 아니고, 위장의 다른 부분으로 퍼지는 것도 아니고, 소장의 발광에 국한된 채로 남아 있다.[5]지아르디아는 숙주체 바깥에서도 생명을 유지할 수 있는 외막을 가지고 있으며 염소 소독에도 내성이 있다.Giardia trophozoites는 루멘으로부터 영양분을 흡수하고 혐기성 물질이다.만약 그 유기체가 분열되고 얼룩이 진다면, 그것의 특징적인 패턴은 친숙한 "웃는 얼굴" 상징과 유사하다.[6]
인간 감염의 주요 경로는 처리되지 않은 식수(이 기생충의 가장 흔한 전염 방법),[3] 음식, 그리고 인간의 배설물에 오염된 토양의 섭취와 많은 개발도상국에서 특히 흔한 현상인 오수의 섭취를 포함한다.[7][3]자연수의 오염은 집중적인 방목 현상이 발생하는 분수령에서도 발생한다.
Giardia 감염은 전 세계적으로 발생한다.탁아소, 등산객, 가족, 면역억제 성인의 어린이들 사이에서 미국과 캐나다에서 가장 흔하게 확인된 장내 기생충이다.미국에서는 연간 약 2만 건이 보고되고 있다.[8]
라이프 사이클
G. 십이지장은 수명주기 동안 두 가지 형태학적으로 뚜렷한 형태를 취한다.복제 형태는 열대우림이라 불리는 숙주의 작은 창자에서만 생존하는 운동성 배 모양의 세포다.[9]대류호조충은 결국 숙주 장내 상피에 달라붙을 때까지 장내 점액을 통해 헤엄친다.[10][9]접착된 대류호조개석은 더 많은 대류호조개 또는 비복제 낭종 단계를 형성하면서 이항 핵분열로 나눈다.[9]낭종은 숙주의 대장을 통과하여 대변에 흘린다.[9]G. 램블리아 낭종은 환경 스트레스 요인에 내성이 있으며, 습기를 유지하면 몇 주 또는 몇 달 동안 환경에서 생존할 수 있다.[10][11][9]낭종은 숙주 동물이 섭취할 때까지 휴면 상태를 유지한다.새로운 숙주에서는 환경조건이 낭종을 촉발하여 두 개의 트로프호조석을 생산하고 상피세포에 부착하여 순환을 새로 시작한다.[9]
생태와 분포
낭종은 찬물에서 몇 주 또는 몇 달 동안 생존할 수 [12]있기 때문에 오염된 우물이나 수계에 존재할 수 있으며, 특히 자연적으로 발생하는 연못, 폭풍우 저장 시스템, 심지어 깨끗해 보이는 산천과 같은 정체된 수원에 존재할 수 있다.낭종은 감염된 사람이나 동물의 배설물로 오염된 표면, 토양, 음식 또는 물에서도 발견될 수 있다.[13]그것들은 또한 도시 저수지에서 발생할 수 있으며 염소 처리와 오조놀리시스 같은 전통적인 물 처리 방법에 내성이 있기 때문에 정수 처리 후에도 지속될 수 있다.[12]조나르디아의 전염 또한 가능하기 때문에, 지아디아 감염은 황야에서 캠핑하거나 오염된 개울이나 호수에서 수영하는 사람들의 걱정거리인데, 특히 비버 댐에 의해 형성된 인공호수(Giardiasis의 통칭, "beaver feather")이다.
수인성 공급원 외에도 분변-구강 전염이 발생할 수 있다. 예를 들어 어린이집에서 어린이가 위생 관행이 불량할 수 있다.아이들과 함께 일하는 사람들도 감염된 사람들의 가족처럼 감염될 위험에 처해 있다.모든 Giardia 감염이 증상인 것은 아니며, 많은 사람들이 자신도 모르게 이 기생충의 보균자 역할을 할 수 있다.
Giardia는 인간을 감염시키지만 고양이, 개, 새를 감염시키는 가장 흔한 기생충 중 하나이다.포유류 숙주들 또한 소, 양,[15] 염소를 [14]포함한 수십 종의 종을 포함한다.[15]
고양이는 쉽게 치료할 수 있고, 양은 보통 단순히 살을 빼지만 송아지에서는 기생충이 치명적일 수 있고 항생제나 전해질에 반응하지 않는 경우가 많다.송아지들 사이의 운반체들은 또한 무증상일 수 있다.이 기생충은 친칠라에게는 치명적이므로 그들에게 안전한 물을 공급하여 각별한 주의를 기울여야 한다.개들은 1세 미만 인구의 30%가 개집에서 감염되는 것으로 알려져 감염률이 높다.그 감염은 어른 개들보다 강아지들에게 더 많이 퍼진다.감염된 개들은 격리하여 치료할 수도 있고, 개집에 있는 모든 무리들은 상관없이 함께 치료할 수도 있다.케넬은 표백제 또는 기타 세척 소독제로 세척해야 한다.운동용으로 사용되는 잔디 부위는 개들이 감염 징후를 보인 후 최소 1개월 이상 오염된 것으로 간주해야 하는데, 이는 낭종이 환경에서 장기간 생존할 수 있기 때문이다.감염견을 최소 20일간 격리하고 깨끗한 물 공급에 대한 세심한 관리와 유지보수를 통해 예방이 가능하다.
세포생물학
G. 십이지장 대류호초는 배 모양 세포로 길이 10~20μm, 가로 7~10μm, 두께 2~4μm이다.[9][10]그들은 대류조족을 장으로 밀어내는 네 쌍의 플라겔라를 통해 운동성이 있다.[10]특히 각 G. 십이지장 세포에는 두 개의 핵이 있는데, 두 핵 모두 유전자를 능동적으로 변환한다.[9]핵에 인접하여 G. 십이지장 세포는 세포의 많은 부분을 통해 확장되는 내소성 망막을 가지고 있다.[16]낭종으로 분화하려는 대류호조류에도 일단 낭포벽 공사가 시작되면 사라지는 엔시스테이션 특유의 두드러진 소변기가 들어 있다.[16]대부분의 다른 진핵생물과 달리 G. 십이지장 세포는 눈에 보이는 미토콘드리아를 포함하고 있지 않지만, 대신에 미토솜이라고 불리는 실질적으로 감소된 대사 기관지를 포함하고 있다.[10]게다가, 세포들은 골지체를 포함하고 있지 않은 것으로 보이며, 대신에 분비 시스템은 완전히 소포체 망막과 세포 전체에 퍼진 수많은 소변기들로 구성된다. 말초성 소변기라고 불린다.[16]말초 음낭은 세포 밖의 영양분을 섭취하고 세포 밖의 노폐물을 배출하는 역할을 한다.[11]각 세포는 또한 G. 람블리아 세포골격의 일부를 구성하는 중앙체라고 불리는 한 쌍의 단단한 구조물을 포함하고 있다.[9]열대우림은 복측 디스크라고 불리는 특수 디스크 모양의 오르간젤을 통해 숙주의 상피 세포를 고수한다.[9]
낭종은 트로포자이트보다 약간 작은 타원형의 세포다.[10]그들은 플라겔라가 부족하고, 부드럽고 투명한 낭포성 벽으로 덮여 있다.[10]각각의 낭종은 핵 4개, 복측 원반 2개 등 두 개의 영양분을 위한 오르가넬을 포함한다.[10]
신진대사
G. 람블리아는 주로 아르기닌 디히드롤라아제 경로뿐만 아니라 글리콜리시스(glycolysis)를 통해 포도당을 분해함으로써 에너지를 생성한다.[17]그것은 핵물질을 숙주로부터 구해내는 대신 스스로 합성할 수 없다.[17]철황 성단의 합성은 미토콘드리아의 잔해일 가능성이 높은 미토솜이라고 불리는 이중 암막 결합 구획에서 이루어진다.[17]각 세포에는 세포 전체에 흩어져 있는 말초미토솜과 알 수 없는 이유로 세포의 중심에 모이는 중앙미토솜의 두 종류로 나뉜 25~100개의 미토솜이 들어 있다.[18]미토콘드리아에서처럼 특정 펩타이드 신호 시퀀스를 가진 단백질이 미토솜으로 밀거래되어 수입된다.[17]미토콘드리아와 달리 미토솜은 자신의 게놈을 갖고 있지 않다.모든 미토소말 유전자는 Giardia 핵 게놈에 의해 암호화된다.[17]
유전학
Giardia와 다른 졸업장들은 외관상 유사한 두 개의 핵, DNA 내용, 전사, 복제 시간 등을 소유한다는 점에서 독특하다.하플로이드 게놈당 5개의 염색체가 발생한다.게놈은 염기서열로 배열되어 2007년에 출판되었지만, 그 염기서열에는 몇 개의 간극이 포함되어 있다.염기서열은 약 1200만 쌍이며 약 5000개의 단백질 코딩 유전자를 포함하고 있다.[19]GC 함량은 46%이다.트로피호조아이트는 4개의 플로이드를 가지고 있고 낭종의 플로이드는 8개의 플로이드를 가지고 있는데, 이는 결국 자르디아가 같은 핵의 염색체들과 반대핵의 염색체들 사이에서 어떻게 동질성을 유지하는가에 대한 의문을 제기한다.현대적인 염기서열 기술은 다른 균주를 재취득하기 위해 사용되어 왔다.[20]
진화
Giardia는 원시적으로 무성하고 핵 사이에서 DNA를 전달할 수단이 없는 것으로 추정되었다.이러한 가정들은 대립이 형 접합성(<>0.01%)의 게놈 격리종, 걸 환영해의 놀랍도록 낮은 수준을 설명하는 매우 힘든 것이었지만 무성의 모든 그러한 추정들 지금 의심에 인구 유전학 recombination[21]과 감수 분열 유전자의 신분 확인을 위해, 재결합에 소이 a중 증거 증거 제공하었다그 nd엔시스테이션 과정 동안 핵들 사이의 유전 물질의 교환에 대한 [22]증거
위와 같은 Giardia의 성생활에 관한 이러한 발견은 진핵생물의 성재생의 기원을 이해하는 데 중요한 의미를 갖는다.현존하는 진핵생물들 사이에 성적 재생산이 널리 퍼져 있지만, 최근까지 성생활은 진핵생물의 원시적이고 근본적인 특징일 것 같지 않았다.섹스가 진핵생물의 근본이 아닐 수 있다는 견해의 유력한 이유는 진핵 혈통의 초기 조상으로부터 갈라진 특정한 인간 병원성 단세포 진핵생식(예: Giardia)에 성생식이 이전에는 결여되어 있는 것으로 나타났기 때문이다.
Malik 등은 Giardia에서 재조합을 위해 위에서 인용한 증거 외에도 많은 감수분열 특이 유전자가 Giardia 게놈에서 발생하며, 나아가 이러한 유전자의 호몰로그램이 또 다른 단세포 진핵생물인 트리코모나스 질리날리스에서도 발생한다고 보고했다.[23]이 두 종은 진핵생물들 사이에서 매우 분화가 심한 선열의 후손들이기 때문에, 말릭 외 연구진은 [23]이 감수성 유전자들이 모든 진핵생물의 공통 조상에 존재한다고 제안했다.따라서 이러한 관점에서 진핵생물의 초기 조상은 성적인 번식을 할 수 있을 가능성이 있었다.게다가, Dacks와 Roger는[24] phylogenetic 분석에 기초하여 모든 진핵생물의 공통 조상에 기능적 성이 존재한다고 제안했다.번스타인 외 연구진도 이 견해를 뒷받침하는 증거를 검토했다.[25]
현재까지 G. 십이지장염의 유전자형 조립품 8개가 인정되었다(A-H).[14]다양한 숙주로부터 격리된 G. 십이지장성의 유전자형은 A와 B 조립체가 가장 큰 범위의 숙주 종을 감염시키고 있으며, 인간 피실험자를 감염시키는 주요 (또는 아마도 유일한) G. 십이지장 조립체로 보인다는 것을 보여주었다.[14]
리서치
샌디에이고 캘리포니아 대학의 프랜시스 길린과 그녀의 동료들은 실험실에서 이 기생충의 전체 라이프사이클을 배양했고, 자르디아의 라이프사이클 변형을 촉발하는 숙주의 소화 시스템에서 생화학적 단서들을 확인했다.[26][27]그들은 또한 기생충이 감염된 유기체의 방어를 회피하는 몇 가지 방법을 밝혀냈다.그 중 하나는 표면에 있는 단백질을 바꾸는 것인데, 이것은 감염된 동물의 면역체계가 기생충을 탐지하고 퇴치할 수 있는 능력을 혼란스럽게 한다(항원적 변화라고 한다).길린의 연구는 왜 지아디아 감염이 극도로 지속적이고 재발하기 쉬운지를 보여준다.게다가, 그것의 생물학과 생존 기술에 대한 이러한 통찰력은 과학자들이 Giardia 감염을 이해하고, 예방하고, 치료하기 위한 더 나은 전략을 개발할 수 있게 해줄 것이다.
2008년 12월 네이처는 자르디아가 숙주 면역 반응을 피하기 위해 변종별 표면 단백질을 전환할 수 있는 RNA 간섭 메커니즘의 발견을 보여주는 기사를 게재했다.[28]이번 발견은 아르헨티나 코르도바 가톨릭대학교의 의과대학 생화학 및 분자생물학 연구소에서 박사 주도로 연구한 연구팀에 의해 이루어졌다.휴고 루잔.
Giardia에 관한 주요 회의는 International Giardia and Cryptosporidium Conference이다.최신판(2019, 프랑스 루앙)에 제시된 결과 요약본을 이용할 수 있다.[29]
역사
Giardia에 대한 최초의 설명은 1681년 Antonie van Leeuwenhoek에 의한 것으로, 그는 Robert Hooke에게 보낸 편지에서 Giardia 대류호조족과 닮은 "동물"을 그의 대변에 묘사했다.[9][30]다음으로 알려진 Giardia에 대한 설명은 1859년에야 체코의 의사 Vilém Lambl이 소아과 환자의 대변에서 본 열대우림 단계에 대한 설명을 발표했다.램블은 그 유기체를 세르코모나스 장막이라고 불렀다.[31]1888년 라파엘 블랜차드는 람블의 명예를 걸고 기생충 람블리아 장염으로 이름을 바꾸었다.[31]1915년 찰스 스타일즈는 람블과 파리의 알프레드 마티외 지아드 교수를 기리기 위해 유기체 이름을 지아디아 람블리아로 바꾸었다.[31][32]1921년 찰스 E. 사이먼은 기생충의 형태학에 대한 자세한 설명을 발표했다.[9]
참고 항목
참조
- ^ Simner, P. J.; Kraft, Colleen Suzanne (January 2017). "Medical Parasitology Taxonomy Update: January 2012 to December 2015". Journal of Clinical Microbiology. 55 (1): 43–47. doi:10.1128/JCM.01020-16. PMC 5228259. PMID 27440818.
- ^ Rumsey, P; Waseem, M (January 2019). "Giardia Lamblia Enteritis". PMID 30285390.
{{cite journal}}:Cite 저널은 필요로 한다.journal=(도움말) - ^ a b c "Giardia Parasites CDC". www.cdc.gov. 24 June 2019. Retrieved 7 April 2020.
- ^ Oxford textbook of Medicine. Vol. 1 (4th ed.). Oxford University Press. 2003. pp. 759–760. ISBN 978-0-19-262922-7.
- ^ 해리슨의 내과, 해리슨의 온라인장 199 원생장염과 트로코모니아시스
- ^ DeMay, Richard M. (1999). Practical principles of cytopathology. the University of Michigan: American Society for Clinical Pathology. p. 88. ISBN 9780891894377.
- ^ Hogan, C. Michael (2010). "Water pollution". In McGinley, Mark; Cleveland, C. (eds.). Encyclopedia of Earth. Washington DC: National Council for Science and the Environment.
- ^ "Pathogen Safety Data Sheet: Infectious Substances – Giardia lamblia". Canada. Public Health Agency of Canada. 30 April 2012. Retrieved 14 April 2018.
- ^ a b c d e f g h i j k l Despommier DD, Griffin DO, Gwadz RW, Hotez PJ, Knirsch CA (2019). "Giardia lamblia". Parasitic Diseases (7 ed.). Parasites Without Borders. pp. 11–20. Retrieved 3 June 2019.
- ^ a b c d e f g h Ryan KJ, ed. (2018). "53:Sarcomastigophora-The Flagellates". Sherris Medical Microbiology (7 ed.). McGraw-Hill Medical. ISBN 9781259859809.
- ^ a b Cernikova L, Faso C, Hehl AB (September 2018). "Five facts about Giardia duodenalis". PLOS Pathogens. 14 (9): e1007250. doi:10.1371/journal.ppat.1007250. PMC 6160191. PMID 30261050.
- ^ a b Huang DB, White AC (2006). "An updated review on Cryptosporidium and Giardia". Gastroenterol. Clin. North Am. 35 (2): 291–314, viii. doi:10.1016/j.gtc.2006.03.006. PMID 16880067.
- ^ "Giardia Parasites CDC". www.cdc.gov. Retrieved 25 October 2017.
- ^ a b c Heyworth, Martin F. (2016). "Giardia duodenalis genetic assemblages and hosts". Parasite. 23: 13. doi:10.1051/parasite/2016013. ISSN 1776-1042. PMC 4794627. PMID 26984116.

- ^ a b Tzanidakis, Nikolaos; Sotiraki, Smaragda; Claerebout, Edwin; Ehsan, Amimul; Voutzourakis, Nikolaos; Kostopoulou, Despoina; Stijn, Casaert; Vercruysse, Jozef; Geurden, Thomas (2014). "Occurrence and molecular characterization of Giardia duodenalis and Cryptosporidium spp. in sheep and goats reared under dairy husbandry systems in Greece". Parasite. 21: 45. doi:10.1051/parasite/2014048. ISSN 1776-1042. PMC 4154256. PMID 25187088.

- ^ a b c Faso C, Hehl AB (April 2011). "Membrane trafficking and organelle biogenesis in Giardia duodenalis:Use it or lose it". International Journal for Parasitology. 41 (5): 471–480. doi:10.1016/j.ijpara.2010.12.014. PMID 21296082.
- ^ a b c d e Einarsson E, Ma'ayeh S, Svard SG (December 2016). "An up-date on Giardia and giardiasis". Current Opinion in Microbiology. 34: 47–52. doi:10.1016/j.mib.2016.07.019. PMID 27501461.
- ^ Ankarklev J, Jerlstrom-Hultqvist JJ, Ringqvist E, Troell K, Svard SG (April 2010). "Behind the smile: cell biology and disease mechanisms of Giardia species". Nature Reviews Microbiology. 8 (6): 413–422. doi:10.1038/nrmicro2317. PMID 20400969. S2CID 28139274.
- ^ Morrison HG; McArthur AG; Gillin FD; et al. (2007). "Genomic minimalism in the early diverging intestinal parasite Giardia lamblia". Science. 317 (5846): 1921–6. Bibcode:2007Sci...317.1921M. doi:10.1126/science.1143837. PMID 17901334. S2CID 29299317.
- ^ Franzén O; Jerlström-Hultqvist J; Castro E; et al. (2009). Petri, William (ed.). "Draft Genome Sequencing of Giardia intestinalis Assemblage B Isolate GS: Is Human Giardiasis Caused by Two Different Species?". PLOS Pathogens. 5 (8): e1000560. doi:10.1371/journal.ppat.1000560. PMC 2723961. PMID 19696920.
- ^ Cooper MA, Adam RD, Worobey M, Sterling CR (November 2007). "Population genetics provides evidence for recombination in Giardia". Curr. Biol. 17 (22): 1984–8. doi:10.1016/j.cub.2007.10.020. PMID 17980591. S2CID 15991722.
- ^ Adam, RD; Svard, SG (2010). "Giardia: Nuclear and Chromosomal Structure and Replication". Anaerobic Parasitic Protozoa: Genomics and Molecular Biology. Caister Academic Press. ISBN 978-1-904455-61-5.[페이지 필요]
- ^ a b Malik SB, Pightling AW, Stefaniak LM, Schurko AM, Logsdon JM (2008). "An expanded inventory of conserved meiotic genes provides evidence for sex in Trichomonas vaginalis". PLOS ONE. 3 (8): e2879. Bibcode:2008PLoSO...3.2879M. doi:10.1371/journal.pone.0002879. PMC 2488364. PMID 18663385.
- ^ Dacks J, Roger AJ (June 1999). "The first sexual lineage and the relevance of facultative sex". J. Mol. Evol. 48 (6): 779–83. Bibcode:1999JMolE..48..779D. doi:10.1007/pl00013156. PMID 10229582. S2CID 9441768. Archived from the original on 15 September 2000.
- ^ Bernstein H, Bernstein C, Michod RE (2012). "Ch. 1: DNA repair as the primary adaptive function of sex in bacteria and eukaryotes". In Sakura Kimura, Sora Shimizu (eds.). DNA Repair: New Research. Hauppauge NY: Nova Science. pp. 1–49. ISBN 978-1-62100-808-8. Archived from the original on 29 October 2013. Retrieved 21 April 2013.
- ^ Hetsko ML, McCaffery JM, Svärd SG, Meng TC, Que X, Gillin FD (1998). "Cellular and transcriptional changes during excystation of Giardia lamblia in vitro". Experimental Parasitology. 88 (3): 172–83. doi:10.1006/expr.1998.4246. PMID 9562420.
- ^ Svärd SG, Meng TC, Hetsko ML, McCaffery JM, Gillin FD (1998). "Differentiation-associated surface antigen variation in the ancient eukaryote Giardia lamblia". Molecular Microbiology. 30 (5): 979–89. doi:10.1046/j.1365-2958.1998.01125.x. PMID 9988475. S2CID 26329209.
- ^ Prucca CG, Slavin I, Quiroga R, Elias EV, Rivero FD, Saura A, Carranza PG, Lujan HD (2008). "Antigenic variation in Giardia lamblia is regulated by RNA interference". Nature. 456 (7223): 750–754. Bibcode:2008Natur.456..750P. doi:10.1038/nature07585. PMID 19079052. S2CID 205215563.
- ^ Buret, André G.; Cacciò, Simone M.; Favennec, Loïc; Svärd, Staffan (2020). "Update on Giardia: Highlights from the seventh International Giardia and Cryptosporidium Conference". Parasite. 27: 49. doi:10.1051/parasite/2020047. ISSN 1776-1042. PMC 7425178. PMID 32788035.

- ^ Feely, Dennis E.; Erlandsen, Stanley L.; Chase, David G. (2013). "Structure of the trophozoite and cyst". In Erlandsen, Stanley L.; Meyer, Ernest A. (eds.). Giardia and Giardiasis: Biology, Pathogenesis, and Epidemiology. Springer Science. p. 3. ISBN 9781489905949.
- ^ a b c Maria Lipoldova (May 2014). "Giardia and Vilém Dušan Lambl". PLOS Neglected Tropical Diseases. 8 (5): e2686. doi:10.1371/journal.pntd.0002686. PMC 4014406. PMID 24810153.
- ^ Ford BJ (2005). "The discovery of Giardia" (PDF). The Microscope. 53 (4): 148–153.
외부 링크
| 위키미디어 커먼즈에는 자르디아 람블리아와 관련된 미디어가 있다. |
- Giardia 람블리아 이미지 라이브러리
- GiardiaDB:Giardia 람블리아 게놈 염기서열 분석 프로젝트
- 자르디아에 관한 워싱턴 주 보건부 자료표.
- 질병 관리 및 예방 센터(CDC) Giardia 정보
- 미국 환경보호청(United Statement Agency)의 물속 Giardia 현황표
- 미크로베의 자르디아 기사위키
- 자르디아 라이프 사이클 비디오
- 자르디아와 시에라 네바다 주
- http://diarrhea.emedtv.com/giardia-lamblia/giardia-lambia.html Wayback Machine에서 2012년 11월 9일 보관
- Prucca CG; Slavin I; Quiroga R; et al. (2008). "Antigenic variation in Giardia lamblia is regulated by RNA interference". Nature. 456 (7223): 750–4. Bibcode:2008Natur.456..750P. doi:10.1038/nature07585. PMID 19079052. S2CID 205215563. Lay summary – The New York Times (15 December 2008).
{{cite journal}}:Cite는 사용되지 않는 매개 변수를 사용한다.lay-source=(도움말) - "Giardia intestinalis". NCBI Taxonomy Browser. 5741.







