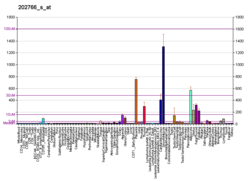
피브릴린-1
Fibrillin-1| FBN1 | |||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||||||||||
| |||||||||||||||||||||||||
| 식별자 | |||||||||||||||||||||||||
| 에일리어스 | FBN1, ACMICD, ECTOL1, FBN, GPHYD2, MASS, MFS1, OCTD, SGS, SSKS, WMS, WMS2, MFLS, 피브릴린 1 | ||||||||||||||||||||||||
| 외부 ID | OMIM: 134797 MGI: 95489 HomoloGene: 30958 GeneCard: FBN1 | ||||||||||||||||||||||||
| |||||||||||||||||||||||||
| |||||||||||||||||||||||||
| |||||||||||||||||||||||||
| 맞춤법 | |||||||||||||||||||||||||
| 종. | 인간 | 마우스 | |||||||||||||||||||||||
| 엔트레즈 | |||||||||||||||||||||||||
| 앙상블 | |||||||||||||||||||||||||
| 유니프로트 | |||||||||||||||||||||||||
| RefSeq(mRNA) | |||||||||||||||||||||||||
| RefSeq(단백질) | |||||||||||||||||||||||||
| 장소(UCSC) | Chr 15: 48.41 ~48.65 Mb | Chr 2: 125.14 ~125.35 Mb | |||||||||||||||||||||||
| PubMed 검색 | [3] | [4] | |||||||||||||||||||||||
| 위키데이터 | |||||||||||||||||||||||||
| |||||||||||||||||||||||||
피브릴린-1은 15번 [5][6]염색체에 위치한 FBN1 유전자에 의해 인간에게 암호화되는 단백질이다.그것은 10-12 nm 칼슘 결합 미세섬유의 구조적 구성 요소 역할을 하는 세포외 기질 당단백질이다.이러한 미세 섬유는 신체 전체에 걸쳐 탄성 및 비탄성 결합 조직에서 힘을 지탱하는 구조적 지지대를 제공합니다.단백질을 변화시키는 돌연변이는 태아 사망, 발달 문제, 마르판 증후군 또는 경우에 따라 바일-마르케사니 증후군을 포함한 다양한 표현형 효과를 발생시킬 수 있다.
FBN1유전자
FBN1은 230kb 유전자로 65개의 코드 엑손이 있으며, 프로피버린이라고 불리는 2,871-아미노산 긴 프로프로틴을 코드화하며, 프로피버린 말단 부근에서 푸린 변환효소 효소에 의해 단백질 분해되어 섬유소인 피브릴린-1과 140-아미노산 긴 프로프로핀을 [7][8]프로신이라고 한다.
FBN-1단백질구조
피브릴린-1의 배열은 47개의 6-시스테인 EGF 유사 도메인, 7개의 8-시스테인 도메인 및 잠복 TGF-β 결합 단백질과 상동하는 프롤린이 풍부한 [9]영역을 포함한다.
태아 심혈관 발달
FBN-1 유전자는 다양한 배아 발달 프로그램에 관여한다.피브릴린-1에서 만들어지는 미세섬유는 탄성구조와 비탄성구조 모두에 기여한다.심장 판막과 대동맥에서 탄성 섬유의 형성을 위해서는 FBN-1과 FBN-2가 [10]모두 관여해야 한다.FBN-1과 FBN-2는 탄성섬유의 다른 성분과 함께 임신 [11]4주 이내에 배아 반월판막에서 발현되는 것으로 나타났다.이 분자들은 반달 판막의 심실층에 탄성 섬유를 형성하기 위해 상호작용합니다.또한 피브릴린-1과 피브릴린-2는 대동맥의 탄성 섬유 발달에 매우 중요하다.태아 발달 후 피브릴린-2의 발현이 현저하게 감소하지만 피브릴린-1의 발현은 성년기에도 계속된다.이는 피브릴린-2가 초기 탄성섬유의 발달을 지시하는 반면, 피브릴린-1은 성숙한 [11]탄성섬유의 구조적 지지를 제공한다는 생각을 뒷받침한다.
FBN-1 또는 FBN-2 유전자의 돌연변이가 발생하면 세포외 매트릭스의 손상으로 인해 상당한 변형이 발생할 수 있다.마르판 증후군은 FBN-1 유전자의 돌연변이로 인해 발생하는 선천성 질환이다.이는 심혈관계 구조를 포함한 환자 몸의 미세섬유의 기형과 그에 따른 약화로 이어진다.약해진 탄성 섬유는 심장 판막과 대동맥의 내구성 및 팽창성을 악화시킵니다.이것은 Marfan [12]Syndrome과 일반적으로 관련된 대동맥류 및 탈수 판막의 설명을 제공한다.
마르판 증후군
마르판 증후군(MFS)은 눈, 심혈관계, 골격계, 피부, 폐계, 경막과 같은 신체 시스템의 결합 조직에 영향을 미치는 상염색체 우성 질환이다.MFS는 5,000명 [13]중 1명꼴로 영향을 미칩니다.MFS는 단일 분자 [14]테스트가 아닌 겐트 병리학적 표라고 불리는 채점 시스템을 사용하여 쉽게 진단되는 병리학적 요소가 아닙니다.가족력이 없는 MFS 개인을 진단하려면 두 가지 기준을 충족해야 합니다.첫째, 두 개의 다른 주요 장기 시스템이 영향을 받아야 하고, 둘째,[15] 세 번째 장기 시스템이 영향을 받아야 합니다.
MFS는 보통 de novo 돌연변이(어느 쪽에서도 유전되지 않은 새로운 생식선 돌연변이)에서 발생하며, 개별 표현형식으로 길고 가는 팔다리와 사지를 나타내며, 일반적으로 흉부 척추측만증, 과굴곡성 관절, 펙투스 exclubatum(선켄 흉부) 및 망막 [13]박리를 일으킨다.심각한 MFS를 초래하는 De Novo 돌연변이는 신생아의 [14]기대 사망률이 높다.고전적인 MFS 증상은 보통 사춘기나 인생의 후반기에 두드러진다; 드물게 삶의 [14]초기 단계에서 발병한다.MFS의 가장 일반적인 피부 징후는 피부 띠가 빨간색, 보라색, 그리고 [16]흰색인 선조 확장증이다.피부 표피가 얇고 평평하며, 상부 보호 피부층의 [16]두께가 감소합니다.이러한 증상은 피부와 탄력 [16]섬유와 평행하게 배치된 직선적이고 얇은 콜라겐 다발로 조직학적으로 특징지어진다.탄성 섬유는 상층 진피에서 더 밀도가 높고, 이 영역 아래에는 탄성 섬유는 국소적으로 존재하지 않는다.줄무늬와 피부 경계 사이에는 때때로 휘고, 부러지고,[17] 그물 모양의 탄성 섬유들이 있습니다.이러한 증상들은 [17]MFS 환자들에게 거미줄 같은 피부 생김새의 원인이 된다.
MFS의 관리는 라이프스타일 조언, 물리치료, 약물치료 및 수술을 포함한 많은 측면을 포함합니다.[14] MFS의 관리에는 신체활동을 감소 및 제한하는 생활습관 상담, 내막 예방, 대동맥 연속영상촬영, 대동맥 보호를 위한 γ차단제 및 대동맥 [14]근부의 예방적 치환 등이 포함된다.MFS에 감염된 성인의 경우 감정적 육체적 스트레스를 줄이고 격투기, 축구, 농구 등 고충격 스포츠에서 맥박이 [14]분당 110회 미만인 수영, 자전거, 조깅 등 저충격 운동으로 전환할 것을 권장합니다.아이들은 또한 [14]MFS의 올바른 관리를 보장하기 위해 유사한 지침을 따라야 합니다.
MFS는 15q21.1 염색체에 위치한 "FBN1" 유전자의 돌연변이에 의해 발생하며, 그 결과 피브릴린-1이 [5]분해된다.피브릴린-1은 350kDa, 2871-아미노산 시스틴이 풍부한 당단백질로서 세포외매트릭스([18][19]ECM) 내 결합조직의 탄성섬유에 엘라스틴을 결합시키는 역할을 한다.결합조직의 취약성은 일반적으로 벽이 관강내 [20]압력을 견딜 수 없기 때문에 대동맥류를 일으킨다.피브릴린-1의 결함은 MFS와 직접적으로 [20]상관되는 TGF-β 수치를 증가시킨다.
마르판증후군 발현에 있어서 TGF-β의 역할
TGF-β는 배아 처리, 세포 성장, 아포토시스 유도를 담당하는 파라크린 조절 단백질로 콜라겐 생성 및 ECM 재모델링을 [20]강화합니다.비MFS 감염 개인에서는 TGF-β 단백질이 세포에서 분비되어 PAI-1 생성 및 Smad2 인산화 촉진된다.[17]TGF-β 단백질은 N 말단 특성에서 잠복기 관련 단백질(LAP)과 3개의 잠복기 단백질(LTBP1, 3 또는 4) 중 하나와 결합하여 작은 잠복기(SLC)[21]를 형성한다.다음으로 SLC는 활성 사이토카인을 [22]포함한 대형 잠복체(LLC)를 형성하는 잠복 TGF-β결합단백질(LTBP)에 세포외적으로 결합한다.LLC는 LTBP를 통해 피브릴린-1의 미세 섬유에 부착되어 비활성 TGF-β를 보존할 수 있다[6].TGF-β는 일련의 조절 메커니즘을 통해서만 활성화될 수 있으며, 배아 [20]발달에서 올바른 기능을 유지합니다.피브릴린-1의 돌연변이는 LLC가 미세 섬유에 부착할 수 없고 잠복 형태가 [21]생성되지 않기 때문에 EC 공간에서 TGF-β의 수치를 증가시킨다.TGF-β는 인산화 [23]캐스케이드를 시작하기 위해 이합체 수용체와 복합체를 형성한다.이 인산화 작용은 대동맥류나 탈수 [13]판막과 같은 기능 부전을 일으킬 수 있다.
대동맥근확장, 폐폐기종, 방실판변화 및 골격근근근근근병증과 같은 MFS의 임상증상은 변화된 TGF-β 활성화 및 [22]신호전달에 의해 유도된다.대동맥 특정 증상은 대동맥 [22]근벽의 과도한 TGF-β 신호 전달과 밀접한 관련이 있다.TGF-β 중화항체(NAB)의 체계적 투여를 통한 TGF-β 길항작용은 MDS와 관련된 대동맥 병리학의 발달, 보다 구체적으로 대동맥 벽의 변화 및 진행성 대동맥 [22]확장의 발생을 막았다.또한 TGF-β의 길항작용은 근육 재생, 구조 및 강도, 폐포 격막 및 승모판 [22]형태학에 도움이 되는 MFS 증상을 더욱 감소시켰다.
ECM에서 제거되지 않은 LLC는 단백질 분해 효소에 의존하거나 독립적인 [22]방식으로 활성화되기 쉽습니다.MMP2 및 MMP9는 선택된 TGF-β 활성제 및 리간드이며, MFS에 감염된 환자의 조직에서 보다 높은 수준에서 발견된다. TGF-β의 복합적이고 자유로운 형태는 돌연변이 ECM 격리 및 LLC [22]활성화 증가로 인해 순환으로 침출될 수 있다.
'FBN1' 유전자의 돌연변이
"FBN-1"은 약 200kb의 유전자이며 15번 염색체에 위치한 65개의 엑손으로 나누어진 큰 코드 배열로 구성되어 있다.이 유전자는 피브릴린-1 [24]단백질을 암호화한다.피브릴린-1은 주로 표피성장인자(EGF) 유사 모듈의 연속 반복 도메인으로 구성된 약 350kDa의 대형 시스테인 리치 당단백질이다.이러한 도메인은 칼슘 결합 표피 성장인자 모듈(cbEGF 유사 모티브)과 상동성이며 탄성과 비탄성 [14][16]조직을 구성하는 별개의 8-시스테인 모듈이다.이러한 탄성 및 비탄성 조직은 피브릴린-1과 피브릴린-2의 [25]헤테로폴리머인 미세섬유다발이다.탄성생성은 미세섬유와 탄성섬유가 여러 [17]고분자에 의해 조직화된 증착을 통해 스스로 조립되는 생물학적 과정이다.중합 피브릴린은 개별 폴리머와 구조 [17]구성요소의 측면 연동을 통해 마이크로 파이브릴 격자를 발생시키는 '줄에 박힌 비드' 마이크로 파이브릴 구조로 특징지을 수 있다.
피브릴린-1 돌연변이는 MFS를 일으키는 주요 돌연변이 단백질이다.이 돌연변이는 보통 지배-음성 메커니즘을 야기하는 미세섬유의 조립을 방해한다.
돌연변이는 다음과 같습니다.
- 피브릴린-1의 칼슘 결합과 관련된 시스테인과 [24]같은 단일 염기 치환에 의해 발생하는 미센스 돌연변이.
- 무의미한 돌연변이 또는 프레임 이동으로 인해 [24]조기 종료됩니다.
- 외음성 스플라이스 부위 내 돌연변이를 통해 암호 스플라이스 [24]부위의 생성으로 인한 삽입 또는 결실을 허용합니다.
- 인트로닉 스플라이스 사이트 베이스 변경으로 인해 대체 스플라이싱 및 프레임 내 엑손 건너뛰기 [24]또는 삭제가 발생합니다.
4종류의 돌연변이를 조합하면 피브릴린-1이 잘못 발현된다.분자 수준에서 표현형과 유전자형 사이에는 상관관계가 없습니다
6개 염색체 위치에서 FBN-1 유전자 돌연변이, 5q13-14에서 TAAD1, 11q23-24에서 FAA1, 3p24-25에서 TAAD2, 15q24-26에서 TAAD3, 10q23-24에서 TAAD4, 16p12-13에서 MYH11이 MFS로 알려져 있다.이 위치들은 혈관 [27]기능에 관여하는 유전자를 가지고 있는 경향이 있다.MYH11 유전자는 평활근 미오신 중쇄와 평활근 알파-액틴을 [27]코드하는 TAAD4의 ACTA2를 담당합니다.
FBN1 유전자의 엑손13에 의해 코드된 CaB-EGF 유사 도메인의 보존된 시스테인에 영향을 미치는 익명의 아미노산 변화가 [17]MFS를 발생시킬 수 있다.MFS의 빈도 및 심각도는 C1-C2 또는 C3-C4 디설피드 결합에 잘못된 치환이 있을 때 발생하므로 이러한 위치의 정확한 시스테인 국재화와 디설피드 결합은 구조적 [17]무결성에 매우 중요하다.C5-C6 이황화 결합에서 잘못된 결합을 초래하는 FBN1 유전자의 돌연변이는 일반적으로 [17]덜 심각한 MFS를 초래한다.FBN1 폴리펩타이드에 따른 CaB-EGF 도메인의 집중 돌연변이는 MFS 심각도 표현형에 [17]영향을 미친다.엑손 13에서는 C538P, 엑손 14에서는 C570R 또는 엑손 15에서는 C587Y에서 시스테인 치환의 국소적 치환 돌연변이는 눈과 관련된 MFS 증상, 특히 외시 렌티스(exopy rentis)[17]를 초래한다.미세섬유 자체는 무척추동물과 작은 척추동물의 [17]순환계에서 혈류역학적 부하를 지탱할 수 있다.엘라스틴과 주변 VSMC와 통합된 ECM 시스템의 개발은 고등 척추동물이 올바르게 [17]기능하기 위해 필요합니다.피브릴린-1은 탄성단위의 안정화에 필수적인 것이 아니라 마이크로파이브릴의 조립에 필수적이다.활성 A의 상향 조절은 피브릴린-1 및 TGF-β 신호 전달 분자와 함께 작용하여 섬유증식 반응을 [17]생성한다.또한 CYR61 유도는 세포 유착을 지원하고 매트릭스 재모델링을 조절하는 기능을 하며, 대형 혈관의 [17]형성과 그 무결성의 기본이다.
FBN1의 일반적인 변종들은 유전자와 인간 표현형에도 영향을 미칠 수 있다.예를 들어 페루 인구의 일반적인 변형(E1297G)으로 인해 [28]높이가 2.2cm 감소할 수 있습니다.
임상적 의의
FBN1 유전자의 돌연변이는 마르판 증후군과 그 변형 마르파노이드-프로게로이드-리포디스트로피 증후군, 상염색체 우성 바일-마르케사니 증후군, 고립된 외시 렌즈형, MAS 표현형, 슈프린트젠-골드버그 [29][30]증후군과 관련이 있다.
FBN1과 FBN2의 돌연변이는 청소년 특발성 척추측만증과 [31]관련이 있다.
대동맥근확장, 폐폐기종, 방실판변화 및 골격근근근근근병증과 같은 MFS의 임상증상은 변화된 TGF-β 활성화 및 [22]신호전달에 의해 유도된다.대동맥 특정 증상은 대동맥 [22]근벽의 과도한 TGF-β 신호 전달과 밀접한 관련이 있다.TGF-β 중화항체(NAB)의 체계적 투여를 통한 TGF-β 길항작용은 MDS와 관련된 대동맥 병리학의 발달, 보다 구체적으로 대동맥 벽의 변화 및 진행성 대동맥 [22]확장의 발생을 막았다.또한 TGF-β의 길항작용은 근육 재생, 구조 및 강도, 폐포 격막 및 승모판 [22]형태학에 도움이 되는 MFS 증상을 더욱 감소시켰다.
로사르탄
Losartan은 TGF-β의 [22]발현과 활성화를 억제하여 TGF-β 시그널링을 길항시키는 것으로 알려진 앤지오텐신II 수용체 차단제이다. Losartan은 독립적으로 또는 γ-blocker 요법과 함께 MFS [22]병리학의 대동맥 근경 변화율을 감소시킬 수 있다.
「 」를 참조해 주세요.
메모들
이 기사의 2018년 버전은 외부 전문가에 의해 이중 출판 모델로 업데이트되었습니다.대응하는 학술 동료 리뷰 기사는 Gene에 게재되었으며 다음과 같이 인용할 수 있다. Lynn Y Sakai; Douglas R Keene; Marjolijn Renard; Julie De Backer (17 July 2016). "FBN1: The disease-causing gene for Marfan syndrome and other genetic disorders". Gene. Gene Wiki Review Series. 591 (1): 279–291. doi:10.1016/J.GENE.2016.07.033. ISSN 0378-1119. PMC 6639799. PMID 27437668. Wikidata Q38903109. |
레퍼런스
- ^ a b c GRCh38: 앙상블 릴리즈 89: ENSG00000166147 - 앙상블, 2017년 5월
- ^ a b c GRCm38: 앙상블 릴리즈 89: ENSMUSG000027204 - 앙상블, 2017년 5월
- ^ "Human PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ "Mouse PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ a b Biery NJ, Eldadah ZA, Moore CS, Stetten G, Spencer F, Dietz HC (February 1999). "Revised genomic organization of FBN1 and significance for regulated gene expression". Genomics. 56 (1): 70–7. doi:10.1006/geno.1998.5697. PMID 10036187.
- ^ Faivre L, Gorlin RJ, Wirtz MK, Godfrey M, Dagoneau N, Samples JR, Le Merrer M, Collod-Beroud G, Boileau C, Munnich A, Cormier-Daire V (January 2003). "In frame fibrillin-1 gene deletion in autosomal dominant Weill-Marchesani syndrome". Journal of Medical Genetics. 40 (1): 34–6. doi:10.1136/jmg.40.1.34. PMC 1735272. PMID 12525539.
- ^ Romere C, Duerrschmid C, Bournat J, Constable P, Jain M, Xia F, Saha PK, Del Solar M, Zhu B, York B, Sarkar P, Rendon DA, Gaber MW, LeMaire SA, Coselli JS, Milewicz DM, Sutton VR, Butte NF, Moore DD, Chopra AR (April 2016). "Asprosin, a Fasting-Induced Glucogenic Protein Hormone". Cell. 165 (3): 566–79. doi:10.1016/j.cell.2016.02.063. PMC 4852710. PMID 27087445.
- ^ Jacquinet A, Verloes A, Callewaert B, Coremans C, Coucke P, de Paepe A, Kornak U, Lebrun F, Lombet J, Piérard GE, Robinson PN, Symoens S, Van Maldergem L, Debray FG (April 2014). "Neonatal progeroid variant of Marfan syndrome with congenital lipodystrophy results from mutations at the 3' end of FBN1 gene". European Journal of Medical Genetics. 57 (5): 230–4. doi:10.1016/j.ejmg.2014.02.012. PMID 24613577.
- ^ Ramachandra CJ, Mehta A, Guo KW, Wong P, Tan JL, Shim W (2015). "Molecular pathogenesis of Marfan syndrome". International Journal of Cardiology. 187: 585–91. doi:10.1016/j.ijcard.2015.03.423. PMID 25863307.
- ^ Quondamatteo F, Reinhardt DP, Charbonneau NL, Pophal G, Sakai LY, Herken R (December 2002). "Fibrillin-1 and fibrillin-2 in human embryonic and early fetal development". Matrix Biology. 21 (8): 637–46. doi:10.1016/s0945-053x(02)00100-2. PMID 12524050.
- ^ a b Votteler M, Berrio DA, Horke A, Sabatier L, Reinhardt DP, Nsair A, Aikawa E, Schenke-Layland K (June 2013). "Elastogenesis at the onset of human cardiac valve development". Development. 140 (11): 2345–53. doi:10.1242/dev.093500. PMC 3912871. PMID 23637335.
- ^ Ammash NM, Sundt TM, Connolly HM (January 2008). "Marfan syndrome-diagnosis and management". Current Problems in Cardiology. 33 (1): 7–39. doi:10.1016/j.cpcardiol.2007.10.001. PMID 18155514.
- ^ a b c Summers KM, Nataatmadja M, Xu D, West MJ, McGill JJ, Whight C, Colley A, Adès LC (November 2005). "Histopathology and fibrillin-1 distribution in severe early onset Marfan syndrome". American Journal of Medical Genetics. Part A. 139 (1): 2–8. doi:10.1002/ajmg.a.30981. PMID 16222666.
- ^ a b c d e f g h i von Kodolitsch Y, Robinson PN (June 2007). "Marfan syndrome: an update of genetics, medical and surgical management". Heart. 93 (6): 755–60. doi:10.1136/hrt.2006.098798. PMC 1955191. PMID 17502658.
- ^ Loeys BL, Dietz HC, Braverman AC, Callewaert BL, De Backer J, Devereux RB, Hilhorst-Hofstee Y, Jondeau G, Faivre L, Milewicz DM, Pyeritz RE, Sponseller PD, Wordsworth P, De Paepe AM (July 2010). "The revised Ghent nosology for the Marfan syndrome". Journal of Medical Genetics. 47 (7): 476–85. doi:10.1136/jmg.2009.072785. hdl:1854/LU-1013955. PMID 20591885.
- ^ a b c d Bergman R, Nevet MJ, Gescheidt-Shoshany H, Pimienta AL, Reinstein E (August 2014). "Atrophic skin patches with abnormal elastic fibers as a presenting sign of the MASS phenotype associated with mutation in the fibrillin 1 gene". JAMA Dermatology. 150 (8): 885–9. doi:10.1001/jamadermatol.2013.10036. PMID 24740214.
- ^ a b c d e f g h i j k l m n Martínez-Quintana E, Rodríguez-González F, Garay-Sánchez P, Tugores A (August 2014). "A novel fibrillin 1 gene mutation leading to marfan syndrome with minimal cardiac features". Molecular Syndromology. 5 (5): 236–40. doi:10.1159/000358846. PMC 4188161. PMID 25337071.
- ^ Sakai LY, Keene DR, Engvall E (December 1986). "Fibrillin, a new 350-kD glycoprotein, is a component of extracellular microfibrils". The Journal of Cell Biology. 103 (6 Pt 1): 2499–509. doi:10.1083/jcb.103.6.2499. PMC 2114568. PMID 3536967.
- ^ Smallridge RS, Whiteman P, Werner JM, Campbell ID, Handford PA, Downing AK (April 2003). "Solution structure and dynamics of a calcium binding epidermal growth factor-like domain pair from the neonatal region of human fibrillin-1". The Journal of Biological Chemistry. 278 (14): 12199–206. doi:10.1074/jbc.M208266200. PMID 12511552.
- ^ a b c d Benke K, Ágg B, Szilveszter B, Tarr F, Nagy ZB, Pólos M, Daróczi L, Merkely B, Szabolcs Z (2013). "The role of transforming growth factor-beta in Marfan syndrome". Cardiology Journal. 20 (3): 227–34. doi:10.5603/CJ.2013.0066. PMID 23788295.
- ^ a b Dietz HC (October 2007). "2006 Curt Stern Award Address. Marfan syndrome: from molecules to medicines". American Journal of Human Genetics. 81 (4): 662–7. doi:10.1086/521409. PMC 2227916. PMID 20529617.
- ^ a b c d e f g h i j k l m Matt P, Schoenhoff F, Habashi J, Holm T, Van Erp C, Loch D, Carlson OD, Griswold BF, Fu Q, De Backer J, Loeys B, Huso DL, McDonnell NB, Van Eyk JE, Dietz HC (August 2009). "Circulating transforming growth factor-beta in Marfan syndrome". Circulation. 120 (6): 526–32. doi:10.1161/CIRCULATIONAHA.108.841981. PMC 2779568. PMID 19635970.
- ^ Chaudhry SS, Cain SA, Morgan A, Dallas SL, Shuttleworth CA, Kielty CM (January 2007). "Fibrillin-1 regulates the bioavailability of TGFbeta1". The Journal of Cell Biology. 176 (3): 355–67. doi:10.1083/jcb.200608167. PMC 2063961. PMID 17242066.
- ^ a b c d e f Katz KW, Greathead MM, Cook RC, Britz R (June 1976). "Experiences in the diagnosis of brucellosis in dairy cows". Journal of the South African Veterinary Association. 47 (2): 97–100. PMID 940103.
- ^ Keene DR, Jordan CD, Reinhardt DP, Ridgway CC, Ono RN, Corson GM, Fairhurst M, Sussman MD, Memoli VA, Sakai LY (August 1997). "Fibrillin-1 in human cartilage: developmental expression and formation of special banded fibers". The Journal of Histochemistry and Cytochemistry. 45 (8): 1069–82. doi:10.1177/002215549704500805. PMID 9267468.
- ^ Charbonneau NL, Carlson EJ, Tufa S, Sengle G, Manalo EC, Carlberg VM, Ramirez F, Keene DR, Sakai LY (August 2010). "In vivo studies of mutant fibrillin-1 microfibrils". The Journal of Biological Chemistry. 285 (32): 24943–55. doi:10.1074/jbc.M110.130021. PMC 2915730. PMID 20529844.
- ^ a b c Barrett PM, Topol EJ (January 2013). "The fibrillin-1 gene: unlocking new therapeutic pathways in cardiovascular disease". Heart. 99 (2): 83–90. doi:10.1136/heartjnl-2012-301840. PMID 22942299.
- ^ Asgari, S; Luo, Y; Akbari, A; Belbin, GM; Li, X; Harris, DN; Selig, M; Bartell, E; Calderon, R; Slowikowski, K; Contreras, C; Yataco, R; Galea, JT; Jimenez, J; Coit, JM; Farroñay, C; Nazarian, RM; O'Connor, TD; Dietz, HC; Hirschhorn, JN; Guio, H; Lecca, L; Kenny, EE; Freeman, EE; Murray, MB; Raychaudhuri, S (June 2020). "A positively selected FBN1 missense variant reduces height in Peruvian individuals". Nature. 582 (7811): 234–239. doi:10.1038/s41586-020-2302-0. PMC 7410362. PMID 32499652.
- ^ "FBN1 fibrillin 1". Entrez Gene.
- ^ 온라인 Mendelian In Man (OMIM) : FIBRYLIN 1; FBN1 - 134797
- ^ Buchan JG, Alvarado DM, Haller GE, Cruchaga C, Harms MB, Zhang T, Willing MC, Grange DK, Braverman AC, Miller NH, Morcuende JA, Tang NL, Lam TP, Ng BK, Cheng JC, Dobbs MB, Gurnett CA (October 2014). "Rare variants in FBN1 and FBN2 are associated with severe adolescent idiopathic scoliosis". Human Molecular Genetics. 23 (19): 5271–82. doi:10.1093/hmg/ddu224. PMC 4159151. PMID 24833718.
추가 정보
- Hayward C, Brock DJ (1998). "Fibrillin-1 mutations in Marfan syndrome and other type-1 fibrillinopathies". Human Mutation. 10 (6): 415–23. doi:10.1002/(SICI)1098-1004(1997)10:6<415::AID-HUMU1>3.0.CO;2-C. PMID 9401003.
- Robinson PN, Godfrey M (January 2000). "The molecular genetics of Marfan syndrome and related microfibrillopathies". Journal of Medical Genetics. 37 (1): 9–25. doi:10.1136/jmg.37.1.9. PMC 1734449. PMID 10633129.
- Handford PA (December 2000). "Fibrillin-1, a calcium binding protein of extracellular matrix". Biochimica et Biophysica Acta (BBA) - Molecular Cell Research. 1498 (2–3): 84–90. doi:10.1016/s0167-4889(00)00085-9. PMID 11108952.
- Robinson PN, Booms P, Katzke S, Ladewig M, Neumann L, Palz M, Pregla R, Tiecke F, Rosenberg T (September 2002). "Mutations of FBN1 and genotype-phenotype correlations in Marfan syndrome and related fibrillinopathies". Human Mutation. 20 (3): 153–61. doi:10.1002/humu.10113. PMID 12203987.
- Adès LC, Holman KJ, Brett MS, Edwards MJ, Bennetts B (April 2004). "Ectopia lentis phenotypes and the FBN1 gene". American Journal of Medical Genetics. Part A. 126A (3): 284–9. doi:10.1002/ajmg.a.20605. PMID 15054843.
- Milewicz DM, Dietz HC, Miller DC (March 2005). "Treatment of aortic disease in patients with Marfan syndrome". Circulation. 111 (11): e150-7. doi:10.1161/01.CIR.0000155243.70456.F4. PMID 15781745.
- Boileau C, Jondeau G, Mizuguchi T, Matsumoto N (May 2005). "Molecular genetics of Marfan syndrome". Current Opinion in Cardiology. 20 (3): 194–200. doi:10.1097/01.hco.0000162398.21972.cd. PMID 15861007.
- Whiteman P, Hutchinson S, Handford PA (2006). "Fibrillin-1 misfolding and disease". Antioxidants & Redox Signaling. 8 (3–4): 338–46. doi:10.1089/ars.2006.8.338. PMID 16677079.
외부 링크
- Marfan Syndrome에 대한 Gene Reviews/NCBI/NIH/UW 엔트리
- PDB for UniProt: P35555(Fibrillin-1)에서 PDBe-KB에 있는 모든 구조 정보의 개요.