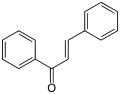
α,β-불포화 카르보닐 화합물
α,β-Unsaturated carbonyl compound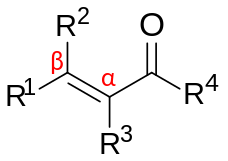
R2&R은4 단일 수소일 수도 있습니다.
α,β-불포화 카르보닐 화합물은 일반 구조(O=CR)-C=C-R을 갖는 유기 화합물입니다. 이러한 화합물에는 에논 및 에날 뿐만 아니라 카르복실산 및 해당 에스테르 및 아미드도 포함됩니다. 이들 화합물에서 카르보닐기는 알켄과 결합합니다(따라서 형용사 불포화). 측면 알켄기가 없는 카르보닐의 경우와 달리 α,β-불포화 카르보닐 화합물은 β-탄소에서 친핵체의 공격을 받기 쉽습니다. 이러한 반응성의 패턴을 바이닐로고스라고 합니다. 불포화 카르보닐의 예로는 아크롤레인(프로펜알), 메시틸 옥사이드, 아크릴산, 말레산 등이 있습니다. 불포화 카르보닐은 실험실에서 알돌 반응과 퍼킨 반응으로 제조될 수 있습니다.
분류
α,β-불포화 카르보닐 화합물은 카르보닐기와 알켄기의 성질에 따라 분류될 수 있습니다.
- 모체 α,β-불포화 카르보닐
- 가장 간단한 α,β-불포화 알데히드인 아크롤레인
- α,β-불포화 에스테르인 메틸 아크릴레이트
- 아크릴아미드, 폴리아크릴아미드의 전구체
- 말레산, α,β-불포화 디카르보닐
- 푸마르산, 말레산 이성질체
아크릴로일기

α,β-불포화 카르보닐 화합물은 말단인 알켄 또는 비닐에 결합된 카르보닐을 포함하는 아크릴로일기(HC=CH-C(=O)-); 및 아크릴산으로부터 유도된 아실기. 그룹에 선호되는 IUPAC 이름은 prop-2-에노일이며, 아크릴 또는 아크릴로 간단히(그리고 부정확하게) 알려져 있습니다. 아크릴로일 그룹을 포함하는 화합물은 "아크릴 화합물"로 지칭될 수 있습니다.
α,β-불포화산, 에스테르 및 아미드
α,β-불포화산은 카르복실산에 결합된 알켄으로 이루어진 α,β-불포화 카르보닐 화합물의 한 종류입니다.[3] 가장 간단한 예는 아크릴산(CH=CHCOH)입니다. 이들 화합물은 중합되기 쉬워 폴리아크릴레이트 플라스틱의 넓은 영역을 형성합니다. 아크릴레이트 폴리머는 아크릴레이트 그룹에서 파생되었지만 아크릴레이트 그룹을 포함하지 않습니다.[4] 아크릴산의 카르복실기는 암모니아와 반응하여 아크릴아미드를 형성하거나, 알코올과 반응하여 아크릴레이트 에스테르를 형성할 수 있습니다. 아크릴아미드 및 메틸 아크릴레이트는 각각 α,β-불포화 아미드 및 α,β-불포화 에스테르의 상업적으로 중요한 예입니다. 또한 쉽게 중합됩니다. 아크릴산, 그 에스테르 및 아미드 유도체는 아크릴로일 그룹을 특징으로 합니다.
α,β-불포화 디카르보닐도 흔합니다. 모체 화합물은 말레산과 이성질체 푸마르산입니다. 말레산은 에스테르, 이미드 및 무수물, 즉 디에틸 말레에이트, 말레이미드 및 무수말레산을 형성합니다. 푸마르산은 푸마르산염으로서 크렙스 시트르산 회로의 중간생성물로서 바이오에너지에서 매우 중요합니다.
에노스
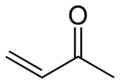
아네논()은 알켄과 케톤 작용기를 모두 포함하는 유기 화합물입니다. α,β-불포화 에논에서, 알켄은 케톤의 카르보닐기에 결합됩니다.[3] 가장 간단한 에논은 메틸 비닐 케톤(부테논, CH=CHCOCH)입니다. 에논은 일반적으로 알돌 응축 또는 Knoevenagel 응축을 사용하여 제조됩니다. 아세톤의 축합에 의해 생성되는 일부 상업적으로 중요한 에논은 메시틸 옥사이드(아세톤의 다이머)와 포론 및 이소포론(삼량체)입니다.[5] 마이어-슈스터 재배열에서 출발 화합물은 프로파길 알코올입니다. α,β-불포화 카르보닐에 접근하는 또 다른 방법은 셀레노옥사이드 제거를 통한 것입니다. 고리형 에논은 Pauson-Khand 반응을 통해 제조될 수 있습니다.

고리형 에논
사이클릭 에논은 사이클로프로페논, 사이클로부테논,[6] 사이클로펜테논, 사이클로헥세논 및 사이클로헵테논을 포함합니다.[7]
에널스
에날(또는 알케날)은 알켄과 알데히드 작용기를 모두 포함하는 유기 화합물입니다. α,β-불포화 에날에서, 알켄은 알데히드의 카르보닐기(포르밀기)에 결합됩니다.[3] 가장 간단한 에날은 crolein(CH=CHCHO)입니다. 다른 예로는 시스-3-헥세날( 깎은 잔디의 진액)과 신남알데히드(계피의 진액)가 있습니다.
- 기타 α,β-불포화 카르보닐
- 이성질체로 존재하는 에날인 E-Crotonaldehyde
- 시클로헥세논, 커먼 사이클릭 에논
- 남성 성호르몬인 테스토스테론
- 계피의 진액인 계피알데히드
- 파라퀴논, 특히 친전자성 α,β-불포화 카르보닐
- 철 트리카르보닐의 에논 복합체
α,β-불포화 카르보닐의 반응
α,β-불포화 카르보닐은 카르보닐 탄소와 β-탄소 모두에서 친전자성을 갖습니다. 조건에 따라 두 부위 모두 친핵체의 공격을 받습니다. 알켄에 첨가하는 것을 컨쥬게이트 첨가라고 합니다. 접합체 첨가의 한 가지 유형은 메시틸 옥사이드를 이소포론으로 전환하는 데 상업적으로 사용되는 미카엘 첨가입니다. α,β-불포화 카르보닐은 그들의 확장된 접합 때문에 중합되기 쉽습니다. 산업 규모 면에서 중합은 α,β-불포화 카르보닐의 사용을 지배합니다. α,β-불포화 카르보닐의 알켄 부분은 그들의 친전자성 특성 때문에 Diels-Alder 반응에서 좋은 다이에노필(dienophil)입니다. 이들은 카르보닐 산소와 결합하는 루이스 산에 의해 더욱 활성화될 수 있습니다. α,β-불포화 카르보닐은 저가 금속 착물에 대한 우수한 리간드로서, 예를 들어 Fe(bda)(CO)3 및 트리스(디벤질리덴아세톤) 디팔라듐(0)을 들 수 있습니다.
α,β-불포화 카르보닐은 쉽게 수소화됩니다. 수소화는 카르보닐 또는 알켄(복합체 환원)을 선택적으로 표적화하거나 또는 두 작용기 모두를 표적화할 수 있습니다.
에논은 나자로프 고리화 반응과 라우후트-커리어 반응(이량체화)을 겪습니다.
α,β-불포화 티오에스테르
α,β-불포화 티오에스테르는 여러 효소 과정에서 중간생성물입니다. 두 가지 두드러진 예는 쿠마로일-코엔자임 A와 크로토닐-코엔자임 A입니다. 이들은 아실-CoA 탈수소효소의 작용에 의해 발생합니다.[8] 플라빈 아데닌 디뉴클레오티드(FAD)는 필수 보조 인자입니다.

안전.
α,β-불포화 화합물은 친전자체 및 알킬화제이기 때문에 많은 α,β-불포화 카르보닐 화합물이 독성이 있습니다. 내인성 스캐빈저 화합물 글루타티온은 체내 독성 전기영동으로부터 자연스럽게 보호합니다. 티올기를 포함하는 일부 약물(아미포스틴, N-아세틸시스테인)은 이러한 유해한 알킬화로부터 보호할 수 있습니다.
참고 항목
참고문헌
- ^ Patai, Saul; Rappoport, Zvi, eds. (1989). Enones: Vol. 1 (1989). Patai's Chemistry of Functional Groups. doi:10.1002/9780470772218. ISBN 9780470772218.
- ^ Patai, Saul; Rappoport, Zvi, eds. (1989). Enones: Vol. 2 (1989). Patai's Chemistry of Functional Groups. doi:10.1002/9780470772225. ISBN 9780470772225.
- ^ a b c Smith, Michael B.; March, Jerry (2007), Advanced Organic Chemistry: Reactions, Mechanisms, and Structure (6th ed.), New York: Wiley-Interscience, ISBN 978-0-471-72091-1
- ^ Ohara, Takashi; Sato, Takahisa; Shimizu, Noboru; Prescher, Günter; Schwind, Helmut; Weiberg, Otto; Marten, Klaus; Greim, Helmut (2003). "Acrylic Acid and Derivatives". Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002/14356007.a01_161.pub2.
- ^ Siegel, Hardo; Eggersdorfer, Manfred (2000). "Ketones". Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002/14356007.a15_077.
- ^ A. G. Ross, X. Li, S. J. Danishefsky (2012). "Preparation of Cyclobutenone". Organic Syntheses. 89: 491. doi:10.15227/orgsyn.089.0491.
{{cite journal}}: CS1 maint: 다중 이름: 저자 목록 (링크) - ^ Y. Ito, S. Fujii, M. Nakatuska, F. Kawamoto,T. Saegusa (1979). "One-Carbon Ring Expansion of Cycloalkanones to Conjugated Cycloalkenones: 2-Cyclohepten-1-One". Organic Syntheses. 59: 113. doi:10.15227/orgsyn.059.0113.
{{cite journal}}: CS1 maint: 다중 이름: 저자 목록 (링크) - ^ Thorpe C, Kim JJ (June 1995). "Structure and mechanism of action of the acyl-CoA dehydrogenases". FASEB Journal. 9 (9): 718–25. doi:10.1096/fasebj.9.9.7601336. PMID 7601336. S2CID 42549744.