과산화바륨
Barium peroxide | |
 | |
| 이름 | |
|---|---|
| IUPAC 이름 과산화바륨 | |
| 기타 이름 이산화바륨, 이산화바륨 | |
| 식별자 | |
3D 모델(JSmol) | |
| 켐스파이더 | |
| ECHA InfoCard | 100.013.754 |
| EC 번호 |
|
펍켐 CID | |
| RTECS 번호 |
|
| 유니 | |
| UN 번호 | 1449 |
CompTox 대시보드 (EPA) | |
| |
| |
| 특성. | |
| BAO2 | |
| 어금질량 | 169.33 g/㎥(무수) 313.45 (옥타하이드레이트) |
| 외관 | 회색-흰색 결정체(무수) 무색 고체(옥타하이드레이트) |
| 냄새 | 무취의 |
| 밀도 | 5.68 g/cm3 (무수) 2.292 g/cm3 (옥타하이드레이트) |
| 녹는점 | 450°C(842°F, 723K) |
| 비등점 | 800 °C(1,470 °F; 1,070 K) (BaO & O.[1]와2 비교) |
| 무수성의 0.091 g/100 mL(20°C) 팔하이드레이트 0.155g/cm3 | |
| 용해성 | 산에서 분해하여 용해하다. |
자기 감수성(magnetic susibility) | -40.6·10cm−63/190cm |
| 구조 | |
| 4각형 | |
| D174h, I4/mm, tI6 | |
| 6 | |
| 위험 | |
| GHS 라벨 표시: | |
  | |
| 경고 | |
| H272, H302, H332 | |
| P210, P220, P221, P261, P264, P270, P271, P280, P301+P312, P304+P312, P304+P340, P312, P330, P370+P378, P501 | |
| NFPA 704(화재 다이아몬드) | |
달리 명시된 경우를 제외하고, 표준 상태(25°C [77°F], 100 kPa)의 재료에 대한 데이터가 제공된다. | |
| Infobox 참조 자료 | |
과산화바륨은 BaO라는2 공식을 가진 무기 화합물이다. 이 백색 고체(불순할 때의 회색)는 가장 흔한 무기 과산화물 중 하나로, 과산화수소 화합물이 최초로 발견된 것이다. 산화제로서 발화시 선명한 녹색의 색상을 주는 것(모든 바륨 화합물처럼)은 불꽃놀이에 어느 정도 사용된다는 것을 발견한다; 역사적으로 과산화수소의 전구체로도 사용되었다.[3]
구조
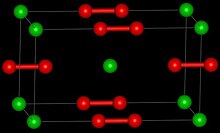
과산화바륨은 과산화수소로서 O 서브유닛을2−
2 함유하고 있다. 고체는 탄화칼슘, CaC와2 이형이다.
준비 및 사용
과산화바륨은 O와2 산화바륨의 가역반응에 의해 발생한다. 과산화물은 약 500 °C를 형성하고 산소는 820 °C 이상에서 방출된다.[1]
- 22 BaO + O ⇌ 2 BaO2
이 반응은 대기와 산소를 분리하기 위한 현재 유기체 브린 공정의 기초가 된다. NaO와2 SrO와 같은 다른 산화물은 비슷하게 행동한다.[4]
또 다른 구식 응용에서 과산화바륨은 한때 황산과의 반응을 통해 과산화수소를 생산하는데 사용되었다.[3]
- BaO2 + HSO24 → HO22 + BaaS4
불용성 황산바륨은 혼합물에서 걸러진다.
각주
- ^ a b 그룹 II Monoxides의 과잉 산소 수용 - S.C. Middleburg, R.W. Grimes 및 K.P.D. Lagerlof Journal of American Ceramic Society 2013, 권 96, 308–311. doi:10.111/j.155-2916-2012.05452.x
- ^ Massalimov, I. A.; Kireeva, M. S.; Sangalov, Yu. A. (2002). "Structure and Properties of Mechanically Activated Barium Peroxide". Inorganic Materials. 38 (4): 363–366. doi:10.1023/A:1015105922260.
- ^ a b Harald Jakob; Stefan Leininger; Thomas Lehmann; Sylvia Jacobi; Sven Gutewort. "Peroxo Compounds, Inorganic". Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002/14356007.a19_177.pub2.
- ^ Holleman, A.F.; Wiberg, E. "In 유기화학" 학술언론: 샌디에이고, 2001. ISBN 0-12-352651-5.



