사포바이러스
Sapovirus| 삿포로 바이러스 | |
|---|---|
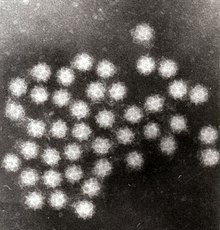 | |
| 삿포로 바이러스의 전송 전자 마이크로그래프 | |
| 바이러스 분류 | |
| (랭킹되지 않음): | 바이러스 |
| 영역: | 리보비리아 |
| 킹덤: | 오르토나비라과 |
| 망울: | 피수비리코타 |
| 클래스: | 피소니비리케테스 |
| 순서: | 피코르나비르목 |
| 패밀리: | 칼리시비루스과 |
| 속: | 사포바이러스 |
| 종: | 삿포로 바이러스 |
사포바이러스는 칼리시비르과(Calicivirae)과에 속하는 단일 가닥 양감 RNA, 비개발 바이러스의 유전적으로 다양한 속이다.[1][2] 노로바이러스와 함께 사포바이러스는 인간과 다른 동물에서 급성 위장염(인플루엔자와는 관련이 없지만 흔히 '스토마치 독감'으로 불린다)의 가장 흔한 원인이다.[3][4] 그것은 삿포로 바이러스 한 종만을 포함하고 있는 단형의 세손이다.[5]
바이러스의 자연적인 숙주는 인간과 돼지다. 그 바이러스는 구강/구강 접촉을 통해 전염된다. 사포바이러스는 어린이와 유아에게 가장 흔하게 발생하기 때문에 탁아소나 탁아소에서 자주 퍼지지만 장기요양시설에서 발견되고 있다.[6] 개인위생과 위생대책이 미흡한 탓일 수 있다. 가장 흔히 나타나는 증상은 설사와 구토를 포함한다.[7] 이 사포바이러스는 1977년 일본 삿포로시의 한 고아원에서 발생한 위장염에서 처음 발견됐다.[8]
전송 경로 및 호스트 민감성
사포바이러스는 분변/구강 경로를 통해 전파된다. 감염된 사람은 10 입자/그램 이상의 배설물이나 구토를 배출한다. 감염된 개인의 입자는 수 년 동안 생존할 수 있으며 감염 선량은 10개 미립자 정도일 수 있다. 작업면, 손 등의 오염은 엄청난 수의 새로운 감염을 일으킬 수 있다. 감염자가 구토할 때 입자가 에어로졸링되거나, 감염자가 구토한 뒤 변기가 붉어지는 등 입자를 흡입하면 감염이 발생할 수 있다. 다른 전송 형태로는 감염된 개인이 음식을 과도하게 취급하는 것(이것은 식당 환경에서 가장 흔히 발생한다), 감염된 배설물에 오염된 물에 사는 조개류의 소비, 오염된 물의 섭취 등이 있다.[9]
증상
잠복기가 1~4일이 지나면 병의 징후가 나타나기 시작한다. 사포바이러스의 증상은 노로바이러스와 매우 유사하다. 가장 흔한 증상은 구토와 설사인데 추가 증상이 나타날 수도 있다. 이러한 것들은 오한, 메스꺼움, 두통, 복통, 근통 등 매우 드물다. 1~4일 잠복기가 지나면 증상이 나타나기 시작하는 경우가 가장 많지만, 개인은 증상이 없는 경우도 있었다. 개인이 증상을 보이지는 않지만 일반 전염 방식인 구강변통로를 통해 바이러스를 전파할 수 있는 능력은 여전하다.[3]
예방
사포바이러스를 예방하는 가장 중요한 방법은 일반 위생이다. 이것은 화장실 사용 후, 그리고 음식을 먹거나 준비하기 전에 손을 완전히 씻으면 된다. 오염된 표면은 소독제 및 표백제를 함유한 용액으로 세척해야 한다. 다른 예방 조치로는 접촉을 피하고 감염된 개인과 음료/음식을 공유하는 것이 있다.
병원 설정에서
- 감염 환자는 격리하고 감염된 직원은 업무정지 조치를 취해야 한다.
- 침대 팬 와셔는 주의하여 작업할 수 있도록 주의하고 교육해야 한다.
- 극단적인 사태가 일어나려면 "신입생에 대한 병동 폐쇄가 필요할 수도 있다"고 말했다.
- "피해를 입은 병동에서 영향을 받지 않는 병동으로 이동하는 것은 금지되어야 한다. 단체 활동은 중단되고 어린이들의 방문은 금지되어야 한다.[9]
치료
사포바이러스에 감염된 개인을 위한 특별한 약은 없다. 사포바이러스는 세균 감염이 아니기 때문에 항생제로 치료할 수 없다. 치료에는 개인을 재하수하는 등의 증상지원이 포함된다.[9]
바이러스 분류
구조와 게놈
사포바이러스는 크기가 약 7.7kb인 비개발, 양성감, 단일 가닥 RNA 바이러스다. 그 바이러스는 3'끝 폴리(A)꼬리를 가지고 있지만 5'모자는 가지고 있지 않다. 사포바이러스는 180 서브유닛(T=3)을 함유한 이코사시드 구조를 갖고 있다. 캡시드의 직경은 27~40nm이다.[10] 다른 칼리시바이러스와 마찬가지로 사포바이러스의 캡시드는 표면에 둥근 의도를 가지고 있다. 그러나, 그것의 "다비드의 별" 표면 형태학은 그것을 다른 칼리시비루스와 구별한다.[3]
사포바이러스의 게놈은 잘 알려진 2개의 (아마도 3개의) 개방형 독서 프레임(ORF)으로 구성된다. ORF1은 비구조적 단백질과 VP1의 주 캡시드 단백질을 위한 인코딩이다. VP1에는 셸(S)과 돌출(P)의 두 가지 표준 도메인이 있다. S단백질의 기능은 "핵산 주위에 비계를 형성"하는 반면, P단백질은 "수용체와 함께 호모디머"를 형성하는데 중요하다.[11] 부구조 다단백질용 ORF2 인코딩, VP2. 제3의 ORF(ORF3)에 대한 예측은 있었지만, 그 기능이 무엇인지에 대한 증거는 없다.[3]
사포바이러스에 대한 최소 21개의 완전한 게놈은 이미 분석되고 확인되었으며, 이 모든 게놈은 5개의 범주(GI-GV)로 분류할 수 있으며, 이는 더 나아가 다른 유전자 군집으로 나눌 수 있다. 5개 그룹 중 4개 그룹(GI, GII, GIV, GV)이 인간을 감염시킬 수 있으며 이 4개 그룹은 항원적으로 구별되는 사포바이러스의 4개 변종인 삿포로, 휴스턴, 런던, 스톡홀름에 해당한다.[9] 이 바이러스의 유전자형은 적어도 21개가 있지만, 새로운 유전자형은 미국, 아시아, 유럽에서 계속 보고되고 있다.[12]
| 속 | 구조 | 대칭 | 캡시드 | 게놈 배열 | 게놈 분할 |
|---|---|---|---|---|---|
| 사포바이러스 | 이코사헤드랄 | T=3 | 개발되지 않음 | 선형 | 단층석 |
실험실 진단
핵산 검출법
역변환-PCR(RT-PCR)은 반응성, 민감성, 속도, 특수성이 뛰어나 사포바이러스에 가장 많이 사용되는 검출 툴이다. 사포바이러스의 다양성 때문에, RNA 의존성 RNA 폴리머라아제를 구체적으로 조준하고 증폭시키기 위해 수백 개의 프라이머가 설계되었다. 이는 "사포바이러스를 부분적으로 특성화하고 검출된 사포바이러스의 유사성을 조사하기 위해 사용할 수 있다.[3]
바이러스 입자 검출
"사포바이러스는 전자현미경 아래 대표적인 '다비드의 별' 표면 형태학으로 다른 위장염 병원체(예: 노로바이러스, 로타바이러스, 아스트로바이러스, 아데노바이러스)와 형태학적으로 구별할 수 있다. 그러나 이는 핵산 검출 방법에 비해 감도가 낮다."[3]
항원검출법
효소연계 면역항암제(ELISA)는 임상 검체에서 인간 사포바이러스를 검출하는 데 사용되어 왔다. ELISA는 인간의 사포바이러스 항원을 검출하는 데 사용될 수 있지만, 일반적으로는 사용되지 않는다. 사포바이러스의 많은 변종의 다양성으로 인해 존재할 수 있는 광범위한 항원을 검출하기가 어렵다. 왜냐하면 항원이 너무 많기 때문에 ELISA는 핵산 검출 방법만큼 정확하거나 민감하지 않기 때문이다.[3]
복제 주기
사포바이러스의 정확한 복제 주기는 결정되지 않았지만, 다른 캘리시바이러스가 표시하는 것과 같거나 유사한 세포질 복제 주기가 있는 것으로 생각된다. 세포질 복제 주기는 다음과 같다.
- 숙주세포로의 진입은 숙주수용체에 부착함으로써 이루어지는데, 숙주세포로 바이러스의 내분포를 매개한다.
- 바이러스 유전체 RNA의 코팅을 풀고 세포질 속으로 방출한다.
- VPg는 바이러스성 RNA에서 제거되고, 그 다음 복제 단백질을 산출하기 위해 가공된 ORF1 다단백질로 변환된다.
- 복제는 바이러스성 공장에서 일어난다. dsRNA 게놈은 게놈 ssRNA(+)로부터 합성된다.
- dsRNA 게놈은 기록/복제되어 바이러스성 mRNA/새로운 ssRNA(+) 게놈을 제공한다.
- 아유전자 RNA번역은 캡시드 단백질과 VP2를 발생시킨다.
- 새로운 바이러스 입자의 조립 및 세포 투석에 의한 방출."[10]
역사
전자현미경을 이용한 이 사포바이러스는 1977년 영국의 설사를 일으키는 대변 샘플에서 처음 발견되었고 곧 위장염 병원체로 알려졌다. 이 바이러스는 영국에서 처음 발견된 반면, "사포바이러스의 원형 변종은 1982년 일본 삿포로에서 또 다른 발생에서 비롯되었다."[3] 사포바이러스의 최초의 완전한 게놈은 1993년 영국의 맨체스터 변종에서 해석되었다. 이전에는 사포바이러스가 "사포로 유사 바이러스"라고 불렸으나, 2002년에는 칼리시비르과에서 삿포로 바이러스, 속주 사포바이러스로 바뀌었다. "현재 칼리시비르과는 사포바이러스, 노로바이러스, 라고바이러스, 베시바이러스, 네보바이러스 등 5개의 기성생물로 구성되어 있다."[3]
발생
2013년 12월
뉴질랜드 기스본병원에서 사포바이러스 감염 양성 반응이 나왔다. 직원 2명이 추가로 발견됐고 5명이 추가로 격리됐다. 병원 직원들은 방에 들어갈 때 신변 보호를 통해 예방 조치를 취했다.[8]
2007년 6월
타이베이 카운티의 한 대학 교직원 55명이 사포바이러스 감염 진단을 받았다.
장기요양시설 2002-2009
연구진은 오리건 주와 미네소타 주 공중보건부 자료를 이용해 20022009년 2161건의 위장염 발생을 조사했다. 이 중 142개(7%)가 노로바이러스 음성 판정을 받았고, 이 중 93개에서 사포바이러스, 아스트로바이러스, 아데노바이러스, 로타바이러스 등 기타 위장관 바이러스가 추가 검사됐으며, 21개(23%)에서 사포바이러스가 확인됐으며, 66%가 장기요양시설에서 발생했다. 이 중 절반 가까이가 2007년에만 발생했다." 연구진은 또 장기요양시설에서 발생하는 사포바이러스의 비중은 높지만 법적으로 의무화된 발병 보고의 유물이 될 가능성이 높다고 설명한다.[6]
관련 질병
노로바이러스는 사포바이러스와 가장 흔히 연관된다. 노로바이러스와 사포바이러스 게놈은 매우 밀접하게 연관되어 있어, 둘의 구별은 코딩 전략과 판독 프레임의 차이에서만 이루어질 수 있다. 노로비루스는 (사포비루스와 함께) 위장염의 가장 흔한 원인이므로 서로 같은 증상을 보인다.[13]
아스트로바이러스는 사포바이러스와 마찬가지로 어린이와 노약자, 특히 면역억제자 등에 위장염을 유발한다. 사포바이러스는 2개의 ORF가 있는 반면 아스트로바이러스는 3개가 있고 6개의 재조합성 균주가 있다. 아스트로바이러스는 세포질 내에서 복제되며 GI 트랙에서 쉽게 전파된다.[9]
노로바이러스, 아스트로바이러스, 사포바이러스와 같은 로타바이러스는 위장염을 유발한다. 그러나 로타바이러스는 훨씬 더 치명적이어서 전세계 어린이 사망자의 37%와 21만5000명의 사망자를 발생시킨다.[14]
동물바이러스
사포비루스는 박쥐, 캘리포니아 바다 사자, 개, 돼지, 밍크에서 발견되었다.[15][16]
참조
- ^ Vinjé, J; Estes, MK; Esteves, P; Green, KY; Katayama, K; Knowles, NJ; L'Homme, Y; Martella, V; Vennema, H; White, PA; ICTV Report Consortium (November 2019). "ICTV Virus Taxonomy Profile: Caliciviridae". The Journal of General Virology. 100 (11): 1469–1470. doi:10.1099/jgv.0.001332. PMC 7011698. PMID 31573467.
- ^ "ICTV Report Caliciviridae".
- ^ a b c d e f g h i Oka, Tomoichiro; Wang, Qiuhong; Katayama, Kazuhiko; Saif, Linda J. (1 January 2015). "Comprehensive Review of Human Sapoviruses". Clinical Microbiology Reviews. 28 (1): 32–53. doi:10.1128/CMR.00011-14. ISSN 0893-8512. PMC 4284302. PMID 25567221.
- ^ Razizadeh, Mohammad Hossein; Khatami, Alireza; Zarei, Mohammad (8 October 2021). "Global molecular prevalence and genotype distribution of Sapovirus in children with gastrointestinal complications: A systematic review and meta‐analysis". Reviews in Medical Virology. doi:10.1002/rmv.2302.
- ^ "Virus Taxonomy: 2018b Release". International Committee on Taxonomy of Viruses (ICTV). March 2019. Retrieved 1 May 2019.
- ^ a b Lee, Lore E.; Cebelinski, Elizabeth A.; Fuller, Candace; Keene, William E.; Smith, Kirk; Vinjé, Jan; Besser, John M. (2012). "Sapovirus Outbreaks in Long-Term Care Facilities, Oregon and Minnesota, USA, 2002–2009". Emerging Infectious Diseases. 18 (5): 873–876. doi:10.3201/eid1805.111843. PMC 3358050. PMID 22516204.
- ^ "Virus Page". web.stanford.edu. Retrieved 5 November 2017.
- ^ a b "ProMED-mail". www.promedmail.org. Retrieved 2 November 2017.
- ^ a b c d e Barer, Mike (17 January 2011). "Caliciviruses and Astroviruses". In Greenwood, David (ed.). Medical Microbiology: A Guide to Microbial Infections: pathogenesis, immunity, laboratory diagnosis and control. pp. 579–586.
- ^ a b "Viral Zone". ExPASy. Retrieved 15 June 2015.
- ^ Miyazaki, Naoyuki; Taylor, David W.; Hansman, Grant S.; Murata, Kazuyoshi (1 March 2016). "Antigenic and Cryo-Electron Microscopy Structure Analysis of a Chimeric Sapovirus Capsid". Journal of Virology. 90 (5): 2664–2675. doi:10.1128/JVI.02916-15. ISSN 0022-538X. PMC 4810723. PMID 26699644.
- ^ Tsinda, Emmanuel Kagning; Malasao, Rungnapa; Furuse, Yuki; Gilman, Robert H.; Liu, Xiaofang; Apaza, Sonia; Espetia, Susan; Cama, Vitaliano; Oshitani, Hitoshi (26 October 2017). "Complete Coding Genome Sequences of Uncommon GII.8 Sapovirus Strains Identified in Diarrhea Samples Collected from Peruvian Children". Genome Announcements. 5 (43): e01137–17. doi:10.1128/genomeA.01137-17. ISSN 2169-8287. PMC 5658493. PMID 29074655.
- ^ Farkas, T.; Zhong, W. M.; Jing, Y.; Huang, P. W.; Espinosa, S. M.; Martinez, N.; Morrow, A. L.; Ruiz-Palacios, G. M.; Pickering, L. K. (1 July 2004). "Genetic diversity among sapoviruses". Archives of Virology. 149 (7): 1309–1323. doi:10.1007/s00705-004-0296-9. ISSN 0304-8608. PMID 15221533. S2CID 35990669.
- ^ Tate, Jacqueline E.; Burton, Anthony H.; Boschi-Pinto, Cynthia; Parashar, Umesh D.; World Health Organization–Coordinated Global Rotavirus Surveillance Network (1 May 2016). "Global, Regional, and National Estimates of Rotavirus Mortality in Children". Clinical Infectious Diseases. 62 Suppl 2: S96–S105. doi:10.1093/cid/civ1013. ISSN 1537-6591. PMID 27059362.
- ^ Meng XJ (January 2012). "Emerging and Re-emerging Swine Viruses". Transboundary and Emerging Diseases. 59: 85–102. doi:10.1111/j.1865-1682.2011.01291.x. PMID 22225855.
- ^ Tse H, Chan WM, Li KS, Lau SK, Woo PC, Yuen KY(2012) 특이한 유전학적 특징과 혈전학적 위치를 가진 새로운 박쥐 사포바이러스의 발견과 유전학적 특성화. PLoS One 7(4):e34987.



