인데네
Indene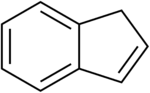 | |
 | |
| 이름 | |
|---|---|
| 선호 IUPAC 이름 1H-인덴[1] | |
| 기타 이름 벤조시클로펜타디엔 인도나프테네 자전거[4.3.0]nona-1,3,5,7-테트라엔 | |
| 식별자 | |
3D 모델(JSmol) | |
| 635873 | |
| 체비 | |
| 켐벨 | |
| 켐스파이더 | |
| 드러그뱅크 | |
| ECHA InfoCard | 100.002.176 |
| EC 번호 |
|
| 27265 | |
| 케그 | |
펍켐 CID | |
| 유니 | |
CompTox 대시보드 (EPA) | |
| |
| |
| 특성. | |
| C9H8 | |
| 어금질량 | 116.16 |
| 외관 | 무색액[2] |
| 밀도 | 0.997 g/mL |
| 녹는점 | -1.8°C(28.8°F, 271.3K) |
| 비등점 | 181.6°C(358.9°F, 454.8K) |
| 불용성 | |
| 산도(pKa) | 20.1(DMSO에서)[3] |
자기 감수성(magnetic susibility) | -80.89×10cm−63/cm |
| 위험 | |
| 산업안전보건(OHS/OSH): | |
주요 위험 | 인화성 |
| 플래시 포인트 | 78.3°C(172.9°F, 351.4K) |
| NIOSH(미국 건강 노출 제한): | |
PEL(허용) | 없는[2] |
REL(권장) | TWA 10ppm(45mg/m3)[2] |
IDLH(즉시 위험) | N.D.[2] |
| 관련 화합물 | |
관련 화합물 | 벤조푸란, 벤조티오페네, 인도엘레 |
달리 명시된 경우를 제외하고, 표준 상태(25°C [77°F], 100 kPa)의 재료에 대한 데이터가 제공된다. | |
| Infobox 참조 자료 | |
인데네는 화학 공식 CH를 가진98 인화성 다순환 탄화수소다.그것은 사이클로펜틴 링과 결합된 벤젠 링으로 구성되어 있다.이 향기로운 액체는 비록 샘플이 종종 옅은 노란색이지만 무색이다.인덴의 주요 산업 용도는 인덴/쿠마론 열가소성 수지 생산에 있다.대체 인데네와 밀접하게 연관된 인데네 유도체는 설린닥과 같은 많은 천연물과 생물학적으로 활성 분자에서 발견되는 중요한 구조적 모티브다.[4]
격리
인데네는 약 175–185 °C에서 끓는 콜타르 분율에서 자연적으로 발생한다.이 분수를 나트륨으로 가열하여 고체 "소디오-인덴"을 침전시키면 얻을 수 있다.이 단계는 나트륨에 의한 디프로토닝에 의해 증명된 인덴의 약한 산성을 이용하여 인데닐 분해를 제공한다.탄산음료는 증기 증류에 의해 다시 인덴으로 전환된다.[5]
반응도
인덴은 쉽게 중합된다.인덴을 산성 디크롬산염으로 산화시키면 호모프탈산(o-carboxylphenylacetic acid)이 발생한다.에산화나트륨이 있는 곳에서 디에틸옥살산염으로 응축하여 인덴-옥살산 에스테르를 형성하고 알칼리가 있는 곳에서는 알데히드나 케톤을 함유하여 벤조풀베네스를 형성하는데, 이 색상은 색감이 매우 높다.인덴을 유기석 시약으로 처리하면 리튬 인데닐 화합물이 나온다.
- C9H8 + RLi → LiC9H7 + RH
인데닐은 유기농 화학에 있어서 리간드로 많은 전이 금속 인데닐 콤플렉스를 발생시킨다.[6]
참고 항목
참조
- ^ International Union of Pure and Applied Chemistry (2014). Nomenclature of Organic Chemistry: IUPAC Recommendations and Preferred Names 2013. The Royal Society of Chemistry. p. 207. doi:10.1039/9781849733069. ISBN 978-0-85404-182-4.
- ^ a b c d NIOSH Pocket Guide to Chemical Hazards. "#0340". National Institute for Occupational Safety and Health (NIOSH).
- ^ Bordwell FG (1988). "Equilibrium acidities in dimethyl sulfoxide solution". Accounts of Chemical Research. 21 (12): 456–463. doi:10.1021/ar00156a004. DMSO의 Bordwell pKa 테이블 Wayback Machine에 2008-10-09 보관
- ^ Wu, Jie; Qiu, Guanyinsheng (2014). "Generation of Indene Derivatives by Tandem Reactions". Synlett. 25 (19): 2703–2713. doi:10.1055/s-0034-1379318.
- ^ Collin, Gerd; Mildenberg, Rolf; Zander, Mechthild; Höke, Hartmut; McKillip, William; Freitag, Werner; Imöhl, Wolfgang. "Resins, Synthetic". Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH.
- ^ O'Connor, Joseph M.; Casey, Charles P. (1987). "Ring-Slippage Chemistry of Transition Metal Cyclopentadienyl and Indenyl Complexes". Chemical Reviews. 87 (2): 307–318. doi:10.1021/cr00078a002.
외부 링크
- W. v. Miller, Rohde (1890). "Zur Synthese von Indenderivaten". Berichte der Deutschen Chemischen Gesellschaft. 23 (2): 1881–1886. doi:10.1002/cber.18900230227.
- W. v. Miller, Rohde (1890). "Zur Synthese von Indenderivaten". Berichte der Deutschen Chemischen Gesellschaft. 23 (2): 1887–1902. doi:10.1002/cber.18900230228.
- Finar, I. L. (1985). Organic Chemistry. Longman Scientific & Technical. ISBN 0-582-44257-5.

