페로케늄 테트라플루오보토스
Ferrocenium tetrafluoroborate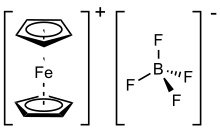 | |
 | |
 | |
| 이름 | |
|---|---|
| 기타 이름 디시클로펜타디엔틸철 테트라플루오보토스 | |
| 식별자 | |
3D 모델(JSmol) | |
| 켐스파이더 | |
| ECHA InfoCard | 100.156.161 |
펍켐 CID |
|
CompTox 대시보드 (EPA) | |
| |
| 특성. | |
| C10H10BFeF4 | |
| 어금질량 | 272.84 g/mb |
| 외관 | 검푸른 가루 |
| 녹는점 | 178 °C(352 °F; 451 K) (손상) |
| 아세토나이트릴에서의 용해성 | 수용성[citation needed] |
| 위험[1] | |
| GHS 라벨 표시: | |
 | |
| 위험 | |
| H314 | |
| P280, P305+P351+P338, P310 | |
| 안전 데이터 시트(SDS) | 외부 MSDS |
| 관련 화합물 | |
관련 화합물 | 페로센 |
달리 명시된 경우를 제외하고, 표준 상태(25°C [77°F], 100 kPa)의 재료에 대한 데이터가 제공된다. | |
| Infobox 참조 자료 | |
페로케늄 테트라플루오보토오보트는 [Fe(CH55)]2BF라는4 공식을 가진 유기농 화합물이다. 이 소금은 양이온[Fe(CH55)]2+과 사불화 음이온(BF−
4)으로 구성된다. 관련 헥사플루오로인산염도 비슷한 성질을 가진 인기 시약이다. cation은 흔히 Fc+ 또는 CpFe로2+ 축약된다. 소금은 짙은 청색과 파라자성이 있다. 페로세늄염은 일렉트로닉 산화제로 쓰이기도 하는데, 줄어든 제품인 페로센은 불활성화 되어 이온성 제품에서 쉽게 분리된다. 페로센-페로세늄 커플은 종종 전기 화학에서 참조로 사용된다. 페로센-페로세늄의 표준 전위는 일반 수소 전극(NHE)[2] 대비 0.400V이며 종종 다른 용매 사이에 불변성인 것으로 가정된다.
준비
상업적으로 이용 가능한 이 화합물은 일반적으로 철염으로 페로센을 산화시킨 후 플루오르산을 첨가하여 제조할 수 있다.[3] 니트로실 테트라플루오로보토와 같은 다양한 산화제들도 잘 작용한다.[4] 많은 유사 페로세늄 염류가 알려져 있다.[5]
참조
- ^ "Ferrocenium tetrafluoroborate 482358". Sigma-Aldrich.
- ^ Bard, A.J.; Parsons, R.; Jordan, J. (1985). Standard Potentials in Aqueous Solution. New York: IUPAC.
- ^ Connelly, N. G.; Geiger, W. E. (1996). "Chemical Redox Agents for Organometallic Chemistry". Chem. Rev. 96 (2): 877–910. doi:10.1021/cr940053x. PMID 11848774.
- ^ Nielson, Roger M.; McManis, George E.; Safford, Lance K.; Weaver, Michael J. (1989). "Solvent and electrolyte effects on the kinetics of ferrocenium-ferrocene self-exchange. A reevaluation". J. Phys. Chem. 93 (5): 2152. doi:10.1021/j100342a086.
- ^ Le Bras, J.; Jiao, H.; Meyer, W. E.; Hampel, F.; Gladysz, J. A. (2000). "Synthesis, Crystal Structure, and Reactions of the 17-Valence-Electron Rhenium Methyl Complex [(η5-C5Me5)Re(NO)(P(4-C6H4CH3)3)(CH3)]+ B(3,5-C
6H
3(CF
3)
2)−
4: Experimental and Computational Bonding Comparisons with 18-Electron Methyl and Methylidene Complexes". J. Organomet. Chem. 616: 54–66. doi:10.1016/S0022-328X(00)00531-3.


