EPSP 싱타아제
EPSP synthase| EPSP 싱타아제(3인산소시크미트 1-카복시비닐전달효소) | |||||||||
|---|---|---|---|---|---|---|---|---|---|
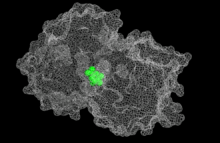 시크메이트로 묶인 EPSP 싱타아제.[1] | |||||||||
| 식별자 | |||||||||
| EC 번호 | 2.5.1.19 | ||||||||
| CAS 번호. | 9068-73-9 | ||||||||
| 데이터베이스 | |||||||||
| 인텐츠 | IntEnz 뷰 | ||||||||
| 브렌다 | 브렌다 입력 | ||||||||
| 엑스퍼시 | 나이스자이메 뷰 | ||||||||
| 케그 | KEG 입력 | ||||||||
| 메타사이크 | 대사통로 | ||||||||
| 프리암 | 프로필 | ||||||||
| PDB 구조 | RCSB PDB PDBe PDBsum | ||||||||
| 진 온톨로지 | 아미고 / 퀵고 | ||||||||
| |||||||||
| EPSP 싱타아제(3인산소시크미트 1-카복시비닐전달효소) | |||||||||
|---|---|---|---|---|---|---|---|---|---|
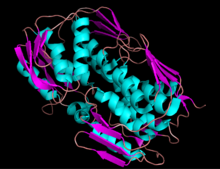 EPSP 싱타아제 리본 다이어그램 | |||||||||
| 식별자 | |||||||||
| 기호 | EPSP_synthase | ||||||||
| Pfam | PF00275 | ||||||||
| 인터프로 | IPR001986 | ||||||||
| 프로사이트 | PDOC00097 | ||||||||
| SCOP2 | 1eps / SCOPe / SUPFAM | ||||||||
| |||||||||
5-enolpyruvikimate-3-phosphate(EPSP) 신타아제는 식물과 미생물이 생산하는 효소다. EPSPS는 화학 반응을 촉진한다.
따라서 이 효소의 두 기질은 인산염(PEP)과 3-인산소시크미트(Phosphoshikimate)인 반면, 그 두 생산물은 인산염과 5-enolpyruvikimate-3-인산염이다.
이 효소는 동물에는 존재하지 않는다. 그것은 글리포세이트와 같은 제초제에 대한 매력적인 생물학적 목표를 제시한다. 이 유전자의 글리포산염 저항성 버전은 유전적으로 조작된 작물에 사용되어 왔다.
명명법
이 효소는 전이효소군에 속하는데, 이는 메틸 그룹 이외의 아릴 또는 알킬 그룹들을 옮기는 특정한 것이다. 이 효소 등급의 체계적 명칭은 인산염피루베이트:3-인산소시크메이트 5-O-(1-카복시비닐)-전달효소다. 일반적으로 사용되는 다른 이름에는 다음이 포함된다.
- 5-enolpyruvylsikimate-3-synthase,
- 3-enolpyruvylsikimate 5-synthase,
- 3-enolpyruvylsikimic acid-5-synthetase,
- 5인치-에놀피프루빌시크미트-3인치 시네타아제
- 5-enolpyruvyl-3-phosphoshikimate synthase,
- 5-enolpyruvylsicimate-3-synthetase,
- 5-enolpyruvylsicimate-3-콜로리아산 신타아제,
- 에놀피루빌시크미트리 인산염 신타아제 및
- 3-시크시크미트 1-xyxyville transferase.
구조
EPSP 싱타아제는 분자 질량이 약 46,000인 단핵 효소다.[2][3][4] 두 개의 영역으로 구성되어 있으며, 단백질 가닥으로 연결되어 있다. 이 가닥은 경첩 역할을 하며, 두 단백질 영역을 더 가깝게 만들 수 있다. 기질이 효소에 결합하면 리간드 본딩은 효소의 두 부분을 활성 부위의 기질 둘레에 옥죄게 한다.
EPSP 싱타아제는 글리포세이트 민감도에 따라 두 그룹으로 나뉜다. 식물과 일부 박테리아에 포함된 1등급 효소는 낮은 미크로폴라 글리포산염 농도에서 억제되는 반면, 다른 박테리아에서 발견된 2등급 효소는 글리포산염에 의한 억제에 내성이 있다.[5]
시크메이트 경로
EPSP 싱타아제는 박테리아, 곰팡이, 식물의 식생 경로를 통해 방향족 아미노산 페닐알라닌, 티로신, 트립토판의 생합성에 참여한다. EPSP 싱타아제는 식물과 미생물에 의해서만 생성된다; 그것에 대한 유전자 코딩은 포유류 게놈에 있지 않다.[6][7] 몇몇 동물들의 내장 식물들은 EPSPS를 함유하고 있다.[8]
반응
EPSP 싱타아제는 아세트성 사면체 중간체를 통해 식생3-인산염+인산염-인산염+인산염-인산염+인산염-인산염(EPSP)을 5-enolpyruvikimate-3-인산염(EPSP)으로 변환하는 반응을 촉진한다.[9][10] 활성 부위의 기초산과 아미노산은 각각 PEP의 히드록실 그룹의 감응과 사면체 중간 자체와 관련된 양성자 교환 단계에 관여한다.[11]
이 반응에 대한 효소 운동학에 대한 연구는 과정의 각 단계의 특정한 순서와 정력성을 결정했다.[12]
제초제 대상
EPSP 싱타아제는 제초제 글리포세이트의 생물학적 표적이다.[13] 글리포세이트는 PEP의 경쟁적 억제제로, PEP보다 EPSPS-S3P 복합체에 더 촘촘하게 결합하고 식생 경로를 억제하는 전환 상태 아날로그 역할을 한다. 이 결합은 효소의 카탈루션을 억제하고 통로를 차단한다. 결국 이것은 유기체가 생존하기 위해 필요한 방향족 아미노산의 부족으로 유기체가 죽는 결과를 낳는다.[5][14]
둘 다 글리포세이트에 내성이 있고 적절한 식물 성장을 이끌 수 있을 정도로 여전히 효율적이었던 효소의 버전이 CP4라고 불리는 아그로박테리움 변종에서 많은 시행착오를 겪은 후에 몬산토 과학자들에 의해 확인되었다. 이 변종 CP4는 글리포세이트 생산 시설의 폐식기둥에서 살아남은 것으로 밝혀졌다. CP4 EPSP 싱타아제 효소는 여러 유전적으로 조작된 작물에 의해 변형되었다.[5][15]
참조
- ^ Priestman MA, Healy ML, Funke T, Becker A, Schönbrunn E (October 2005). "Molecular basis for the glyphosate-insensitivity of the reaction of 5-enolpyruvylshikimate 3-phosphate synthase with shikimate". FEBS Lett. 579 (25): 5773–80. doi:10.1016/j.febslet.2005.09.066. PMID 16225867. S2CID 26614581.
- ^ Goldsbrough, Peter (1990). "Gene amplification in glyphosate tolerant tobacco cells". Plant Science. 72 (1): 53–62. doi:10.1016/0168-9452(90)90186-r.
- ^ Abdel-Meguid SS, Smith WW, Bild GS (Dec 1985). "Crystallization of 5-enolpyruvylshikimate 3-phosphate synthase from Escherichia coli". Journal of Molecular Biology. 186 (3): 673. doi:10.1016/0022-2836(85)90140-8. PMID 3912512.
- ^ Ream JE, Steinrücken HC, Porter CA, Sikorski JA (May 1988). "Purification and Properties of 5-Enolpyruvylshikimate-3-Phosphate Synthase from Dark-Grown Seedlings of Sorghum bicolor". Plant Physiology. 87 (1): 232–8. doi:10.1104/pp.87.1.232. PMC 1054731. PMID 16666109.
- ^ a b c Pollegioni L, Schonbrunn E, Siehl D (Aug 2011). "Molecular basis of glyphosate resistance-different approaches through protein engineering". The FEBS Journal. 278 (16): 2753–66. doi:10.1111/j.1742-4658.2011.08214.x. PMC 3145815. PMID 21668647.
- ^ Funke T, Han H, Healy-Fried ML, Fischer M, Schönbrunn E (Aug 2006). "Molecular basis for the herbicide resistance of Roundup Ready crops". Proceedings of the National Academy of Sciences of the United States of America. 103 (35): 13010–5. Bibcode:2006PNAS..10313010F. doi:10.1073/pnas.0603638103. JSTOR 30050705. PMC 1559744. PMID 16916934.
- ^ Maeda H, Dudareva N (2012). "The shikimate pathway and aromatic amino Acid biosynthesis in plants". Annual Review of Plant Biology. 63 (1): 73–105. doi:10.1146/annurev-arplant-042811-105439. PMID 22554242.
The AAA pathways consist of the shikimate pathway (the prechorismate pathway) and individual postchorismate pathways leading to Trp, Phe, and Tyr.... These pathways are found in bacteria, fungi, plants, and some protists but are absent in animals. Therefore, AAAs and some of their derivatives (vitamins) are essential nutrients in the human diet, although in animals Tyr can be synthesized from Phe by Phe hydroxylase....The absence of the AAA pathways in animals also makes these pathways attractive targets for antimicrobial agents and herbicides.
- ^ Cerdeira AL, Duke SO (2006). "The current status and environmental impacts of glyphosate-resistant crops: a review". Journal of Environmental Quality. 35 (5): 1633–58. doi:10.2134/jeq2005.0378. PMID 16899736.
- ^ "8.18.4.1.1. EPSP synthase: A tetrahedral ketal phosphate enzyme intermediate". Comprehensive Natural Products II. Chemistry and Biology. Reference Module in Chemistry, Molecular Sciences and Chemical Engineering. Vol. 8. 2010. pp. 663–688.
- ^ Anderson, Karen S.; Sammons, R. Douglas; Leo, Gregory C.; Sikorski, James A.; Benesi, Alan J.; Johnson, Kenneth A. (1990). "Observation by carbon-13 NMR of the EPSP synthase tetrahedral intermediate bound to the enzyme active site". Biochemistry. 29 (6): 1460–1465. doi:10.1021/bi00458a017. PMID 2334707.
- ^ Park, HaJeung; Hilsenbeck, Jacqueline L.; Kim, Hak Jun; Shuttleworth, Wendy A.; Park, Yong Ho; Evans, Jeremy N.; Kang, ChulHee (2004). "Structural studies of Streptococcus pneumoniae EPSP synthase in unliganded state, tetrahedral intermediate‐bound state and S3P‐GLP‐bound state". Molecular Microbiology. 51 (4): 963–971. doi:10.1046/j.1365-2958.2003.03885.x. PMID 14763973. S2CID 45549442.
- ^ Anderson, Karen S.; Sikorski, James A.; Johnson, Kenneth A. (1988). "A tetrahedral intermediate in the EPSP synthase reaction observed by rapid quench kinetics". Biochemistry. 27 (19): 7395–7406. doi:10.1021/bi00419a034. PMID 3061457.
- ^ Fonseca, Emily C. M.; da Costa, Kauê S.; Lameira, Jerônimo; Alves, Cláudio Nahum; Lima, Anderson H. (2020). "Investigation of the target-site resistance of EPSP synthase mutants P106T and T102I/P106S against glyphosate". RSC Advances. 10 (72): 44352–44360. doi:10.1039/D0RA09061A. ISSN 2046-2069.
- ^ Schönbrunn E, Eschenburg S, Shuttleworth WA, Schloss JV, Amrhein N, Evans JN, Kabsch W (Feb 2001). "Interaction of the herbicide glyphosate with its target enzyme 5-enolpyruvylshikimate 3-phosphate synthase in atomic detail". Proceedings of the National Academy of Sciences of the United States of America. 98 (4): 1376–80. Bibcode:2001PNAS...98.1376S. doi:10.1073/pnas.98.4.1376. PMC 29264. PMID 11171958.
- ^ Green JM, Owen MD (Jun 2011). "Herbicide-resistant crops: utilities and limitations for herbicide-resistant weed management". Journal of Agricultural and Food Chemistry. 59 (11): 5819–29. doi:10.1021/jf101286h. PMC 3105486. PMID 20586458.
추가 읽기
- Morell H, Clark MJ, Knowles PF, Sprinson DB (Jan 1967). "The enzymic synthesis of chorismic and prephenic acids from 3-enolpyruvylshikimic acid 5-phosphate". The Journal of Biological Chemistry. 242 (1): 82–90. doi:10.1016/S0021-9258(18)96321-0. PMID 4289188.



