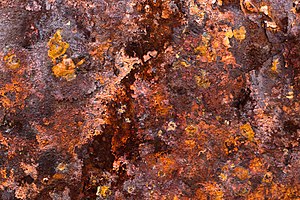녹
Rust| 강철 |
|---|
 |
| 단계 |
| 미세 구조 |
| 반 |
| 기타 철기 재료 |
녹은 산화철로, 물이나 공기 중의 수분이 촉매 작용으로 존재할 때 철과 산소가 반응하여 형성되는 보통 적갈색 산화철입니다.녹은 수성철(III) 산화물(FeO23·nHO2)과 산화철(III) 수산화물(FeO(OH), Fe(OH))3로 구성되며 일반적으로 정제철의 부식과 관련이 있습니다.
충분한 시간이 주어지면, 물과 산소가 있는 상태에서 철 덩어리는 결국 완전히 녹으로 변할 수 있다.표면 녹은 일반적으로 벗겨지고 부서지기 쉬우며 구리 표면에 패티나가 형성되는 것과 달리 기초 철에 패시브 보호 기능을 제공하지 않습니다.녹은 원소 철과 강철과 같은 그 합금의 부식을 일컫는 일반적인 용어입니다.다른 많은 금속들도 비슷한 부식을 겪지만, 그 결과 생기는 산화물을 흔히 "녹"[1]이라고 부르지는 않습니다.
녹의 여러 형태는 시각적으로나 분광학적으로나 구별할 수 있으며,[2] 다양한 환경에서 형성된다.다른 형태의 녹은 산소가 부족한 환경에서 철과 염화물 사이의 반응의 결과를 포함한다.녹색 녹을 발생시키는 수중 콘크리트 기둥에 사용되는 철근이 그 예이다.녹은 일반적으로 철의 부정적인 측면이지만, 안정된 녹으로 알려진 특정한 형태의 녹은 물체 위에 얇은 녹을 입히는 원인이 됩니다.낮은 상대 습도로 유지되면 "안정적" 층이 아래의 철에 대해 보호되지만 알루미늄 산화물([3]예: 알루미늄 산화물)의 범위에서는 보호되지 않습니다.
화학 반응


녹은 [4]철의 산화물과 수산화물 복합체의 총칭으로, 철 또는 철을 포함한 일부 합금이 산소와 습기에 장기간 노출될 때 발생합니다.시간이 지남에 따라 산소는 금속과 결합해 집단적으로 녹이라고 불리는 새로운 화합물을 형성한다.녹은 일반적으로 "산화"라고 칭할 수 있지만, 이 용어는 훨씬 더 일반적이며 반응의 일부로서 전자의 손실 또는 산화 상태의 증가를 수반하는 광범위한 과정을 설명한다.이러한 반응들 중 가장 잘 알려진 것은 산소와 관련이 있기 때문에 "산화"라는 이름이 붙습니다."녹"과 "녹"이라는 용어는 철과 그 결과 발생하는 산물의 산화만을 의미합니다.철을 포함하지 않거나 녹을 생성하지 않는 많은 산화 반응이 존재합니다.그러나 철을 함유한 철이나 합금만이 녹슬 수 있다.그러나 다른 금속들도 비슷한 방식으로 부식될 수 있다.
녹슨 과정의 주요 촉매는 물입니다.철이나 강철 구조물은 단단한 것처럼 보일 수 있지만, 물 분자는 노출된 금속의 미세한 구멍과 균열을 통과할 수 있습니다.물 분자에 존재하는 수소 원자는 산을 형성하기 위해 다른 원소와 결합할 수 있으며, 이는 결국 더 많은 금속이 노출되도록 할 것이다.염화물 이온이 존재하는 경우, 소금물처럼 부식이 더 빨리 발생할 가능성이 높다.한편, 산소 원자는 금속 원자와 결합해 파괴적인 산화물 화합물을 형성한다.원자가 결합하면서 금속을 약화시켜 구조를 부서지기 쉽게 만듭니다.
철의 산화
철분이 물과 산소와 접촉하면 녹이 [5]슬어요.바닷물이나 소금 스프레이와 같이 소금이 존재할 경우 화학 반응의 결과로 철이 더 빨리 녹슬기 쉽습니다.철금속은 순수한 물이나 건조한 산소의 영향을 받지 않습니다.알루미늄과 같은 다른 금속과 마찬가지로, 단단하게 달라붙는 산화물 코팅, 즉 수동화층은 벌크 철을 더 이상의 산화로부터 보호합니다.소극적인 산화철층이 녹으로 전환되는 것은 두 가지 물질(일반적으로 산소와 물)의 결합 작용에서 비롯됩니다.
다른 분해 용액으로는 물 속의 아황산가스와 물 속의 이산화탄소가 있다.이러한 부식 조건하에서 수산화철종이 형성된다.산화철과 달리 하이드록시드는 벌크메탈에 부착되지 않습니다.그것들이 형성되고 표면에서 벗겨지면서 신선한 철이 노출되고, 부식 과정은 철이 모두 소비되거나 시스템 내의 산소, 물, 이산화탄소 또는 아황산소가 모두 제거되거나 [6]소비될 때까지 계속됩니다.
철이 녹슬면 산화물은 원래 금속보다 더 많은 부피를 차지합니다. 이 팽창은 엄청난 힘을 발생시켜 철로 만들어진 구조물을 손상시킬 수 있습니다.자세한 내용은 경제 효과를 참조하십시오.
관련 반응
철의 녹은 전자가 철에서 [7]산소로 전달되면서 시작되는 전기화학적 과정이다.철은 환원제(전자를 포기함)이고 산소는 산화제(전자를 획득함)입니다.부식 속도는 자동차의 부식에 대한 도로염의 영향에서 알 수 있듯이 물에 의해 영향을 받고 전해질에 의해 가속화됩니다.주요 반응은 산소 감소입니다.
수산화 이온을 형성하기 때문에 이 과정은 산의 존재에 의해 강한 영향을 받습니다.마찬가지로 산소에 의한 대부분의 금속의 부식은 낮은 pH에서 가속화됩니다.상기 반응의 전자는 다음과 같이 설명될 수 있는 철의 산화입니다.
- Fe → Fe2+ + 2− e
다음과 같은 산화환원 반응도 물이 있는 경우 발생하며 녹의 형성에 매우 중요합니다.
- 42+ Fe + O2 → 43+ Fe + 2 O2−
또한 다음과 같은 다단계 산-염기 반응은 녹 형성 과정에 영향을 미칩니다.
다음과 같은 탈수 평형 상태를 수행한다.
위의 공식에서 부식 생성물은 물과 산소의 가용성에 의해 결정된다는 것도 알 수 있다.제한된 용존 산소와 함께 FeO 및 검은색 자석 또는 마그네타이트(FeO34)를 포함한 철(II) 함유 재료가 선호됩니다.높은 산소 농도는 공칭 식 Fe(OH)3−xO.mw-parser-output .frac{white-space:nowrap}.mw-parser-output.frac.num,.mw-parser-output.frac .den{:80%;line-height:0;vertical-align:슈퍼 font-size}.mw-parser-output.frac .den{vertical-align:서브}.mw-parser-output .sr-only{과 제2철 재료를 선호한다.국경:0;클립:rect(0,0,0,0), 높이:1px, 마진:-1px, 오버 플로: 숨어 있었다. 패딩:0;위치:절대, 너비:1px}x⁄2.녹의 성질은 고체의 반응 속도가 [5]느리다는 것을 반영하여 시간에 따라 변한다.
또한 이러한 복잡한 과정은 녹 형성을 촉진하는 전해질 역할을 하는 Ca와 같은 다른2+ 이온의 존재에 의해 영향을 받거나 수산화물 및 철산화물과 결합하여 다양한 Ca, Fe, O, OH종을 침전시킨다.
녹의 시작은 또한 실험실에서 페록실 지시 용액을 사용하여 검출할 수 있다.이 용액은 Fe 이온과 히드록실 이온을 모두2+ 검출한다.Fe이온 및2+ 히드록실 이온의 형성은 각각 청색, 분홍색으로 나타낸다.
예방

철과 철강 제품의 광범위한 사용과 중요성으로 인해 녹 방지 또는 둔화는 많은 전문 기술에서 주요 경제 활동의 기초가 됩니다.여기에서는 방법에 대한 간단한 개요를 설명합니다.자세한 내용은 상호 참조 문서를 참조하십시오.
녹은 공기와 물에 침투하기 때문에 녹층 아래의 내부 금속 철이 계속 부식됩니다.따라서 방청에는 녹 형성을 방지하는 코팅이 필요합니다.
방청 합금
스테인리스강은 [8][9]산화크롬(II)의 부동층을 형성한다.마그네슘, 티타늄, 아연, 산화아연, 알루미늄, 폴리아닐린 및 기타 전기 활성 전도성 [10]고분자에서도 유사한 패시베이션 동작이 발생합니다.
Cor-Ten과 같은 특수 "풍화강" 합금은 녹이 보호층의 금속 표면에 부착되기 때문에 정상 속도보다 훨씬 느린 속도로 녹이 발생합니다.이 재료를 사용하는 설계에는 재료가 거의 이상적인 [citation needed]조건에서도 여전히 느리게 녹슬기 때문에 최악의 경우 노출을 방지하는 조치가 포함되어야 한다.
아연도금
아연도금은 용융아연도금 또는 전기도금으로 금속아연층을 보호하는 대상물에 도포하는 것으로 구성된다.아연은 값싸고 강철에 잘 붙으며 아연층이 손상되었을 때 강철 표면에 음극방지를 제공하기 때문에 전통적으로 사용됩니다.부식성이 높은 환경(예: 소금물)에서는 카드뮴 도금이 선호됩니다.코팅에 틈이 있는 이음새, 구멍 및 이음새에서 아연도금이 실패하는 경우가 많습니다.이러한 경우, 코팅은 여전히 철에 대해 부분 음극 보호 기능을 제공하며, 갈바닉 양극으로 작용하고 기본 보호 금속 대신 자체적으로 부식됩니다.이 작용에 의해 보호 아연층이 소비되므로 아연도금은 제한된 시간 동안만 보호를 제공합니다.
보다 현대적인 코팅은 알루미늄을 아연-알룸으로 코팅에 추가합니다. 알루미늄은 스크래치를 커버하기 위해 이동하므로 장기간 보호 기능을 제공합니다.이러한 접근 방식은 기존의 아연도금 코팅에서처럼 희생 양극으로 산화되기보다는 긁힌 표면을 보호하는 알루미늄 및 산화 아연에 의존합니다.매우 공격적인 환경이나 긴 설계 수명과 같은 경우에 아연과 코팅이 모두 적용되어 부식 방지 기능을 강화합니다.
외부 환경에서 일상적인 풍화 과정을 거쳐야 하는 강철 제품의 일반적인 아연도금은 용융 85µm 아연 코팅으로 구성됩니다.정상적인 기상 조건에서는 연간 1µm의 속도로 악화되어 약 85년 동안 [citation needed]보호됩니다.
음극 방식
음극방식은 전기화학반응을 억제하는 전하를 공급하여 매립 또는 침지구조물의 부식을 억제하는 기술이다.올바르게 도포하면 부식을 완전히 막을 수 있습니다.가장 간단한 형태에서는 희생 양극을 부착하여 셀 내에 철 또는 강철을 음극으로 형성함으로써 실현된다.희생 양극은 일반적으로 아연, 알루미늄 또는 마그네슘과 같이 철이나 강철보다 더 많은 음극 전위를 가진 것으로 만들어야 합니다.희생 양극은 결국 부식되어 적시에 교체하지 않으면 보호 조치를 중단합니다.
인가된 전류를 사용하여 음극 보호를 제공할 수도 있습니다.이를 ICCP 인가 전류 음극 [11]방식이라고 합니다.
코팅 및 도장
녹의 형성은 페인트, 래커, 니스 또는 왁스[12] 테이프와 같은 코팅으로 제어할 수 있으며,[13] 이 코팅은 철을 환경으로부터 격리시킵니다.선박이나 현대 자동차와 같이 밀폐된 박스 섹션이 있는 대형 구조물에는 종종 왁스 기반 제품(기술적으로는 "세척유")이 이러한 섹션에 주입됩니다.이러한 처리에는 일반적으로 녹 억제제도 포함되어 있습니다.강철을 콘크리트로 피복하면 강철-콘크리트 계면의 알칼리성 pH 환경 때문에 강철을 어느 정도 보호할 수 있습니다.그러나 콘크리트 내 강철의 녹은 여전히 문제가 될 수 있다. 녹이 확장되면 콘크리트가 내부에서 [14][15]깨질 수 있기 때문이다.
1898년 그리스 아테네의 파르테논 신전을 복원하는 과정에서 철제 클램프가 대리석 블록을 접합하는 데 사용됐지만, 보호되지 않은 철이 녹슬고 부풀어 올라 대리석에 큰 손상을 입혔다.고대 그리스 건축업자들은 건축 과정에서 대리석 블록에 비슷한 고정 시스템을 사용했지만, 그들은 또한 지진 충격과 부식으로부터 보호하기 위해 녹은 납을 철 이음매 위에 부었다.이 방법은 2500년 된 이 구조물에 성공했지만, 1세기도 안 되어 원유 수리가 [16]붕괴될 위기에 처했다.

보관 또는 운송을 위해 임시 보호만 필요한 경우, 얇은 오일, 그리스 또는 Cosmoline과 같은 특수 혼합물을 철 표면에 도포할 수 있습니다.이러한 처리는 장기 보관을 위해 강철 선박, 자동차 또는 기타 장비를 "모트볼"할 때 광범위하게 사용됩니다.
특수 고착 방지 윤활제 혼합물을 사용할 수 있으며 금속 나사산 및 기타 정밀 가공 표면에 도포하여 녹으로부터 보호합니다.이러한 화합물에는 일반적으로 구리, 아연 또는 알루미늄 분말과 혼합된 그리스 및 기타 독점 [17]성분이 포함되어 있습니다.
블루잉
블루잉은 화기 등 소강재에 대해 녹슬지 않는 기술이며, 이를 위해 블루드강과 다른 강철에 물 제거 오일을 문지릅니다.
억제제
밀봉된 시스템 내부의 부식을 방지하기 위해 기상 또는 휘발성 억제제와 같은 부식 억제제를 사용할 수 있습니다.공기 순환에 의해 분산되어 신선한 산소와 수분을 가져올 때는 효과가 없습니다.
습도 조절
대기 [18]중의 수분을 조절함으로써 녹을 피할 수 있습니다.예를 들어 실리카 겔 패킷을 사용하여 해상에서 출하되는 기기의 습도를 제어하는 것이 있습니다.
치료
전기분해로 작은 철이나 강철 물체에 대한 녹 제거는 수돗물에 녹은 세정 소다로 구성된 전해질을 채운 플라스틱 버킷, 양극으로 작용하기 위해 용액에 수직으로 매달린 철근의 길이, 버킷의 상부에 걸쳐 수지로 작용하기 위한 철근 길이와 같은 간단한 재료를 사용하여 가정 작업장에서 수행할 수 있다.물체를 매달기 위한 pport, 용액 중의 물체를 수평 철근에 매달기 위한 볼링 와이어, 양극에 양극에 양극을 고정하고 음극이 되는 피처리물에 음극 [19]단자를 고정하는 전원으로서의 배터리 충전기.
녹은 녹과 결합하는 탄닌산 또는 인산을 포함하는 녹 변환기로 알려진 상업용 제품으로 처리될 수 있으며, 구연산, 식초 또는 더 강한 염산과 같은 유기산으로 제거되거나, 일부 상업용 제제 또는 [20]당밀 용액에서처럼 킬레이트제로 제거될 수 있습니다.
경제적 효과
녹은 철 기반 공구 및 구조물의 열화와 관련이 있습니다.녹은 원래 철질량보다 부피가 훨씬 높기 때문에, 녹의 축적에 의해서 인접하는 부품을 떼어내 고장도 일으킬 수 있습니다.이것은, 「녹 패킹」이라고 불리는 현상입니다.1983년 미아누스 강 다리 붕괴의 원인으로 베어링 내부가 녹슬어 도로 슬래브의 한쪽 모서리가 지지대에서 밀려났다.
녹은 1967년 웨스트버지니아에서 발생한 실버브릿지 참사의 중요한 요소였다. 당시 강철 현수교가 1분도 안 되어 붕괴되어 다리 위의 운전자와 승객 46명이 사망했다.펜실베니아 킨주아 다리는 2003년 토네이도에 의해 폭파되었는데, 이는 구조물을 지상으로 고정하는 중앙 베이스 볼트가 녹슬어 다리가 중력에 의해서만 고정되었기 때문이다.
철근콘크리트도 녹손상에 취약하다.콘크리트 피복 강재 및 철재 부식의 확대로 인한 내부 압력은 콘크리트가 분출되어 심각한 구조적 문제를 야기할 수 있습니다.철근콘크리트 교량 및 건물에서 가장 일반적인 고장 모드 중 하나입니다.
- 녹에 의한 구조적 고장
Kinzua Bridge가 무너진 후
문화적 상징성
녹은 강한 철과 강철의 금속을 점차 부드러운 분쇄 가루가 되기 때문에 방치로 인한 느린 부패를 비유하는 말로 흔히 사용됩니다.한때 철강 주조 공장, 자동차 산업 및 기타 제조업체가 지배했던 산업화된 미국 중서부와 미국 북동부의 광범위한 지역이 "러스트 벨트"로 불리게 된 혹독한 경제 삭감을 경험했습니다.
음악, 문학, 예술에서 녹은 빛바랜 영광, 무시, 부패, 그리고 파멸의 이미지와 연관되어 있다.
「 」를 참조해 주세요.
레퍼런스
- ^ "Rust, n.1 and adj". OED Online. Oxford University Press. June 2018. Retrieved 7 July 2018.
- ^ "Interview, David Des Marais". NASA. 2003. Archived from the original on 2007-11-13.
- ^ Ankersmit, Bart; Griesser-Stermscheg, Martina; Selwyn, Lindsie; Sutherland, Susanne. "Rust Never Sleeps: Recognizing Metals and Their Corrosion Products" (PDF). depotwijzer. Parks Canada. Archived (PDF) from the original on 9 August 2016. Retrieved 23 July 2016.
- ^ Sund, Robert B.; Bishop, Jeanne (1980). Accent on science. C.E. Merrill. ISBN 9780675075695. Archived from the original on 2017-11-30.
- ^ a b "Oxidation Reduction Reactions". Bodner Research Web. Retrieved 28 April 2020.
- ^ Holleman, A. F.; Wiberg, E. (2001). Inorganic Chemistry. San Diego: Academic Press. ISBN 0-12-352651-5.
- ^ Gräfen, H.; Horn, E. M.; Schlecker, H.; Schindler, H. (2000). "Corrosion". Ullmann's Encyclopedia of Industrial Chemistry. Wiley-VCH. doi:10.1002/14356007.b01_08. ISBN 3527306730.
- ^ Ramaswamy, Hosahalli S.; Marcotte, Michele; Sastry, Sudhir; Abdelrahim, Khalid (2014-02-14). Ohmic Heating in Food Processing. CRC Press. ISBN 9781420071092. Archived from the original on 2018-05-02.
- ^ Heinz, Norbert. "Corrosion prevention - HomoFaciens". www.homofaciens.de. Archived from the original on 2017-12-01. Retrieved 2017-11-30.
- ^ "Formation of stable passive film on stainless steel by electrochemical deposition of polypyrrole". Electrochimica Acta.
- ^ "Cathodic Protection Systems - Matcor, Inc". Matcor, Inc. Archived from the original on 2017-03-30. Retrieved 2017-03-29.
- ^ "Archived copy" (PDF). Archived (PDF) from the original on 2018-03-23. Retrieved 2018-03-22.
{{cite web}}: CS1 maint: 제목으로 아카이브된 복사(링크) - ^ Schweitzer, Philip A (2007). Corrosion engineering handbook. Boca Raton: CRC Press. ISBN 978-0-8493-8246-8. OCLC 137248977.
- ^ "Corrosion of Embedded Metals". cement.org. Portland Cement Association. Retrieved 9 July 2021.
- ^ "Rust Wedge: Expanding rust is a force strong enough to shatter concrete". exploratorium.edu. 17 April 2018. Retrieved 9 July 2021.
- ^ Hadingham, Evan. "Unlocking Mysteries of the Parthenon". smithsonianmag.com. Retrieved 9 July 2021.
- ^ "Anti-seize Compounds Information". globalspec.com. Engineering 360. Retrieved 9 July 2021.
- ^ Gupta, Lorraine Mirza, Krishnakali. Young Scientist Series ICSE Chemistry 7. Pearson Education India. ISBN 9788131756591. Archived from the original on 2017-11-30.
- ^ "Rust Removal using Electrolysis". antique-engines.com. Archived from the original on March 30, 2015. Retrieved April 1, 2015.
- ^ "Rust Removal with Molasses". Archived from the original on September 25, 2016. Retrieved November 29, 2017.
추가 정보
- Waldman, J. (2015):녹 - 가장 긴 전쟁.사이먼 & 슈스터, 뉴욕ISBN 978-1-4516-9159-7
- Schweitzer, Philip A. (2007). Corrosion engineering handbook. Fundamentals of metallic corrosion : atmospheric and media corrosion of metals (2 ed.). Boca Raton: CRC Press. ISBN 978-0-8493-8244-4. OCLC 137248972.
- Corrosion of reinforcement in concrete construction. C. L. Page, P. B. Bamforth, J. W. Figg, International Symposium on Corrosion of Reinforcement in Concrete Construction. Cambridge: Royal Society of Chemistry, Information Services. 1996. ISBN 0-85404-731-X. OCLC 35233292.
{{cite book}}: CS1 유지보수: 기타 (링크) - 부식 - 제2판 (elsevier.com) 제1권 및 제2권, 편집자: L L Shreir ISBN 9781483164106