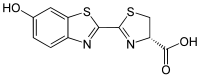
루시페린
Luciferin
|
루시페린(Luciferin, 라틴어 "light-bearer")은 생물발광을 일으키는 유기체에서 발견되는 발광 화합물의 총칭이다.루시페린은 전형적으로 산소분자와 효소촉매반응을 일으킨다.그 결과 발생하는 변환은 보통 분자 조각의 분열을 수반하며, 지면 상태로 붕괴될 때 빛을 방출하는 들뜬 상태의 중간체를 생성한다.이 용어는 루시페라아제 및 [1]광단백질의 기질인 분자를 나타낼 수 있습니다.
종류들
루시페린은 빛의 형태로 에너지를 방출하기 위해 루시페라아제(효소)의 존재 하에서 산소와 반응하는 작은 분자 기질이다.루시페린의 종류가 몇 가지인지는 알려지지 않았지만, 아래에 더 잘 연구된 화합물들이 나열되어 있다.
루시페린의 화학적 다양성 때문에, 모든 것이 분자 [2]산소를 필요로 한다는 것, 루시페린과 루시페라아제의 다양성, 그들의 다양한 반응 메커니즘과 산란된 계통학적 분포는 그들 중 많은 수가 [2]진화 과정에서 독립적으로 발생했음을 나타낸다.
반딧불
반딧불 루시페린은 많은 람피리대 종에서 발견되는 루시페린이다.이것은 반딧불이의 노란 빛을 방출하는 특징적인 역할을 하는 딱정벌레 루시페라아제(EC 1.13.12.7)의 기질이지만, 빛이 나지 않는 [3]종의 관련 효소와 교차 반응하여 빛을 낼 수 있습니다.발광에는 분자산소 외에 아데노신3인산([4]ATP)이 필요하기 때문에 화학작용이 특이하다.
달팽이
라티아 루시페린은 화학적으로 (E)-2-메틸-4-(2,6,6-트리메틸-1-시클로헥스-1-일)-1-부텐-1-ol 포름산염이며, 민물 달팽이 라티아 [5]네리토이드에서 유래한다.
세균
세균 루시페린은 생물 발광 박테리아에서 발견되는 플라빈 모노뉴클레오티드와 지방 알데히드로 이루어진 2성분 시스템이다.
실렌타진
실렌테라진은 방사선학자, ctenophores, cnidarians, 오징어, 부서지기 쉬운 별, 요각류, 채토그나스, 물고기, 그리고 새우에서 발견됩니다.그것은 청색 빛의 [6]방출을 담당하는 단백질 에이코린의 보철기이다.
쌍편모충류
디노플라겔라 루시페린은 엽록소 유도체이고 몇몇 디노플라겔라이트에서 발견되는데, 디노플라겔라이트는 종종 야간 발광 파동의 현상에 책임이 있다.비슷한 종류의 루시페린은 몇몇 종류의 읍하우스과 [7]새우에서 발견됩니다.
바구린
버글린은 특정 배척동물과 심해어, 구체적으로는 포릭티스에서 발견됩니다.화합물인 실레라진처럼 이미다조피라진이며 주로 동물들에게 푸른 빛을 방출한다.
곰팡이

폭스파이어는 썩어가는 나무에 존재하는 곰팡이들에 의해 만들어진 생물 발광이다.곰팡이의 왕국에는 여러 가지 다른 루시페린이 있을 수 있지만, 3-히드록시 히스피딘은 Neonotopanus nambi, Ompalotus [8]ollearius, Ompalotus nidiformis, Panelus stipticus를 포함한 여러 종의 곰팡이의 자실체에서 루시페린으로 결정되었다.
과학에서의 용법
이 섹션은 어떠한 출처도 인용하지 않습니다.(2022년 8월 ( 템플릿메시지를 에 대해 알아보기) |
루시페린은 생체 내 이미징의 한 방법으로 과학 및 의학 분야에서 널리 사용되며, 생체 내 이미징의 비침습적 이미지 및 분자 이미징에 생물체를 사용합니다.루시페린 기질과 수용체 효소 루시페라아제 간의 반응은 촉매 반응을 일으켜 생물 발광 작용을 일으킨다.이 반응과 생성된 발광은 암으로 인한 종양을 발견하거나 유전자 발현을 측정할 수 있는 영상촬영에 유용하다.
레퍼런스
- ^ Hastings JW (1996). "Chemistries and colors of bioluminescent reactions: a review". Gene. 173 (1 Spec No): 5–11. doi:10.1016/0378-1119(95)00676-1. PMID 8707056.
- ^ a b Hastings JW (1983). "Biological diversity, chemical mechanisms, and the evolutionary origins of bioluminescent systems". J. Mol. Evol. 19 (5): 309–21. Bibcode:1983JMolE..19..309H. doi:10.1007/BF02101634. PMID 6358519. S2CID 875590.
- ^ Viviani, V.R., Bechara, E.J.H. (1996). "Larval Tenebrio molitor (Coleoptera: Tenebrionidae) Fat Body Extracts Catalyze Firefly D-Luciferin-and ATP-Dependent Chemiluminescence: A Luciferase-like Enzyme". Photochemistry and Photobiology. 63 (6): 713–718. doi:10.1111/j.1751-1097.1996.tb09620.x. S2CID 83498776.
{{cite journal}}: CS1 maint: 여러 이름: 작성자 목록(링크) - ^ Green A, McElroy WD (October 1956). "Function of adenosine triphosphate in the activation of luciferin". Arch. Biochem. Biophys. 64 (2): 257–71. doi:10.1016/0003-9861(56)90268-5. PMID 13363432.
- ^ EC 1.14.99.21ORENZA: Orphan ENZyme 액티비티 데이터베이스, 2009년 11월 27일 접속.
- ^ Shimomura O, Johnson FH (April 1975). "Chemical nature of bioluminescence systems in coelenterates". Proc. Natl. Acad. Sci. U.S.A. 72 (4): 1546–49. Bibcode:1975PNAS...72.1546S. doi:10.1073/pnas.72.4.1546. PMC 432574. PMID 236561.
- ^ Dunlap, JC; Hastings, JW; Shimomura, O (1980). "Crossreactivity between the light-emitting systems of distantly related organisms: Novel type of light-emitting compound". Proc. Natl. Acad. Sci. U.S.A. 77 (3): 1394–97. Bibcode:1980PNAS...77.1394D. doi:10.1073/pnas.77.3.1394. PMC 348501. PMID 16592787.
- ^ Purtov KV, Petushkov VN, Baranov MS, Mineev KS, Rodionova NS, Kaskova ZM, Tsarkova AS, Petunin AI, Bondar VS, Rodicheva EK, Medvedeva SE, Oba Y, Arseniev AS, Lukyanov S, Gitelson JI, Yampolsky IV (2015). "The Chemical Basis of Fungal Bioluminescence". Angewandte Chemie International Edition. 54 (28): 8124–8128. doi:10.1002/anie.201501779. PMID 26094784.
외부 링크
- "Major luciferin types". The Bioluminescence Web Page. University of California, Santa Barbara. 2009-01-09. Retrieved 2009-03-06.