촉진 확산
Facilitated diffusion촉진 확산(촉진성 전달 또는 수동 매개 전달이라고도 함)은 특정 막간 통합 [1]단백질을 통해 생체막을 가로질러 분자 또는 이온의 자발적인 수동 전달 과정이다.수동적인 운반은 운반 단계 자체에서 직접적으로 ATP 가수분해로부터 화학 에너지를 필요로 하지 않는다; 대신, 분자와 이온은 그것의 확산 특성을 반영하여 농도 구배를 아래로 이동한다.
촉진 확산은 몇 가지 면에서 단순 확산과 다르다.
- 수송은 화물과 막-피막 채널 또는 운반 단백질 사이의 분자 결합에 의존한다.
- 촉진 확산 속도는 두 위상 간의 농도 차이에 대해 포화된다. 농도 차이에 선형인 자유 확산과는 달리.
- 활성 결합 이벤트의 존재로 인해 촉진 수송의 온도 의존성은 온도에 대한 의존성이 [2]경미한 자유 확산과 비교하여 상당히 다르다.
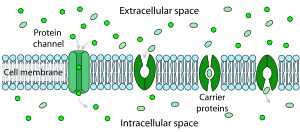
극성 분자와 물에 용해된 큰 이온은 지질 이중층을 구성하는 인지질 지방산 꼬리의 소수성 특성 때문에 플라즈마 막을 가로질러 자유롭게 확산될 수 없다.산소나 이산화탄소와 같은 극성이 아닌 작은 분자만이 쉽게 막을 통해 확산될 수 있습니다.따라서 작은 극성 분자는 막 통과 채널의 형태로 단백질에 의해 운반된다.이러한 채널은 게이트되어 있어 열리고 닫히고, 따라서 막을 가로지르는 이온이나 작은 극성 분자의 흐름을 규제하지 않으며, 때로는 삼투압 구배에 반대합니다.더 큰 분자는 투과제와 같은 트랜스막 캐리어 단백질에 의해 운반되며, 이는 분자가 운반될 때 그 구조를 변화시킨다(예: 포도당 또는 아미노산).레티놀이나 지질과 같은 비극성 분자는 물에 잘 녹지 않습니다.그것들은 수용성 운반체(예: 레티놀 결합 단백질)에 의해 세포의 수용성 구획 또는 세포외 공간을 통해 운반된다.대사물은 확산 촉진에 에너지가 필요하지 않기 때문에 변경되지 않습니다.오직 투과효소만이 대사물을 운반하기 위해 형태를 바꾼다.대사물이 변형되는 세포막을 통한 수송의 형태를 그룹 전위 수송이라고 한다.
포도당, 나트륨 이온, 염화 이온은 플라즈마 막을 효율적으로 통과해야 하지만 막의 지질 이중층이 사실상 투과되지 않는 분자와 이온의 몇 가지 예입니다.그러므로 그들의 수송은 막을 가로지르는 단백질에 의해 "촉진"되어야 하며 대체 경로 또는 우회 메커니즘을 제공해야 한다.이 과정을 매개하는 단백질의 예로는 포도당 운반체, 유기 양이온 운반 단백질, 요소 운반체, 모노카르본산 운반체 8 및 모노카르본산 운반체 10이 있다.
촉진 확산의 생체내 모델
많은 물리적 및 생화학적 과정이 [3]확산에 의해 조절된다.촉진 확산은 확산의 한 형태이며 여러 대사 과정에서 중요하다.촉진 확산은 DNA 분자의 지정된 표적 부위에 전사 인자(TF)가 결합하는 주요 메커니즘입니다.생체외에서 일어나는 매우 잘 알려진 촉진 확산 방법인 체외 모델은 세포 내에서의 3차원 확산 패턴과 DNA [4]윤곽을 따른 1차원 확산을 설명한다.세포 밖에서 발생하는 프로세스에 대한 광범위한 연구를 수행한 후, 이 메커니즘은 일반적으로 받아들여졌지만, 이 메커니즘이 생체 내 또는 살아있는 세포 내부에서 일어날 수 있는지 검증할 필요가 있었다.따라서 Bauer & Metzler(2013)[4]는 박테리아 게놈을 사용하여 TF – DNA 결합이 발생하는 평균 시간을 조사하여 실험을 수행하였다.TF가 박테리아 DNA의 윤곽과 세포질에 걸쳐 확산되는 데 걸리는 시간을 분석한 결과, TF와 DNA의 연관성과 해리율이 비슷하다는 점에서 체외와 체외가 비슷하다는 결론을 내렸다.또한 DNA 윤곽에서는 움직임이 느리고 표적 부위가 국소화되기 쉬운 반면 세포질에서는 움직임이 빠르지만 TF는 표적에 민감하지 않기 때문에 결합이 제한된다.
세포내 확산 촉진
단분자 이미징은 살아있는 세포의 [5]전사인자 결합 메커니즘 연구에 필요한 이상적인 해상도를 제공하는 이미징 기술입니다.대장균과 같은 원핵 박테리아 세포에서, 조절 단백질이 DNA 염기쌍의 [3][5][6]표적 부위에 위치하여 결합하기 위해서는 촉진 확산이 필요하다.관련된 두 가지 주요 단계가 있습니다: 단백질은 DNA의 비특이적인 부위에 결합하고, 그리고 나서 표적 부위를 찾을 때까지 DNA 사슬을 따라 확산되는데,[3] 슬라이딩이라고 불리는 과정입니다.Brackley et al. (2013)에 따르면 단백질 슬라이딩 과정에서 단백질은 3-D 및 1-D 확산 패턴을 사용하여 DNA 사슬의 전체 길이를 탐색한다.3D 확산 동안 크로더 단백질의 높은 발병률은 탐색자 단백질(예: Lac Repressor)을 DNA에 더 가까이 가져와 흡인력을 증가시키고 결합을 가능하게 하는 삼투압을 생성하며, 또한 이 영역(Lac 연산자 영역)에서 크로더 단백질을 제외하는 입체 효과를 생성한다.차단제 단백질은 1-D 확산에만 관여한다. 즉, 세포질이 아닌 DNA 윤곽선을 따라 결합하고 확산된다.
염색질 단백질 확산 촉진
위에서 언급한 생체내 모델은 DNA 가닥을 따라 3-D 및 1-D 확산과 사슬의 표적 부위에 대한 단백질의 결합을 명확하게 설명한다.진핵생물에서 원핵세포와 마찬가지로, 촉진 확산은 염색질 필라멘트의 핵플라스마에서 일어나며, 이는 단백질이 염색질 실에 결합되거나 핵플라스마에서 [7]자유롭게 확산될 때 단백질의 전환 역학에 의해 설명된다.또한 염색질 분자가 단편화되어 있기 때문에 그 프랙탈 특성을 고려할 필요가 있다.염색질 프랙탈 구조상의 3-D 확산상과 1-D 확산상을 번갈아 가면서 표적 단백질의 탐색시간을 계산한 결과, 진핵생물에서의 원활한 확산이 탐색과정을 촉진하고 DNA-단백질 [7]친화성을 높여 탐색시간을 최소화하는 것으로 추정됐다.
산소의 경우
적혈구 표면의 헤모글로빈과의 산소 친화력은 이러한 결합 [8]능력을 강화합니다.산소 확산 촉진 시스템에서 산소인 리간드와 헤모글로빈 또는 미오글로빈 [9]중 하나의 운반체 사이에는 밀접한 관계가 있다.헤모글로빈 또는 미오글로빈에 의한 산소의 확산 촉진 메커니즘은 비텐버그와 [10]스콜랜더에 의해 발견되고 시작되었습니다.그들은 다양한 압력에서 산소가 일정하게 확산되는 상태를 테스트하기 위한 실험을 수행했다.산소 촉진 확산은 산소 압력을 상대적으로 [11]제어할 수 있는 균질 환경에서 발생합니다.[12] 산소 확산이 일어나려면 막의 한쪽이 완전 포화 압력(더 높음)이고 다른 한쪽이 완전 감소 압력(더 낮음)이어야 합니다. 즉, 막의 한쪽이 더 높은 농도로 되어 있어야 합니다.촉진 확산 동안, 헤모글로빈은 산소의 지속적인 확산 속도를 증가시키고 옥시 헤모글로빈 분자가 무작위로 치환될 때 촉진 확산이 일어납니다.
일산화탄소용
일산화탄소의 확산 촉진은 산소와 유사하다.일산화탄소는 헤모글로빈,[12] 미오글로빈과도 결합하지만 일산화탄소는 산소보다 100배 낮은 해리속도를 보인다.산소에 비해 미오글로빈에 [13]대한 친화력은 40배, 헤모글로빈에 대한 친화력은 250배 높다.
포도당의 경우
포도당은 큰 분자이기 때문에 막 전체에 퍼지는 것이 어렵다.[14]따라서 농도 구배를 따라 확산이 촉진되어 막 전체에 확산됩니다.막에 있는 운반 단백질은 포도당에 결합하고 운반이 [15]쉽도록 모양을 바꾼다.세포 내 포도당의 이동은 막 확장 단백질의 수에 따라 빠를 수도 있고 느릴 수도 있다.그것은 세포 내의 다른 포도당 분자에 추진력을 제공하는 의존성 포도당 심포터에 의해 농도 구배에 대해 운반된다.촉진 확산은 축적된 포도당을 [15]혈관에 인접한 세포외 공간으로 방출하는 것을 돕는다.
「 」를 참조해 주세요.
레퍼런스
- ^ Pratt CA, Voet D, Voet JG (2002). Fundamentals of biochemistry upgrade. New York: Wiley. pp. 264–266. ISBN 0-471-41759-9.
- ^ Friedman, Morton (2008). Principles and models of biological transport. Springer. ISBN 978-0387-79239-2.
- ^ a b c Klenin, Konstantin V.; Merlitz, Holger; Langowski, Jörg; Wu, Chen-Xu (2006). "Facilitated Diffusion of DNA-Binding Proteins". Physical Review Letters. 96 (1): 018104. arXiv:physics/0507056. Bibcode:2006PhRvL..96a8104K. doi:10.1103/PhysRevLett.96.018104. ISSN 0031-9007. PMID 16486524. S2CID 8937433.
- ^ a b Bauer M, Metzler R (2013). "In vivo facilitated diffusion model". PLOS ONE. 8 (1): e53956. arXiv:1301.5502. Bibcode:2013PLoSO...853956B. doi:10.1371/journal.pone.0053956. PMC 3548819. PMID 23349772.
- ^ a b Hammar, P.; Leroy, P.; Mahmutovic, A.; Marklund, E. G.; Berg, O. G.; Elf, J. (2012). "The lac Repressor Displays Facilitated Diffusion in Living Cells". Science. 336 (6088): 1595–1598. Bibcode:2012Sci...336.1595H. doi:10.1126/science.1221648. ISSN 0036-8075. PMID 22723426. S2CID 21351861.
- ^ Brackley CA, Cates ME, Marenduzzo D (September 2013). "Intracellular facilitated diffusion: searchers, crowders, and blockers". Phys. Rev. Lett. 111 (10): 108101. arXiv:1309.1010. Bibcode:2013PhRvL.111j8101B. doi:10.1103/PhysRevLett.111.108101. PMID 25166711. S2CID 13220767.
- ^ a b Bénichou O, Chevalier C, Meyer B, Voituriez R (January 2011). "Facilitated diffusion of proteins on chromatin". Phys. Rev. Lett. 106 (3): 038102. arXiv:1006.4758. Bibcode:2011PhRvL.106c8102B. doi:10.1103/PhysRevLett.106.038102. PMID 21405302. S2CID 15977456.
- ^ Kreuzer, F. (1970). "Facilitated diffusion of oxygen and its possible significance; a review". Respiration Physiology. 9 (1): 1–30. doi:10.1016/0034-5687(70)90002-2. ISSN 0034-5687. PMID 4910215.
- ^ Jacquez JA, Kutchai H, Daniels E (June 1972). "Hemoglobin-facilitated diffusion of oxygen: interfacial and thickness effects" (PDF). Respir Physiol. 15 (2): 166–81. doi:10.1016/0034-5687(72)90096-5. hdl:2027.42/34087. PMID 5042165.
- ^ Rubinow SI, Dembo M (April 1977). "The facilitated diffusion of oxygen by hemoglobin and myoglobin". Biophys. J. 18 (1): 29–42. Bibcode:1977BpJ....18...29R. doi:10.1016/S0006-3495(77)85594-X. PMC 1473276. PMID 856316.
- ^ Kreuzer F, Hoofd LJ (May 1972). "Factors influencing facilitated diffusion of oxygen in the presence of hemoglobin and myoglobin". Respir Physiol. 15 (1): 104–24. doi:10.1016/0034-5687(72)90008-4. PMID 5079218.
- ^ a b Wittenberg JB (January 1966). "The molecular mechanism of hemoglobin-facilitated oxygen diffusion". J. Biol. Chem. 241 (1): 104–14. doi:10.1016/S0021-9258(18)96964-4. PMID 5901041.
- ^ Murray JD, Wyman J (October 1971). "Facilitated diffusion. The case of carbon monoxide". J. Biol. Chem. 246 (19): 5903–6. doi:10.1016/S0021-9258(18)61811-3. PMID 5116656.
- ^ Thorens B (1993). "Facilitated glucose transporters in eithelial cells". Annu. Rev. Physiol. 55: 591–608. doi:10.1146/annurev.ph.55.030193.003111. PMID 8466187.
- ^ a b Carruthers, A. (1990). "Facilitated diffusion of glucose". Physiological Reviews. 70 (4): 1135–1176. doi:10.1152/physrev.1990.70.4.1135. ISSN 0031-9333. PMID 2217557.