5배 결합
Quintuple bond화학에서 5중 결합은 특이한 형태의 화학 결합으로 2005년에 디크롬 화합물에 대해 처음 보고되었습니다.단결합, 이중결합, 삼중결합은 화학에서 흔히 볼 수 있다.4중 결합은 더 드물지만 현재 전이 금속, 특히 Cr28, 4−Mo, W 및 Re(2−예: [MoCl] 및 [ReCl28])에서만 알려져 있습니다.5중 결합에서는 10개의 전자가 두 금속 중심 사이의 결합에 참여하며, δδ로 할당된다244.
금속 원자 간의 고차 결합의 경우, 금속-금속 결합은 두 금속 중심을 연결하고 원자 간 거리를 감소시키는 리간드에 의해 촉진된다.반면 5중 결합을 가진 크롬 이합체는 부피가 큰 테르페닐(2,6-[(2,6-디이소프로필)페닐]페닐) 리간드에 의해 안정화된다.이 종은 200 °[1][2]C까지 안정적입니다.크롬-크롬 5중 결합은 다기준 및 DFT [3]방법으로 분석되었으며, 이는 측면 아릴이 크롬 원자와 매우 약하게 상호작용하여 5중 [4]결합의 약화를 야기하는 것으로 나타난 테르페닐 배위자의 역할을 설명하는 데에도 사용되었다.2007년 이론 연구에서는 5중 결합 RMMR 화합물에 대한 두 가지 글로벌 최소값이 확인되었습니다. 즉, R 치환기가 브리지 [5]위치에 있는 트랜스벤트 분자 기하학과 놀랍게도 또 다른 트랜스벤트 기하학입니다.
2005년, 계산 [6][7]화학에 기초한 가상의 우라늄 분자2 U에 5중 결합이 존재한다고 가정했다.디우라늄 화합물은 드물지만, UCl 음이온과
22−
8 같이 존재합니다.
2007년에 가장 짧은 금속-금속 결합(180.28pm)이 디아자디엔 가교 리간드와 [8]함께 5중 크롬-크롬 결합을 포함하는 화합물에도 존재하는 것으로 보고되었다.보고된 다른 금속-금속 5중 결합에는 [6-(2,4,6-트라이소프로필페닐)피리딘-2-일](2,4,6-트리메틸페닐)아민 가교[9] [10]리간드를 가진 5중 결합 디크롬 복합체와 아미드 가교 리간드가 포함된다.
5중 결합의 합성은 보통 칼륨 흑연을 이용한 2중 결합의 감소를 통해 이루어진다.이것은 금속 중심부에 원자가 전자를 추가하여 5중 결합에 참여하는 데 필요한 수의 전자를 제공합니다.다음은 전형적인 5중 결합 합성의 그림이다.
디몰리브덴 5중 결합
2009년에는 5중 결합과 2개의 디아미도 브리지 리간드를 가진 디몰리브덴 화합물이 202pm의 [11]Mo-Mo 결합 길이로 보고되었다.화합물은 옥타클로로디몰리브덴산칼륨(이미 Mo 4중 결합 포함2)과 리튬아미딘산염에서 합성된 후 흑연칼륨으로 환원되었다.
본딩
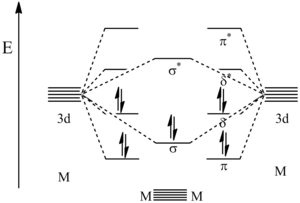
앞에서 설명한 바와 같이 금속-금속 5중 결합의 구성은 δδ이다244.금속중심 사이에 존재하는 5개의 결합 중 하나는 시그마 결합, 2개는 파이 결합, 2개는 델타 결합이다.γ 결합은 각 금속 중심에서 dz2 오비탈을 혼합한 결과입니다.첫 번째 γ 결합은 각 금속의 d 오비탈yz 혼합에서 오는 반면, 다른 γ 결합은 각 금속 혼합의 d 오비탈에서xz 오는 것이다.마지막으로 γ 결합은 dxy 오비탈의 혼합뿐만 아니라 각 금속으로부터의x2−y2 d 오비탈 간의 혼합에서 비롯된다.
분자 궤도 계산은 이러한 결합 상호작용에 의해 생성된 궤도의 상대적 에너지를 설명했습니다.아래 그림과 같이 가장 낮은 에너지 오비탈은 δ 결합 오비탈에 이어 δ 결합 오비탈입니다.다음으로 높은 것은 HOMO를 나타내는 δ결합궤도입니다.금속들의 10개의 원자가 전자가 처음 5개의 궤도를 채우기 위해 사용되기 때문에 다음으로 높은 오비탈은 δ* 반결합궤도인 LUMO가 됩니다.θ와 θ 오비탈은 축퇴된 것으로 나타나지만 실제로는 그렇지 않다.이는 여기에 표시된 모델이 단순화된 것이며 s, p 및 d 궤도의 혼성화가 발생하여 궤도 에너지 수준의 변화를 [citation needed]일으킬 것으로 생각되기 때문입니다.
금속-금속 5중 결합 길이에서의 배위자 역할
5중 결합 길이는 금속 중심에 결합된 리간드에 크게 의존합니다.금속-금속 5중 결합을 포함하는 거의 모든 복합체는 쌍방향 브리지 리간드를 가지며, 앞에서 언급한 테르페닐 복합체와 같이 그렇지 않은 복합체도 금속-ipso-탄소 상호작용을 통해 일부 브리지 특성을 가진다.
이원배위자는 킬레이트화 발생을 위해 금속 원자가 서로 더 가깝게 움직여야 하기 때문에 5중 결합 길이를 단축할 수 있습니다.짧은 금속-금속 거리를 얻는 두 가지 방법은 구조를 변화시킴으로써 배위자에서 킬레이트 원자 사이의 거리를 줄이거나, 또는 킬레이트 원자를 서로 더 가깝게 만드는 방식으로 분자를 구부리는 배위자의 구조 변화를 강제하는 입체 효과를 사용하는 것이다.후자의 예를 다음에 나타냅니다.
위의 예는 앞에서 설명한 디몰리브덴 복합체에 사용된 배위자를 나타낸다.배위자에 있는 두 니트로겐 사이의 탄소에 수소가 결합되어 있으면 입체 반발이 작습니다.그러나 수소가 훨씬 더 부피가 큰 페닐 고리로 대체되면 입체 반발이 급격히 증가하고 질소 원자에 있는 외로운 전자 쌍의 방향 변화를 일으키는 배위자가 "무지개"를 일으킨다.이러한 단일한 쌍은 금속 중심과의 결합을 형성하기 때문에 금속 중심은 서로 더 가깝게 움직이게 하고 금속 중심은 서로 더 가깝게 위치하게 합니다.따라서 5배 결합의 길이를 줄입니다.이 배위자가 5중 결합 디몰리브덴에 결합되어 있는 경우, 5중 결합 길이는 페닐기로 치환되었을 때 201.87pm에서 201.57pm으로 증가한다.디크롬 5중 결합 복합체에서도 유사한 결과가 입증되었다.[12]
조사 경향
단기 5배 [13][14]채권을 준비하기 위한 노력은 계속된다.
5중 결합 디크롬 복합체는 마그네슘처럼 작용하여 그리냐드 [15]시약을 생성하는 것으로 보인다.
레퍼런스
- ^ Ritter, Steve (26 September 2005). "Quintuple Bond Makes Its Debut: First stable molecule with fivefold metal–metal bonding is synthesized". Chemical & Engineering News. 83 (39).
- ^ Nguyen, Tailuan; Sutton, Andrew D.; Brynda, Marcin; Fettinger, James C.; Long, Gary J.; Power, Philip P. (2005). "Synthesis of a Stable Compound with Fivefold Bonding Between Two Chromium(I) Centers". Science. 310 (5749): 844–847. Bibcode:2005Sci...310..844N. doi:10.1126/science.1116789. PMID 16179432. S2CID 42853922.
- ^ Brynda, Marcin; Gagliardi, Laura; Widmark, Per-Olof; Power, Philip P.; Roos, Björn O. (2006). "Quantum Chemical Study of the Quintuple Bond between Two Chromium Centers in [PhCrCrPh]: trans-Bent versus Linear Geometry". Angew. Chem. Int. Ed. 45 (23): 3804–3807. doi:10.1002/anie.200600110. PMID 16671122.

- ^ La Macchia, Giovanni; Gagliardi, Laura; Power, Philip P.; Brynda, Marcin (2008). "Large Differences in Secondary Metal−Arene Interactions in the Transition-Metal Dimers ArMMAr (Ar = Terphenyl; M = Cr, Fe, or Co): Implications for Cr−Cr Quintuple Bonding". J. Am. Chem. Soc. 130 (15): 5104–5114. doi:10.1021/ja0771890. PMID 18335988. S2CID 207046428.
- ^ Merino, Gabriel; Donald, Kelling J.; D'Acchioli, Jason S.; Hoffmann, Roald (2007). "The Many Ways To Have a Quintuple Bond". J. Am. Chem. Soc. 129 (49): 15295–15302. doi:10.1021/ja075454b. PMID 18004851. S2CID 18838267.
- ^ Gagliardi, Laura; Roos, Björn O. (24 February 2005). "Quantum chemical calculations show that the uranium molecule U2 has a quintuple bond". Nature. 433 (7028): 848–851. Bibcode:2005Natur.433..848G. doi:10.1038/nature03249. PMID 15729337. S2CID 421380.
- ^ Dumé, Belle (23 February 2005). "New look for chemical bonds". PhysicsWeb.
- ^ Kreisel, Kevin A.; Yap, Glenn P. A.; Dmitrenko, Olga; Landis, Clark R.; Theopold, Klaus H. (2007). "The Shortest Metal–Metal Bond Yet: Molecular and Electronic Structure of a Dinuclear Chromium Diazadiene Complex". J. Am. Chem. Soc. (Communication). 129 (46): 14162–14163. doi:10.1021/ja076356t. PMID 17967028.
- ^ Noor, Awal; Wagner, Frank R.; Kempe, Rhett (2008). "Metal–Metal Distances at the Limit: A Coordination Compound with an Ultrashort Chromium–Chromium Bond". Angew. Chem. Int. Ed. 47 (38): 7246–7249. doi:10.1002/anie.200801160. PMID 18698657. S2CID 30480347.
- ^ Tsai, Yi-Chou; Hsu, Chia-Wei; Yu, Jen-Shiang K.; Lee, Gene-Hsiang; Wang, Yu; Kuo, Ting-Shen (2008). "Remarkably Short Metal–Metal Bonds: A Lantern-Type Quintuply Bonded Dichromium(I) Complex". Angew. Chem. Int. Ed. 47 (38): 7250–7253. doi:10.1002/anie.200801286. PMID 18683844. S2CID 5510753.
- ^ Tsai, Yi-Chou; Chen, Hong-Zhang; Chang, Chie-Chieh; Yu, Jen-Shiang K.; Lee, Gene-Hsiang; Wang, Yu; Kuo, Ting-Shen (2009). "Journey from Mo–Mo Quadruple Bonds to Quintuple Bonds". J. Am. Chem. Soc. 131 (35): 12534–12535. doi:10.1021/ja905035f. PMID 19685872. S2CID 207144833.
- ^ Hsu, Chai-Wei; Yu, Jen-Shiang K.; Yen, Chun-Hsu; Lee, Gene-Hsiang; Wang, Yu; Tsa, Yi-Chou (2008). "Quintuply-Bonded Dichromium(I) Complexes Featuring Metal–Metal Bond Lengths of 1.74 Å". Angew. Chem. Int. Ed. 47 (51): 9933–9936. doi:10.1002/anie.200803859. PMID 19016281. S2CID 46033904.
- ^ Noor, Awal; Glatz, Germund; Muller, Robert; Kaupp, Martin; Demeshko, Serhiy; Kempe, Rhett (2009). "Carboalumination of a chromium–chromium quintuple bond". Nature Chemistry. 1 (4): 322–325. Bibcode:2009NatCh...1..322N. doi:10.1038/NCHEM.255. PMID 21500603.
- ^ Ni, Chengbao; Ellis, Bobby D.; Long, Gary J.; Power, Philip P. (2009). "Reactions of Ar′CrCrAr′ with N2O or N3(1-Ad): complete cleavage of the Cr–Cr quintuple bond interaction". Chemical Communications. 2009 (17): 2332–2334. doi:10.1039/b901494b. PMID 19377676.
- ^ Noor, Awal; Schwarz, Stefan; Kempe, Rhett (9 Feb 2015). "Low-Valent Aminopyridinato Chromium Methyl Complexes via Reductive Alkylation and via Oxidative Addition of Iodomethane by a Cr–Cr Quintuple Bond". Organometallics. 34 (11): 2122–2125. doi:10.1021/om501230g.