발파
Blastulation| 블라큘라 | |
|---|---|
 발파: 1. 모룰라에서 2. 발파까지 | |
| 세부 사항 | |
| 날들 | 4 |
| 전구체 | 모룰라 |
| 낳다 | 가스트룰라 |
| 식별자 | |
| 메슈 | D036703 |
| 해부학적 용어 | |
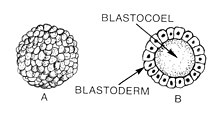
폭발은 초기의 동물 배아 발달의 단계로서 배아를 생산한다.[1]블라큘라(그리스어 βλασόςς(blastos, 싹을 뜻하는 blastos)로부터)는 내부 유체가 채워진 충치(blastomeres)를 둘러싸고 있는 속이 빈 세포(blastomeres)이다.[1][2]배아발달은 정자가 난자를 수정하여 지고테가 되는 것에서 시작되는데, 이 세포는 모룰라라고 불리는 세포덩어리로 발달하기 위해 많은 갈라진 곳을 겪는다.블라스토켈이 형성되어야 초기 배아는 블라스토콜라가 된다.배아의 배아 층이 형성되는 미식가 형성에 앞서 배아 균이 형성된다.[3]
척추동물의 공통적인 특징은 블라스토데럼으로 알려진 블라스토메르 층으로 구성되어 있으며, 블라스토멜을 둘러싸고 있다는 것이다.[4][5]포유류에서는 배반포를 배반포라고 부른다.배반포체는 결국 태아의 결정적인 구조를 만들어낼 태아(또는 내부 세포질량)와 자궁외 조직을 형성하는 영양소를 포함하고 있다.[3][6]
발파 중 세포 극성, 세포 사양, 축 형성을 설정하고 유전자 발현을 조절하기 위해 초기 배아 내에서 상당한 양의 활동이 발생한다.[7]드로소필라와 제노푸스와 같은 많은 동물에서, 중간 발파 전환(MBT)은 산모 mRNA가 저하되고 발육에 대한 통제가 배아에게 전달되는 발달의 중요한 단계다.[8]블라스토메르 사이의 많은 상호작용은 특히 포유류의 E-카데린과 양서류의 EP-카데린 등 캐더린 표현에 의존한다.[7]
발파체와 세포 사양 연구는 줄기세포 연구와 보조 생식 기술에 많은 시사점을 가지고 있다.[6]Xenopus에서, 발광체는 세포 신호에 따라 여러 경로로 이동할 수 있는 전지전능한 줄기세포로 작용한다.[9]발광 단계에서 세포 신호를 조작함으로써 다양한 조직을 형성할 수 있다.이 잠재력은 질병과 부상 사례의 재생 의학에 도움이 될 수 있다.체외 수정은 산모의 자궁에 발파제를 이식하는 것을 포함한다.[10]발파 세포 이식술은 불임을 없애는 데 도움이 될 수 있다.
개발
초기 배아발달의 배아 단계는 배아발달의 출현으로 시작된다.크세노푸스의 블라스토켈의 기원은 넓어지고 촘촘한 접합부로 밀봉되어 충치가 생기는 첫 번째 갈라진 고랑에서 나온 것으로 밝혀졌다.[11]
많은 유기체에서 배아의 발육은 이 시점까지 그리고 배아기의 초기 단계까지 모성 mRNA에 의해 조절되는데, 그것은 수정되기 전에 알에서 생산되었기 때문에 그렇게 불린다.[12][13]
미들블라스툴라 전이
Xenopus와 Drosophila를 포함한 많은 유기체에서, 중간블라스툴라 전환은 대개 특정 종의 세포 분열 후에 일어나며, 초기 발광의 동기식 세포 분열 주기의 종료와 G1과 G2 단계의 추가에 의한 세포 주기 연장에 의해 정의된다.이러한 전환 이전에 분열은 세포 주기의 합성 및 유사분열 단계에서만 발생한다.[13]두 성장 단계를 세포 주기에 추가하면 세포의 크기가 증가하는데, 이때까지 발광체는 배아의 전체 크기가 증가하지 않고 더 많은 세포가 생성되는 환원 분열을 겪게 된다.이러한 변화는 유기체의 크기 성장을 시작한다.[3]
중간 쇄골 전환은 또한 생물의 게놈에서 필사된 새로운 비문명 mRNA의 전사량이 눈에 띄게 증가한 것이 특징이다.드로소필라의[14] SMAG와 같은 단백질이나 마이크로RNA에 의해 이 시점에서 다량의 산모 mRNA가 파괴된다.[15]이 두 과정은 배아의 조절을 산모 mRNA에서 핵으로 이동시킨다.
구조
블라큘라는 블라스토켈을 둘러싸고 있는 세포의 한 영역이다.블라스토켈은 세포 분화에 필요한 아미노산, 단백질, 성장 인자, 당, 이온 및 기타 성분을 포함하는 유체 충진강이다.블라스토켈은 또한 식욕의 과정에서 블라스토메르가 움직일 수 있도록 한다.[16]
제노푸스 배아에서, 배아는 세 개의 다른 지역으로 구성되어 있다.동물 모자는 블라스토켈의 지붕을 형성하며 주로 외피 유도체를 형성한다.블라스토켈의 벽을 구성하는 적도 또는 한계 영역은 주로 중피 조직으로 분화된다.식물성 질량은 블라스토켈 바닥으로 구성되어 있으며 주로 피부 내 조직으로 발달한다.[7]
포유류 배반포에서는 나중에 조직 발달을 일으키는 세 개의 선(선)이 있다.후두엽은 태아 자체를 생기게 하고, 영양소는 태반의 일부분으로 발달하고 원시 내두엽은 노른자낭이 된다.[6]
생쥐 배아에서, 블라스토켈 형성은 32세포 단계에서 시작된다.이 과정에서 물은 삼투성 경사로 인해 배아에 유입되며, 이는 대류권 기저측면에서 높은 Na+ 경사로를 생성하는 Na+/K+ ATPases의 결과물이다.이 물의 움직임은 아쿠아포린에 의해 촉진된다.물개는 블라스토켈에 줄지어 있는 상피세포가 촘촘히 결합하여 만들어진다.[6]
세포접착
촘촘한 결합은 배아 발달에 매우 중요하다.블라큘라에서 이러한 캐더린 매개 세포 상호작용이 가장 중요한 상피세포의 개발, 세포 극성의 유지, 블라스토켈 형성을 조절하기 위한 투과성 밀봉의 생성에 필수적이다.이러한 촘촘한 접합은 상피세포의 극성이 확립된 후 발생하며, 이는 향후 개발과 규격을 위한 토대를 마련한다.블라큘라 내에서 내부 블라토메르는 일반적으로 극성이 아닌 반면 상피세포는 극성을 나타낸다.[16]
포유류 배아는 E-cadherin뿐만 아니라 알파와 베타 카테닌이 표현되는 8세포 단계를 전후해 콤프레션을 거친다.이 과정은 확산과 미분화 세포의 그룹보다는 상호작용이 가능한 배아 세포의 덩어리를 만든다.E-cadherin 접착은 발달하는 배아에서 아피코 기저축을 정의하고 배아를 불분명한 공에서 완전히 형성된 배반포체로 더 이상 발달할 수 있는 단계를 설정하는 더 분극화된 표현형으로 변화시킨다.[16]
제노푸스 막 극성은 첫 번째 세포 분열로 확립된다.양서류 EP-캐더린과 XB/U 캐더린은 포유류에서 E-캐더린과 유사한 역할을 수행하며 이는 향후 개발에 중요한 블라스토메르 극성을 확립하고 세포-세포 상호작용을 공고히 한다.[16]
임상적 시사점
수정 기술
생쥐에 이식 실험을 한 결과 호르몬 유도, 과대배란, 인공수정이 성공적으로 이식 전 생쥐 배아를 만들어 내는 것으로 나타났다.쥐의 경우 90%의 암컷이 기계적 자극에 의해 유도되어 임신을 하고 적어도 한 개의 배아를 이식했다.[17]이러한 결과는 인간과 같은 다른 포유류 종에 이식될 수 있는 근거를 제공하기 때문에 고무적인 것으로 판명된다.
줄기세포
블라큘라 단계 세포는 많은 종에서 전지전능한 줄기세포 역할을 할 수 있다.전능줄기세포는 부상과 퇴화의 치유와 예방에 잠재적으로 도움을 줄 수 있는 장기 특이세포를 생산하기 위한 출발점이다.발파세포의 전사인자와 위치추정을 결합하면 유도기능장기와 조직의 발달로 이어질 수 있다.전능한 Xenopus 세포는 체내 전략에 사용되었을 때 기능적 망막으로 형성될 수 있었다.이들을 신경판의 눈장에 이식하고, 여러 가지 잘못된 전사 인자의 표현을 유도함으로써, 세포는 망막 혈통에 전념하게 되었고, 제노푸스에서 시력 기반 행동을 지도할 수 있게 되었다.[18]
참고 항목
참조
- ^ a b "Blastulation". www.web-books.com.
- ^ "Blastula". Encyclopædia Britannica. 2013.
- ^ a b c Gilbert, Scott (2010). Developmental Biology 9th Ed + Devbio Labortatory Vade Mecum3. Sinauer Associates Inc. pp. 243–247, 161. ISBN 978-0-87893-558-1.[영구적 데드링크]
- ^ Lombardi, Julian (1998). "Embryogenesis". Comparative vertebrate reproduction. Springer. p. 226. ISBN 978-0-7923-8336-9.
- ^ 구닥스 & 뉴먼, 2005: 페이지 27
- ^ a b c d Cockburn, Katie; Rossant, Janet (1 April 2010). "Making the blastocyst: lessons from the mouse". Journal of Clinical Investigation. 120 (4): 995–1003. doi:10.1172/JCI41229. PMC 2846056. PMID 20364097.
- ^ a b c Heasman, J (November 1997). "Patterning the Xenopus blastula". Development. 124 (21): 4179–91. PMID 9334267.
- ^ Tadros, Wael; Lipshitz, Howard D. (1 March 2004). "Setting the stage for development: mRNA translation and stability during oocyte maturation and egg activation in Drosophila". Developmental Dynamics. 232 (3): 593–608. doi:10.1002/dvdy.20297. PMID 15704150.
- ^ Gourdon, John B.; Standley, Henrietta J. (December 2002). "Uncommitted Xenopus blastula cells can be directed to uniform muscle gene expression by gradient interpretation and a community effect". The International Journal of Developmental Biology (Cambridge, UK). 46 (8): 993–8. PMID 12533022.
- ^ Toth, Attila. "Treatment: Addressing the Causes of Infertility in Men and Women". Macleod Laboratory. Retrieved 22 March 2013.
- ^ Kalt, MR (August 1971). "The relationship between cleavage and blastocoel formation in Xenopus laevis. I. Light microscopic observations". Journal of Embryology and Experimental Morphology. 26 (1): 37–49. PMID 5565077.
- ^ Tadros, W; Lipshitz, HD (March 2005). "Setting the stage for development: mRNA translation and stability during oocyte maturation and egg activation in Drosophila". Developmental Dynamics. 232 (3): 593–608. doi:10.1002/dvdy.20297. PMID 15704150.
- ^ a b Etkin, LD (1988). "Regulation of the mid-blastula transition in amphibians". Developmental Biology. 5: 209–25. doi:10.1007/978-1-4615-6817-9_7. PMID 3077975.
- ^ Tadros, W; Westwood, JT; Lipshitz, HD (June 2007). "The mother-to-child transition". Developmental Cell. 12 (6): 847–9. doi:10.1016/j.devcel.2007.05.009. PMID 17543857.
- ^ Weigel, D; Izaurralde, E (24 March 2006). "A tiny helper lightens the maternal load". Cell. 124 (6): 1117–8. doi:10.1016/j.cell.2006.03.005. PMID 16564001.
- ^ a b c d Fleming, Tom P.; Papenbrock, Tom; Fesenko, Irina; Hausen, Peter; Sheth, Bhavwanti (1 August 2000). "Assembly of tight junctions during early vertebrate development". Seminars in Cell & Developmental Biology. 11 (4): 291–299. doi:10.1006/scdb.2000.0179. PMID 10966863.
- ^ Watson, J.G. (October 1977). "Collection and Transfer of Preimplantation Mouse Embryos". Biology of Reproduction. 17 (3): 453–8. doi:10.1095/biolreprod17.3.453. PMID 901897.
- ^ Viczian, Andrea S.; Solessio, Eduardo C.; Lyou, Yung; Zuber, Michael E. (August 2009). "Generation of Functional Eyes from Pluripotent Cells". PLoS Biology. 7 (8): e1000174. doi:10.1371/journal.pbio.1000174. PMC 2716519. PMID 19688031.
참고 문헌 목록
- Forgács, G. & Newman, Stuart A. (2005). "Cleavage and blastula formation". Biological physics of the developing embryo. Cambridge University Press. ISBN 978-0-521-78337-8.
- Cullen, K.E. (2009). "embryology and early animal development". Encyclopedia of life science, Volume 2. Infobase. ISBN 978-0-8160-7008-4.
- McGeady, Thomas A., ed. (2006). "Gastrulation". Veterinary embryology. Wiley-Blackwell. ISBN 978-1-4051-1147-8.