이라이드
Ylide이라이드 또는 이라이드(/ˈɪlɪd/)는 형식 양전하(일반적으로 질소, 인 또는 유황)로 이형 원자(일반적으로 카르바니온)에 직접 부착된 공식 음전하 원자(일반적으로 카바니온)를 포함하고 있으며, 이 원자에는 두 원자가 모두 전자의 8진법을 완전하게 가지고 있다. 그 결과는 두 개의 인접한 원자가 공밸런트와 이온 결합 둘 다에 의해 연결되는 구조로 볼 수 있다. 보통 X-Y로+− 표기된다. 이라이드는 따라서 1,2-디폴라 화합물이며 zwitterion의 하위 등급이다.[1] 그것들은 유기화학에서 시약이나 반응성 매개체로 나타난다.[2]
화합물의 클래스 이름"일리드"는 접미사"-ylide"와 혼동해서는 안 된다.
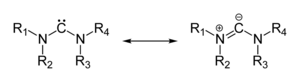
공명 구조
실제 구조는 두 형태 사이에 있는 반면, 많은 ylene 형태라고 알려진 공명 구조에서 복수의 결합 형태로 묘사될 수 있다.[citation needed]
이러한 유형의 이라이드의 실제 본딩 그림은 "오늄" 원자와 결합 길이를 감소시킨 인접 탄소 사이의 강한 쿨롬빅 흡인력을 가진 엄밀히 zwitterionic(오른쪽 구조)이다. 결과적으로, 탄소 음이온은 삼각 피라미드다.[citation needed]
인산염 이라이드
 메틸렌트리페닐인스포레인의 구조
메틸렌트리페닐인스포레인의 구조
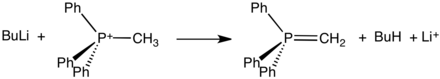
인산염 이라이드는 위티그 반응에 사용되는데, 이것은 케톤과 특히 알데히드를 알케인으로 전환하는 데 사용되는 방법이다. 이들 위티그 시약에서 양전하 는 페닐 대체물 3개와 카르바니온과의 결합을 가진 인 원자에 의해 운반된다. 이라이드는 '안정화' 또는 '안정화되지 않음'이 될 수 있다. 인산염 이라이드는 다소 간단하게 준비될 수 있다. 일반적으로 트리페닐인산염은 S2N 반응과 유사한 메커니즘에서 알킬 할라이드와 반응할 수 있다. 이 쿼터닌화는 알킬트리페닐인스포늄 소금을 형성하는데, 이 염소는 강한 염기(이 경우 부틸리튬)로 현장에서 격리시키거나 치료하여 ylide를 형성할 수 있다.
S2N 메커니즘 때문에, 덜 강직하게 방해되는 알킬 할라이드는 상당한 강직 방해(테르트-부틸 브로미드 등)를 가진 알킬 할라이드보다 트리페닐인산염에 더 호의적으로 반응한다. 이 때문에, 그러한 화합물을 포함하는 합성에는 일반적으로 다른 것보다 더 유리한 하나의 합성 경로가 있을 것이다.
인산염은 유기화학에서 특히 생물학적, 약리학적 활동과 함께 자연적으로 발생하는 제품의 합성에 중요한 시약이다. a-keto 안정화 인 ylides의 조정 특성에 대한 많은 관심은 분자 구조에 다른 기능 그룹이 존재하기 때문에 이들의 조정 다용도에서 비롯된다.
비대칭인산일라이드
The a-keto stabilized ylides derived from bisphosphines like dppe, dppm, etc., viz., [Ph2PCH2PPh2]C(H)C(O)R and [Ph2PCH2CH2PPh2]C(H)C(O)R (R = Me, Ph or OMe) constitute an important class of hybrid ligands containing both phosphine and ylide functionalities, and can exist in ylidic and enolate forms. 따라서 이러한 리간드는 팔라듐과 백금 같은 금속 이온과 다른 종류의 결합에 관여할 수 있다.[3]
기타유형
유황 기준
다른 일반적인 ylides로는 sulfonium ylides와 sulfoxium ylides가 있다. 예를 들어, 에폭시드를 준비하거나 스티븐스 재배열할 때 사용되는 Corey-Chaykovsky 시약이다.
산소를 기반으로 함
카보닐 이라이드(RR'C=OCRR+−')는 에폭시드를 링으로 열거나 보통 디아조 화합물에서 제조되는 전기생성 카보네와 카보닐의 반응에 의해 형성될 수 있다.[4] 옥소늄 이릴리드(RR'-O-CR+−'R)는 에테르와 전기영양성 카르베네의 반응에 의해 형성된다.
질소 기준
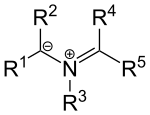
일반적인 구조를 가진 아조메틴 이라이드와 같은 특정한 질소 기반 이라이드도 존재한다.
이 화합물들은 카르바니온 옆에 놓인 이미늄 계정으로 상상할 수 있다. 대체품 R1, R은2 전자 인출 그룹이다. 이러한 이라이드는 α-아미노산과 알데히드의 응축이나 특정 N 대체 아지리딘의 열 링 개방 반응에 의해 생성될 수 있다.
다소 이국적인 디니트로겐 기반 이라이드 계열은 이소디아젠: RRN12+=N이다–. 일반적으로 이산화질소의 압출에 의해 분해된다.
안정된 카르베네에는 또한 ylidic 공명 기여자가 있다. 예:
기타
할로늄 이라이드는 아릴 할리데스와 금속 카바노이드로부터 준비될 수 있다. [2,3]-재분배 후 호몰릴할라이드를 얻는다.
테베 시약의 활성 형태는 종종 티타늄 이라이드로 간주된다. 위티그 시약처럼 카보닐 그룹의 산소 원자를 메틸렌 그룹으로 대체할 수 있다. 위티그 시약에 비해 기능성 그룹 내구성도 뛰어나다.
반응
중요한 일라이드 반응은 물론 위티그 반응(인용)이지만 더 있다.
쌍극 사이클로아데이션
일부 이라이드는 1,3-디폴로지로 되어 있으며 1,3-다극성 사이클로아데스로 상호작용한다. 예를 들어 아조메틴 이라이드는 풀레네와의 프라토 반응에서 쌍극이다.
사일랜드를 이용한 탈수커플링
그룹 3 호몰레틱 촉매 Y[N(SiMe3)]23가 존재하는 경우 트리페닐인스포늄 메틸라이드를 페닐실레인과 결합할 수 있다.[5] 이 반응은 제품별로 H2 가스를 생성하며, 실릴 안정화된 이라이드를 형성한다.
시그마티방성 재배열
많은 이라이드는 시그마티안 반응으로 반응한다.[6] Sommelet-Hauser 재배치는 [2,3]-시방성 반응의 예다. 스티븐스 재배치는 [1,2]-재배열이다.
특정 인산염 일라이드에서[7][8] [3,3]-시방성 반응이 관찰되었다.
아군 재배열
위티그 시약은 SN의2 대체에서 핵물질로 반응하는 것으로 확인된다.[9]
초기 추가 반응은 제거 반응이 뒤따른다.
참고 항목
- 1,3리졸
- 베테인: 오늄 양이온과 음전하를 가진 중성 분자
- Zwitterion: 하나 이상의 양전하와 음전하 쌍을 가진 중성 분자
참조
- ^ IUPAC, 화학용어 종합편찬, 제2편. ("금책")(1997년). 온라인 수정 버전: (2006–) "ylides". doi:10.1351/골드북.Y06728
- ^ McMurry, John (2008). Organic Chemistry, 7th Ed. Thomson Brooks/Cole. pp. 720–722. ISBN 978-0-495-11258-7.
- ^ Sabouncheia, Seyyed Javad; Ahmadi, Mohsen; Nasri, Zahra; Shams, Esmaeil; Salehzadeh, Sadegh; Gholiee, Yasin; Karamian, Roya; Asadbegy, Mostafa; Samiee, Sepideh (2013). "Synthesis, characterization, thermal, electrochemical, and DFT studies of mononuclear cyclopalladated complexes containing bidentate phosphine ligands and their biological evaluation as antioxidant and antibacterial agents". Comptes Rendus Chimie. 16 (2): 159–175. doi:10.1016/j.crci.2012.10.006.
- ^ Padwa, Albert (2005). "Catalytic Decomposition of Diazo Compounds as a Method for Generating Carbonyl‐Ylide Dipoles". Helvetica Chimica Acta. 88 (6): 1357–1374. doi:10.1002/hlca.200590109.
- ^ Nako, Adi E.; White, Andrew J. P.; Crimmin, Mark R. (2013). "A metal–amide dependent, catalytic C–H functionalisation of triphenylphosphonium methylide" (PDF). Chemical Science. 4 (2): 691–695. doi:10.1039/C2SC21123H. hdl:10044/1/15254.
- ^ Sweeney, J. B. (2009). "Sigmatropic rearrangements of 'onium' ylides". Chemical Society Reviews. 38 (4): 1027–1038. doi:10.1039/b604828p. PMID 19421580.
- ^ Ferguson, Marcelle L.; Senecal, Todd D.; Groendyke, Todd M.; Mapp, Anna K. (2006). "[3,3]-Rearrangements of Phosphonium Ylides". J. Am. Chem. Soc. 128 (14): 4576–4577. doi:10.1021/ja058746q. PMID 16594686.
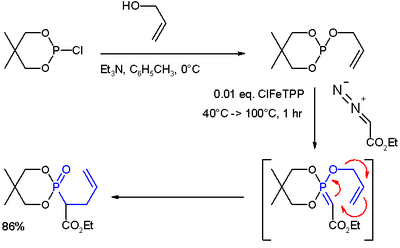
- ^ (i) 2-클로로-5,5-디메틸-1,3,2-디옥사포스포리닌을 사용한 아릴 알코올의 반응은 인산염 에스테르를 형성한다. (ii) 금속 카베네 첨가물(에틸 디아조아세테이트 및 ClFeTPP로부터)은 이라이드를 형성한다. (iii) 재배열 반응(파란색)은 인산염을 생성한다.
- ^ Patel, Ramesh M.; Argade, Narshinha P. (2007). "Facile SN2' Coupling Reactions of Wittig Reagents with Dimethyl Bromomethylfumarate: Synthesis of Enes, Dienes, and Related Natural Products". J. Org. Chem. 72 (13): 4900–4904. doi:10.1021/jo070728z. PMID 17539690.