바나다테
Vanadate화학에서 바나데이트는 바나듐의 음이온적 조정 콤플렉스다. 흔히 바나다이트는 바나듐의 산소를 말하며, 대부분은 +5의 가장 높은 산화 상태로 존재한다. [V(CN)]63-와 [VCL29]3- 콤플렉스를 헥사시아노바나드와 비아클로디바나이트라고 한다.
단순 바나다이트 이온은 사면체, 정형외과, VO3−
4 음이온으로, 예를 들어 정형외과산나트륨과 강한25 염기(pH > 13[1])의 VO 용액에 존재한다. 일반적으로 이 이온은 단일 이중 결합으로 표현되지만, 이온이 4개의 등가 산소 원자를 가진 일반 사면체이기 때문에 공진 형태다.
또한 이산 이온과 "무한" 중합체 이온을 포함하는 다양한 폴리오소보바나이트 이온이 존재한다.[2] 또한 Rhodium3+ vanadate, RhVO와 V5+ 이온이 발정 격자 내 Ti4+ 위치를 임의로 점유하는 통계적 발정 구조를 가지고 있는 Rhodium vanadate, RhVO와4 같은 바나데이트도 있는데,[3] 이 구조물은 양이온의 격자와 균형을 유지하는 바나데이트 음이온을 포함하지는 않지만 혼합 산화물이다.
바나다이트가 이름의 일부를 형성하는 화학적 명칭에서, 그것은 화합물이 중심 바나듐 원자를 가진 음이온을 포함하고 있음을 나타낸다. 예를 들어, 암모늄 헥사플루오로바나다이트(III)의 IUPAC 이름을 가진 화합물 (NH4)3VF의6 공통 명칭이다.
옥소바나다이트 이온의 예
이산 이온의 몇 가지 예는 다음과 같다.
- VO3−
4 "정맥류"[2] 사면체 - VO
24−
7 "pyrovanadate", 코너 공유 VO4 테트라헤드라, 이크롬산 이온과[2] 유사 - VO
33−
9, 모서리 공유 VO4 사분면(tetrahedra[4])을 사용한 순환 - VO
44−
12, 모서리 공유 VO4 사분면(tetrahedra[5])을 사용한 순환 - VO
53−
14, 코너 공유 VO4 테트라헤드라[6] - VO
66−
18, 벨.[7] - VO
106−
28 "decavanadate", 가장자리 및 모서리가 공유된 VO6 옥타헤드라[2] - V
12O4−
32 - VO
133−
34, 퓨전 VO6 옥타헤드라 - V
18O12−
42[9]
일부 고분자 "무한" 이온의 예는 다음과 같다.
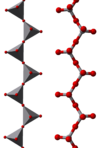 |  | 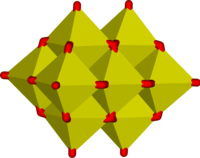 |
이온에서 바나듐은 사면체, 사각 피라미드 및 팔면체 조율을 나타낸다. 이 점에서 바나듐은 텅스테이트와 몰리브데이트와 유사성을 보이는 반면 크롬은 이온의 범위가 더 제한적이다.
수용액
강력한 기초 수용액에서 오산화 바나듐을 분해하면 무색 VO이온이3−
4 된다. 산성화 시 이 용액의 색상은 pH 7경에서 주황색에서 적색으로 점차 어두워진다. 갈색 수화 VO는25 pH 2경에서 침전되어 [VO2(HO2)]4+ 이온이 함유된 연한 황색 용액을 형성한다. pH 13과 2 사이에 존재하는 옥시온의 수와 정체는 농도뿐만 아니라 pH에 의존한다. 예를 들어 바나다이트의 양성자는 일련의 응축을 시작하여 폴리옥소보바나다이트 이온을 생성한다.[2]
- pH 9-12; HVO2−
4, VO
24−
7 - pH 4–9; H
2VO−
4, V
4O4−
12, HV
10O5−
28 - pH 2–4; H3VO4, H
2V
10O4−
28
약리학적 특성
바나다이트는 Na+/K-ATPase와+ Ca-ATPase2+(PMCA)와 같은 특정 혈장막 ATPASes의 강력한 억제제다. 인산염의 전환 상태 아날로그 역할을 하는 바나데이트는 인산염 전달 중 핵포착 공격을 받게 되는데, 기본적으로 인산염 E2 상태에서 P형 ATPases를 "트랩"한다. [11][12] 단, SERCA(sarco/endopplasmic reticulum Ca-ATPase2+), Actomosin ATPase, 미토콘드리아 ATPase와 같은 다른 ATPases를 억제하지는 않는다.[13][14][15]
참조
- ^ Cotton, F. Albert; Wilkinson, Geoffrey; Murillo, Carlos A.; Bochmann, Manfred (1999), Advanced Inorganic Chemistry (6th ed.), New York: Wiley-Interscience, ISBN 0-471-19957-5
- ^ a b c d e f Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (2nd ed.). Butterworth-Heinemann. ISBN 978-0-08-037941-8.
- ^ 웰스 A.F. (1984) 구조 무기 화학 제5판 옥스퍼드 과학 간행물 ISBN 0-19-855370-6
- ^ Hamilton E. E.; Fanwick P.E.; Wilker J.J. (2002). "The Elusive Vanadate (V3O9)3−: Isolation, Crystal Structure, and Nonaqueous Solution Behavior". J. Am. Chem. Soc. 124 (1): 78–82. doi:10.1021/ja010820r. PMID 11772064.
- ^ G.-Y. Yang, D.-W. Gao, Y. Chen, J.-Q. Xu, Q.-X. Zeng, H.-R. Sun, Z.-W. Pei, Q. Su, Y. Xing, Y.-H. Ling and H.-Q. Jia (1998). "[Ni(C10H8N2)3]2[V4O12]·11H2O". Acta Crystallographica C. 54 (5): 616–618. doi:10.1107/S0108270197018751.CS1 maint: 여러 이름: 작성자 목록(링크)
- ^ V. W. Day; Walter G. Klemperer; O. M. Yaghi (1989). "A new structure type in polyoxoanion chemistry: synthesis and structure of the V
5O3−
14 anion". J. Am. Chem. Soc. 111 (12): 4518. doi:10.1021/ja00194a068. - ^ Guang-Chuan Ou.; Long Jiang; Xiao-Long Feng; Tong-Bu Lu (2009). "Vanadium polyoxoanion-bridged macrocyclic metal complexes: from one-dimensional to three-dimensional structures". Dalton Transactions. 1 (1): 71–76. doi:10.1039/B810802A. PMID 19081973.
- ^ Hou D.; Hagen K.D.; Hill C.L. (1992). "Tridecavanadate, [V13O34]3−, a new high-potential isopolyvanadate". J. Am. Chem. Soc. 114 (14): 5864. doi:10.1021/ja00040a061.
- ^ Müller A.; Sessoli R.; Krickemeyer E.; Bögge H.; Meyer J.; Gatteschi D.; Pardi L.; Westphal J.; Hovemeier K.; Rohlfing R.; Döring J; Hellweg F.; Beugholt C.; Schmidtmann M. (1997). "Polyoxovanadates: High-Nuclearity Spin Clusters with Interesting Host–Guest Systems and Different Electron Populations. Synthesis, Spin Organization, Magnetochemistry, and Spectroscopic Studies". Inorg. Chem. 36 (23): 5239. doi:10.1021/ic9703641.
- ^ Jouanneau, S.; Verbaere, A.; Guyomard, D. (2003). "On a new calcium vanadate: synthesis, structure and Li insertion behaviour". Journal of Solid State Chemistry. 172 (1): 116–122. Bibcode:2003JSSCh.172..116J. doi:10.1016/S0022-4596(02)00164-0.
- ^ Kühlbrandt, Werner (April 2004). "Biology, structure and mechanism of P-type ATPases". Nature Reviews. Molecular Cell Biology. 5 (4): 282–295. doi:10.1038/nrm1354. ISSN 1471-0072. PMID 15071553.
- ^ Davies, Douglas R.; Hol, Wim G.J. (2004-11-19). "The power of vanadate in crystallographic investigations of phosphoryl transfer enzymes". FEBS Letters. 577 (3): 315–321. doi:10.1016/j.febslet.2004.10.022. ISSN 0014-5793. PMID 15556602.
- ^ Luo D.; Nakazawa M.; Yoshida Y.; Cai J.; Imai S. (2000). "Effects of three different Ca2+ pump ATPase inhibitors on evoked contractions in rabbit aorta and activities of Ca2+ pump ATPases in porcine aorta". General Pharmacology: The Vascular System. 34 (3): 211–220. doi:10.1016/S0306-3623(00)00064-1. PMID 11120383.
- ^ Bowman B.J.; Slayman C.W. (1979). "The Effects of Vanadate on the Plasma Membrane ATPase of Neurospora crassa". Journal of Biological Chemistry. 254 (8): 2928–2934. PMID 155060.
- ^ Aureliano, Manuel; Crans, Debbie C. (2009). "Decavanadate (V
10O6−
28) and oxovanadates: Oxometalates with many biological activities". Journal of Inorganic Biochemistry. 103 (4): 536–546. doi:10.1016/j.jinorgbio.2008.11.010. ISSN 0162-0134.