코발트
Cobalt in biology
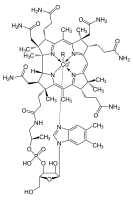
코발트는 모든 동물의 신진대사에 필수적이다.그것은 초경량 [1][2]원소로서 코발트의 1차 생물학적 저장고인 비타민12 B로도 알려진 코발라민의 핵심 성분이다.반추동물의 위에 있는 박테리아는 코발트 소금을 박테리아나 고세균에 의해서만 생산될 수 있는 화합물인 비타민12 B로 변환한다.따라서 토양에 코발트가 최소한으로 존재하면 방목동물의 건강이 현저하게 개선되고 비타민12 [3]B의 다른 공급원이 없기 때문에 하루에 0.20mg/kg의 섭취가 권장된다.
코발라민을 기반으로 하는 단백질은 코발트를 유지하기 위해 코린을 사용한다.코엔자임12 B는 [4]반응에 참여하는 반응성 C-Co 결합을 특징으로 합니다.사람에서 B는12 메틸과 아데노실이라는 두 가지 종류의 알킬 배위자를 가지고 있다.MeB는12 메틸(-CH3) 그룹 전달을 촉진합니다.B의12 아데노실 버전은 수소 원자가 두 개의 인접한 원자 간에 직접 전달되는 재배열을 촉매하며, 두 번째 치환기 X는 치환기가 있는 탄소 원자, 알코올의 산소 원자 또는 아민일 수 있습니다.메틸말로닐 코엔자임 A 뮤타아제([5]MUT)는 단백질과 지방으로부터 에너지를 추출하는 중요한 단계인 MML-CoA를 Su-CoA로 변환합니다.
다른 금속단백질(예: 아연 및 철)보다 훨씬 덜 흔하지만, B 외에12 다른 코발토프로틴이 알려져 있다.이러한 단백질은 B의12 코린 고리를 사용하지 않고 코발트와 직접 결합하는 인간과 다른 포유동물에서 발생하는 효소인 메티오닌 아미노펩티다아제 2를 포함한다.또 다른 비코발트 효소는 니트릴 하이드라타아제인데, 니트릴 하이드라타아제는 니트릴을 [6]대사하는 박테리아 중의 효소이다.
코발트 결핍증
인간의 경우 코발트 함유 비타민12 B의 섭취는 코발트의 모든 요구를 충족시킨다.반추에 상주하는 박테리아에 의한 합성을 통해 비타민B12 요구를 충족시키는 소와 양의 경우 무기 코발트 기능이 있다.20세기 초, 뉴질랜드의 북섬 화산 고원에서 농사를 짓는 동안, 소들은 소위 "부시병"으로 고통 받았다.화산 토양에는 소 먹이 [7][8]사슬에 필수적인 코발트 소금이 부족하다는 것이 밝혀졌다.1930년대 사우스오스트레일리아 남동부 90마일 사막에서 발생한 양의 '코발트병'은 코발트와 구리의 영양 결핍에서 비롯됐다.코발트 부족은 코발트 탄환(코발트 탄환)의 개발로 극복되었다.코발트 탄환(코발트 탄환)은 동물의 [clarification needed][9][8][10]반추에 머물기 위해 경구용 점토와 혼합된 고밀도 산화 코발트 탄환이다.
레퍼런스
- ^ Yamada, Kazuhiro (2013). "Chapter 9. Cobalt: Its Role in Health and Disease". In Astrid Sigel; Helmut Sigel; Roland K. O. Sigel (eds.). Interrelations between Essential Metal Ions and Human Diseases. Metal Ions in Life Sciences. Vol. 13. Springer. pp. 295–320. doi:10.1007/978-94-007-7500-8_9. PMID 24470095.
- ^ 크리스틴, 발렌타인, 밴더, 럼(2013)코발트 10 코발트 및 생화학부"밴쉬리아(, 루시아)메탈믹스와 셀입니다.생명과학에서 금속 이온.12번.봄머.p. 333-337-4.10.7/9-75561-5561-1_10.75561-1_10.BN 978-15560-4007-5560-4007-5560-4입니다.PMID 235677777777입니다.전자북은 BN 1559-15561-15561-5561-15561-SN 1559-15561-SN 1559-200836 전자 메일입니다.
- ^ Schwarz, F. J.; Kirchgessner, M.; Stangl, G. I. (2000). "Cobalt requirement of beef cattle – feed intake and growth at different levels of cobalt supply". Journal of Animal Physiology and Animal Nutrition. 83 (3): 121–131. doi:10.1046/j.1439-0396.2000.00258.x.
- ^ Voet, Judith G.; Voet, Donald (1995). Biochemistry. New York: J. Wiley & Sons. p. 675. ISBN 0-471-58651-X. OCLC 31819701.
- ^ Smith, David M.; Golding, Bernard T.; Radom, Leo (1999). "Understanding the Mechanism of B12-Dependent Methylmalonyl-CoA Mutase: Partial Proton Transfer in Action". Journal of the American Chemical Society. 121 (40): 9388–9399. doi:10.1021/ja991649a.
- ^ Kobayashi, Michihiko; Shimizu, Sakayu (1999). "Cobalt proteins". European Journal of Biochemistry. 261 (1): 1–9. doi:10.1046/j.1432-1327.1999.00186.x. PMID 10103026.
- ^ "Soils". Waikato University. Archived from the original on 2012-01-25. Retrieved 2012-01-16.
- ^ a b McDowell, Lee Russell (2008). Vitamins in Animal and Human Nutrition (2nd ed.). Hoboken: John Wiley & Sons. p. 525. ISBN 978-0-470-37668-3.
- ^ 호주과학아카데미> 고인이 된 펠로우> 헤들리 랄프 마스턴1900~1965 2013년 5월 12일 접속.
- ^ Snook, Laurence C. (1962). "Cobalt: its use to control wasting disease". Journal of the Department of Agriculture, Western Australia. 4. 3 (11): 844–852.