재결정(화학)
Recrystallization (chemistry)화학에서 재결정화는 화학물질을 정제하는 데 사용되는 기술이다.불순물과 화합물을 모두 적절한 용매에 용해시킴으로써 원하는 화합물 또는 불순물 중 하나를 용액에서 제거할 수 있고 다른 한쪽은 남겨둘 수 있다.그것은 화합물이 침전될 때 종종 형성되는 결정체들의 이름을 따서 붙여졌다.또는 재결정화는 작은 얼음 결정을 희생시키면서 큰 얼음 결정의 자연스러운 성장을 나타낼 수 있다.
화학
화학에서 재결정화는[1]: 127–132 화합물을 정제하는 과정이다.가장 일반적인 상황은 원하는 "복합물 A"가 소량의 "불순물 B"에 의해 오염되는 것입니다.다양한 정제 방법이 있으며(분리 프로세스 참조), 재결정화도 그 중 하나입니다.또한 다음과 같은 다양한 재결정 기술을 사용할 수 있습니다.
단일 솔루션 재결정
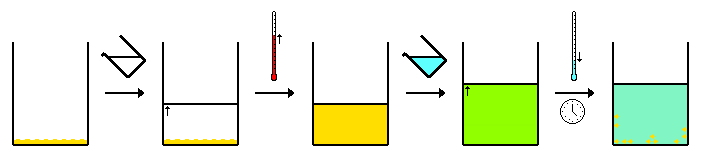
일반적으로 '복합 A'와 '불순물 B'의 혼합물을 극소량의 뜨거운 용매에 녹여 완전히 녹여 포화용액을 만든다.그런 다음 용액을 냉각시킵니다.용액이 식으면 용액의 화합물 용해도가 떨어집니다.그 결과 원하는 화합물이 솔루션에서 폐기(재결정)됩니다.냉각 속도가 느릴수록 결정이 더 커집니다.

이상적으로는 불순물 B의 용해도 생성물 B를 어느 온도에서도 넘지 않는다.이 경우 고체결정은 순수한 A로 구성되며 모든 불순물은 용액에 남아 있게 됩니다.고체결정은 여과로 수집되고 여과수는 폐기됩니다.불순물의 용해도 생성물이 초과되면 불순물 일부가 공침전된다.그러나 불순물의 농도가 상대적으로 낮기 때문에 침전 결정 중의 불순물 농도는 원래 고체 중의 불순물 농도보다 낮아진다.재결정화를 반복하면 더 순수한 결정성 침전이 발생합니다.재결정 후에는 불순물이 녹는점을 낮추기 때문에 녹는점을 측정하여 순도를 확인한다.NMR 분광법은 불순물 수준을 확인하는 데도 사용할 수 있다.재결정화를 반복하면 화합물 A의 용해도가 0이 아니기 때문에 재료의 손실이 발생합니다.
결정화 프로세스에는 "시드" 결정의 추가와 같은 시작 단계가 필요합니다.실험실에서 유리 재결정 용기의 측면을 긁어낸 아주 작은 유리 조각이 결정체가 자랄 수 있는 핵을 제공할 수 있습니다.재결정화의 성공 여부는 적절한 용제를 찾는 데 달려 있습니다.이는 보통 예측/경험과 시행/오차의 조합입니다.화합물은 낮은 온도보다 높은 온도에서 더 잘 용해되어야 합니다.불용성 불순물은 열여과법에 의해 제거된다.
멀티솔벤트 재결정
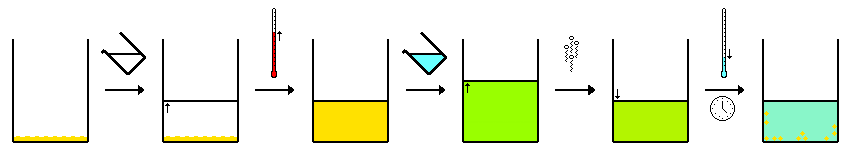
이 방법은 위와 동일하지만 두 개 이상의 용제가 사용되는 경우입니다.이것은 "복합 A"와 "불순물 B"가 모두 첫 번째 용매에 용해되는 것에 의존한다.제2의 용제를 천천히 첨가한다."복합 A" 또는 "불순물 B" 중 하나는 이 용매에 용해되지 않고 침전되며, "복합 A"/"불순물 B" 중 다른 하나는 용액에 남습니다.따라서 첫 번째 용제와 두 번째 용제의 비율이 매우 중요합니다.일반적으로 두 번째 용매는 화합물 중 하나가 용액에서 결정화되기 시작할 때까지 천천히 첨가되며 그 후 용액이 냉각됩니다.가열은 이 기술에 필요하지 않지만 사용할 수 있습니다.
이 방법의 반대는 용제의 혼합물이 A와 B를 모두 녹일 때 사용할 수 있습니다.그런 다음 증류 또는 적용된 진공에 의해 용제 중 하나를 제거합니다.이로 인해 "복합 A" 또는 "불순물 B" 중 하나가 침전되는 용제의 비율이 변화한다.
열여과 재결정
열여과를[1]: 74 사용하여 "불순물 B" 및 일부 "불용성 물질 C"에서 "복합물 A"를 분리할 수 있다.이 기술은 일반적으로 위에서 설명한 싱글솔벤트 시스템을 사용합니다.'복합 A'와 '불순물 B'를 모두 최소량의 뜨거운 용매에 녹이면 용액을 여과하여 '불용성 물질 C'를 제거한다.이 물질은 제3의 불순물 화합물부터 깨진 유리 조각에 이르기까지 무엇이든 될 수 있다.성공적인 공정을 위해서는 여과 중에 용액에서 결정되어 여과지 또는 깔때기에 결정체가 형성되는 것을 방지하기 위해 여과 장치가 뜨겁도록 해야 한다.
이를 위한 한 가지 방법은 소량의 깨끗한 용제가 들어 있는 원뿔형 플라스크를 뜨거운 플레이트에 가열하는 것입니다.필터 깔때기를 입 위에 올려놓고 뜨거운 용매 증기가 줄기를 따뜻하게 유지한다.재킷이 있는 필터 깔때기를 사용할 수도 있다.여과지는 4분의 1로 접는 것보다 홈이 있는 것이 좋습니다.이렇게 하면 여과 속도가 빨라져 원하는 화합물이 냉각되어 용액에서 결정화될 기회가 줄어듭니다.
대부분의 경우 여과 및 재결정 작업은 두 가지 독립된 단계로 수행하는 것이 더 간단합니다.상온에서 적절한 용매에 "복합 A"와 "불순물 B"를 녹인 후 (불용성 화합물/유리를 제거하기 위해) 여과하여 용매를 제거한 후 위의 방법 중 하나를 사용하여 재결정한다.
씨뿌리기
결정화에는 시작 단계가 필요합니다.이것은 자발적일 수도 있고, 포화 용액에 소량의 순수한 화합물(종자 [1]결정)을 첨가함으로써 이루어질 수도 있고, 결정 성장을 위한 씨앗 표면을 만들기 위해 유리 표면을 긁어내는 것만으로 이루어질 수도 있습니다.먼지 입자도 단순한 씨앗 역할을 할 수 있다고 생각된다.
단일 완벽한 결정(X선 분석용)
X선 결정학을 위한 결정체를 키우는 것은 매우 어려울 수 있습니다.X선 분석을 위해서는 단일 완벽한 결정이 필요합니다.일반적으로 소량의 순수 화합물(5~100mg)이 사용되며, 결정은 매우 느리게 성장합니다.다음과 같은 여러 기술을 사용하여 완벽한 크리스털을 기를 수 있습니다.
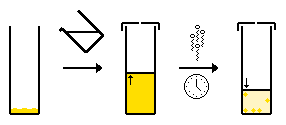
- 단일 용제의 느린 증발 - 일반적으로 화합물은 적절한 용매에 용해되고 용매는 천천히 증발됩니다.일단 용액이 포화 상태가 되면 결정이 형성될 수 있다.
- 멀티솔벤트 시스템의 느린 증발 - 위와 동일하지만 휘발성이 더 높은 용제의 증발로 인해 용매 조성이 변화합니다.이 화합물은 휘발성 용매에 더 잘 용해되므로 화합물은 용액에 점점 더 용해되지 않고 결정화된다.
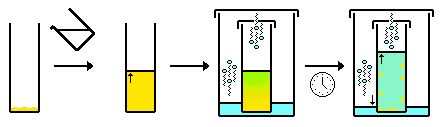
- 느린 확산 - 위와 유사합니다.단, 제2의 용제는 1개의 용기에서 복합용액을 유지하는 용기(가스 확산)로 증발할 수 있다.기체가 용액으로 확산된 용매의 증가로 용매 조성이 변화함에 따라 화합물이 용액에 점점 불용성화되어 결정화된다.
- 인터페이스/저속 혼합(종종 NMR 튜브에서 수행됨).위와 비슷하지만 하나의 용제가 다른 용제로 확산되는 대신 두 용제가 액체 확산에 의해 혼합(확산)됩니다.일반적으로 두 번째 용제는 화합물이 포함된 용액 위에 조심스럽게 "적층"됩니다.시간이 지남에 따라 두 솔루션이 혼합됩니다.확산에 의해 용제조성이 변화함에 따라 화합물은 용액에서 점점 불용성화되어 보통 계면에서 결정화된다.또, 용제의 혼입이 늦어지기 때문에, 하층으로서 고밀도 용제를, 상층으로서 고온 용제를 사용하는 것이 좋다.
- H의 수직선 중 하나는 화합물의 용액을 포함하는 튜브이고, 다른 수직선은 화합물이 용해되지 않는 용매를 포함하는 튜브이며, H의 수평선은 두 수직선을 연결하는 튜브이다.튜브: 또한 두 용제의 혼합을 제한하는 미세한 유리 소결체가 있습니다.
- 단일 완벽한 결정을 얻은 후에는 결정이 '건조'되지 않도록 결정화 액체와 함께 밀폐된 용기에 보관하는 것이 좋습니다.단일 완전 결정체는 결정 격자에 결정화 용매를 포함할 수 있다.결정에서 이 내부 용제를 잃으면 결정 격자가 분해되어 결정이 가루로 변할 수 있습니다.
얼음
얼음의 경우, 재결정화는 작은 결정들을 희생시키면서 더 큰 결정들이 성장하는 것을 의미한다.일부 생물학적 부동 단백질은 이 과정을 억제하는 것으로 나타났으며, 그 효과는 내결빙성 [2]유기체와 관련이 있을 수 있다.
「 」를 참조해 주세요.
레퍼런스
- ^ a b c Harwood, Laurence M.; Moody, Christopher J. (1 January 1990). Experimental Organic Chemistry: Principles and Practice (Illustrated ed.). Blackwell Scientific Publications. ISBN 978-0-632-02016-4. LCCN 88007680. OCLC 18816225. OL 2032038M. Wikidata Q107313989. Retrieved 2021-06-22 – via Internet Archive.
- ^ Kumar Verma, Ashok (2014). "Recrystallization of Ice". Encyclopedia of Snow, Ice and Glaciers. Encyclopedia of Earth Sciences Series. p. 932. doi:10.1007/978-90-481-2642-2_439. ISBN 978-90-481-2641-5.
참고 도서
- Laurence M. Harwood; Christopher J. Moody; Jonathan M. Percy (1999). Experimental organic chemistry: standard and microscaling. ISBN 9780632048199.
- John Leonard; B. Lygo; Garry Procter (2 June 1994). Advanced practical organic chemistry. ISBN 9780748740710.