수소화디이소부틸알루미늄
Diisobutylaluminium hydride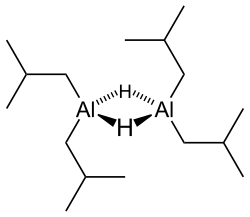 | |
 | |
| 이름 | |
|---|---|
| IUPAC 이름 디이소부틸알루미늄수소화물 | |
| 기타 이름 DIBAH; DIBAL; DiBAlH; DIBAL-H; DIBALH | |
| 식별자 | |
3D 모델(JSmol) | |
| 켐스파이더 | |
| ECHA 정보 카드 | 100.013.391 |
| EC 번호 |
|
PubChem CID | |
| 유니 | |
CompTox 대시보드 (EPA ) | |
| |
| |
| 특성. | |
| CHAL819(단량체) CHAL16382(조광) | |
| 몰 질량 | 142.22 g/g (단량체) 284.44 g/120 (조광) |
| 외모 | 무색 액체 |
| 밀도 | 0.798 g/cm3 |
| 녹는점 | - 80 °C (-112 °F, 193 K) |
| 비등점 | 1 mmHg에서 116 ~ 118 °C (241 ~244 °F, 389 ~391 K) |
| 물과 반응하다 | |
| 용해성 | 탄화수소, THF 및 에테르에 용해됨 |
| 위험 요소 | |
| 산업안전보건(OHS/OSH): | |
주요 위험 요소 | 공중에서 점화하다 |
| GHS 라벨링: | |
  | |
| 위험. | |
| H220, , , , , | |
| P210, , , , , , , , , , , , , , , , , , , , , , , , , , ,, | |
달리 명시되지 않은 한 표준 상태(25°C[77°F], 100kPa)의 재료에 대한 데이터가 제공됩니다. | |
디이소부틸알루미늄수소화물(DIBALH, DIBAL, DIBAL-H 또는 DIBAH)은 식2(i-BuAlH)2의 환원제로, i-Bu는 이소부틸(-CH2(CH3))2을 나타낸다.이 유기 알루미늄 화합물은 유기 [1]합성 시약이다.
특성.
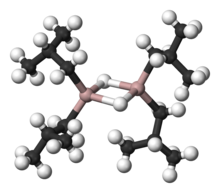
대부분의 유기 알루미늄 화합물처럼, 화합물의 구조는 아마도 그것의 경험 공식에 의해 제시된 것보다 더 많을 것이다.X선 결정학을 포함하지 않는 다양한 기법은 이 화합물이 이합체 및 삼합체로 존재하며, 가교 수소화물 [2]배위자를 공유하는 사면체 알루미늄 중심부로 구성되어 있음을 시사합니다.하이드라이드는 크기가 작고 알루미늄 파생 모델의 경우 매우 염기성이 높기 때문에 알킬기를 선호합니다.
DIBAL은 트리이소부틸 알루미늄(이합체 자체)을 가열하여 β-수소화물 [3]제거를 유도하여 제조할 수 있습니다.
DIBAL은 무색 액체로 시판할 수 있지만 톨루엔이나 헥산 등의 유기용매에 용액으로 구입하여 분사하는 것이 일반적이다.
유기 합성에 사용
DIBAL은 카르본산, 그 유도체 및 질화물을 알데히드로 변환하는 것을 포함한 다양한 환원 작용을 위한 유기 합성에 유용하다.DIBAL은 α-β 불포화 에스테르를 대응하는 알릴 [1]알코올로 효율적으로 환원한다.반면, LiAlH는4 에스테르와 아실 염화물을 1차 알코올로, 질화물을 1차 아민으로 환원합니다(Fieser 작업 절차 사용).DIBAL은 전자가 부족한 화합물에서는 천천히 반응하고, 전자가 풍부한 화합물에서는 더 빠르게 반응합니다.따라서4 친전자 환원제인 반면 LiAlH는 친핵 환원제로 생각할 수 있다.
DIBAL은 질소를 알데하이드로 확실하게 환원시키지만, 에스테르를 알데하이드로 환원하는 것은 표면적으로는 유용해 보이지만 실제로는 알코올과 알데하이드 혼합물로 이어지는 악랄할 정도로 민감한 반응이다.그럼에도 불구하고 연속 흐름 [4]화학을 이용하여 반응 조건을 세심하게 제어함으로써 이러한 고장을 방지할 수 있다.
DIBALH는 원래 알케인의 [5]중합 촉매로 조사되었다.
안전.
DIBAL은 대부분의 알킬 알루미늄 화합물과 마찬가지로 공기와 물과 격렬하게 반응하여 폭발을 일으킬 수 있습니다.
레퍼런스
- ^ a b Galatsis, P. (2001). "Diisobutylaluminum Hydride". Encyclopedia of Reagents for Organic Synthesis. New York: John Wiley & Sons. doi:10.1002/047084289X.rd245. ISBN 0471936235.
- ^ Self, M. F.; Pennington, W. T.; Robinson, G. H. (1990). "Reaction of Diisobutylaluminum Hydride with a Macrocyclic Tetradentate Secondary Amine. Synthesis and Molecular Structure of [Al(iso-Bu)]2[C10H20N4][Al(iso-Bu)3]2: Evidence of an Unusual Disproportionation of (iso-Bu)2AlH". Inorganica Chimica Acta. 175 (2): 151–153. doi:10.1016/S0020-1693(00)84819-7.
- ^ Eisch, J. J. (1981). Organometallic Syntheses. Vol. 2. New York: Academic Press. ISBN 0-12-234950-4.
- ^ Webb, Damien; Jamison, Timothy F. (2012-01-20). "Diisobutylaluminum Hydride Reductions Revitalized: A Fast, Robust, and Selective Continuous Flow System for Aldehyde Synthesis". Organic Letters. 14 (2): 568–571. doi:10.1021/ol2031872. hdl:1721.1/76286. ISSN 1523-7060. PMID 22206502.
- ^ Ziegler, K.; Martin, H.; Krupp, F. (1960). "Metallorganische Verbindungen, XXVII Aluminiumtrialkyle und Dialkyl-Aluminiumhydride aus Aluminiumisobutyl-Verbindungen". Justus Liebigs Annalen der Chemie. 629 (1): 14–19. doi:10.1002/jlac.19606290103.
외부 링크
- Stockman, R. (2001). "Dibal reduction of an amino acid derived methyl ester; Garner's Aldehyde". ChemSpider Synthetic Pages. doi:10.1039/SP161. SyntheticPage 161.[영구 데드링크]
- "Oxidation And Reduction Reactions in Organic Chemistry". University of Southern Maine, Department of Chemistry. Archived from the original on 2011-06-11.
- "Diisobutyl Aluminum hydride (DIBAL-H) and Other Isobutyl Aluminum Alkyls (DIBAL-BOT, TIBAL) as Specialty Organic Synthesis Reagents" (PDF). Akzo-Nobel. Archived from the original (PDF) on 2011-04-08. Retrieved 2011-02-23.


