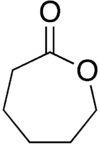
카프로락톤
Caprolactone| | |||
| 이름 | |||
|---|---|---|---|
| 선호 IUPAC 이름 옥세판-2-1 | |||
| 기타 이름 카프로락톤 ε-카프로락톤 헥사노-6락톤 6-헥사놀락톤 헥산-6-올라이드 1-옥사-2-옥소시클로헵탄 | |||
| 식별자 | |||
3D 모델(JSmol) | |||
| 체비 | |||
| 켐벨 | |||
| 켐스파이더 | |||
| ECHA InfoCard | 100.007.217 | ||
| 케그 | |||
펍켐 CID | |||
| 유니 | |||
CompTox 대시보드 (EPA) | |||
| |||
| |||
| 특성. | |||
| C6H10O2 | |||
| 어금질량 | 114.14 g/190 | ||
| 밀도 | 1.030 g/cm3 | ||
| 녹는점 | -1°C(30°F; 272K) | ||
| 비등점 | 241°C(466°F, 514K)[2] | ||
| 불능 | |||
달리 명시된 경우를 제외하고, 표준 상태(25°C [77°F], 100 kPa)의 재료에 대한 데이터가 제공된다. | |||
ε-카프로락톤 또는 단순 카프로락톤은 7엠베드 링을 가진 락톤(순환 에스테르)이다.그것의 이름은 카프로산에서 유래되었다.이 무색의 액체는 대부분의 유기 용매와 물과 섞일 수 있다.한때 카프로락탐의 전조로 대규모로 생산되기도 했다.[3]
생산 및 사용
카프로락톤은 페라세트산을 사용한 사이클로헥사논의 배이어빌라이거 산화에 의해 산업적으로 제조된다.
카프로락톤은 고도로 전문화된 중합체의 생산에 사용되는 단량체다.예를 들어, 링 개방 중합은 폴리카프로락톤을 제공한다.[3]또 다른 중합체는 폴리글카프론인데 수술 시 봉합재로 사용된다.[4]
반응
비록 더 이상 경제적이지 않지만, 카프로락톤은 한때 카프로락탐의 전구체로 생산되었다.카프로락톤은 높은 온도에서 암모니아로 처리되어 락탐을 만든다.
- (CH2)5CO2 + NH3 → (CH2)5C(O)NH + H2O
카프로락톤의 카보닐화는 가수분해 후에 피멜산을 준다.락톤 링은 알코올과 물을 포함한 핵성분으로 쉽게 열려서 폴리락톤을 주고 결국 6-히드록시디프산을 준다.
관련 화합물
몇 개의 다른 카프로락톤이 알려져 있다.이러한 이소머에는 α-, β-, β- 및 Δ-카프롤락톤이 포함된다.모두 치랄이다. (R)-기름-카프로락톤은 꽃향기와 일부 과일과 야채의 향의 성분이며,[5] 또한 카프라 딱정벌레가 페로몬으로 생산하기도 한다.[6]Δ-caprolactone은 가열된 유지방에서 발견된다.[7]
AP/AN/Al로켓 추진체 HTCE: 히드록시 종단 카프로락톤에테르를 바인더로 사용한다.
안전
카프롤락톤은 빠르게 수산화되며, 그 결과 히드록시카르복실산은 다른 히드록시카르복실산에서도 흔히 볼 수 있듯이 예외 없이 독성을 보인다.[9]심한 눈 자극을 유발하는 것으로 알려져 있다.노출되면 각막 부상이 발생할 수 있다.[1]
참조
- ^ a b "ε-caprolactone SIDS Initial Assessment Report" (PDF). OECD. Archived from the original (PDF) on 2011-08-15. Retrieved 2017-10-12.
- ^ "Capa Monomer product data sheet" (PDF). Perstorp. 2015-02-27. Archived from the original (PDF) on 2017-02-02. Retrieved 2017-10-11.
- ^ a b Köpnick, Horst; Schmidt, Manfred; Brügging, Wilhelm; Rüter, Jörn; Kaminsky, Walter (2002). "Polyesters". Ullmann's Encyclopedia of Industrial Chemistry (6th ed.). Weinheim: Wiley-VCH. doi:10.1002/14356007.a21_227.
- ^ "glycolide E-caprolactone copolymer Summary Report". CureHunter. Retrieved 2017-10-11.
- ^ Mosandl, A.; Günther, C. (1989). "Stereoisomeric flavor compounds: structure and properties of gamma-lactone enantiomers". Journal of Agricultural and Food Chemistry. 37: 413–418. doi:10.1021/jf00086a031.
- ^ Nunez, M. Teresa; Martin, Victor S. (1990). "Efficient oxidation of phenyl groups to carboxylic acids with ruthenium tetraoxide. A simple synthesis of (R)-gamma-caprolactone, the pheromone of Trogoderma granarium". Journal of Organic Chemistry. 55 (6): 1928–1932. doi:10.1021/jo00293a044.
- ^ Parliament, Thomas H.; Nawar, Wassef W.; Fagerson, Irving S. (1965). "Delta-Caprolactone in Heated Milk Fat". Journal of Dairy Science. 48 (5): 615–616. doi:10.3168/jds.S0022-0302(65)88298-4.
- ^ HTCE
- ^ Miltenberger, Karlheinz (2002). "Hydroxycarboxylic Acids, Aliphatic". Ullmann's Encyclopedia of Industrial Chemistry (6th ed.). Weinheim: Wiley-VCH. doi:10.1002/14356007.a13_507.