과산화 스트론튬
Strontium peroxide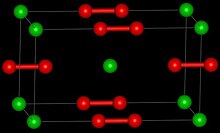 | |
| 식별자 | |
|---|---|
3D 모델(JSmol) | |
| ECHA InfoCard | 100.013.841 |
| EC 번호 |
|
펍켐 CID | |
| 유니 | |
CompTox 대시보드 (EPA) | |
| |
| |
| 특성. | |
| SRO2 | |
| 어금질량 | 119.619 g/1911 |
| 외관 | 백색 가루 |
| 냄새 | 무취의 |
| 밀도 | 4.56 g/cm3 (무수) 1.91 g/cm3 (옥타하이드레이트) |
| 녹는점 | 215°C(419°F, 488K) (손상)[1] |
| 약간 녹는 | |
| 용해성 | 알코올에 매우 용해성, 염화암모늄 아세톤에 녹지 않는. |
| 구조 | |
| 4각형 | |
| D174h, I4/mm, tI6 | |
| 6 | |
| 위험 | |
| GHS 라벨 표시: | |
   [3] [3] | |
| 위험 | |
| H302, H312, H317, H331, H350 | |
| P220, P261, P280, P305+P351+P338 | |
| 안전 데이터 시트(SDS) | 외부 SDS |
달리 명시된 경우를 제외하고, 표준 상태(25°C [77°F], 100 kPa)의 재료에 대한 데이터가 제공된다. | |
| Infobox 참조 자료 | |
과산화 스트론튬은 무수 및 옥타하이드레이트 형태로 존재하는 SrO라는2 공식을 가진 무기 화합물로, 둘 다 백색 고형분이다. 무수 형태는 탄화칼슘과 유사한 구조를 채택한다.[4][5]
사용하다
표백에 쓰이는 산화제다. 그것은 산화제와 선명한 적색 폭약 색소로 일부 폭약 성분에 사용된다. 그것은 또한 방부제와 추적기 탄약으로도 사용될 수 있다.
생산
과산화 스트론튬은 가열된 스트론튬 산화물 위에 산소를 통과시켜 생성된다. O가2 없는 상태에서 가열하면 SrO와 O로2 분해된다. 그것은 BaO보다2 열적으로 더 쉽다.[6][7]
참조
- ^ Middleburgh, Simon C.; Lagerlof, Karl Peter D.; Grimes, Robin W. (2013). "Accommodation of Excess Oxygen in Group II Monoxides". Journal of the American Ceramic Society. 96: 308–311. doi:10.1111/j.1551-2916.2012.05452.x.
- ^ Massalimov, I. A.; Kireeva, M. S.; Sangalov, Yu. A. (2002). "Structure and Properties of Mechanically Activated Barium Peroxide". Inorganic Materials. 38 (4): 363–366. doi:10.1023/A:1015105922260.
- ^ "Strontium Peroxide". American Elements. Retrieved March 7, 2019.
- ^ Bernal, J. D.; D'yatlova, E.; Kasarnovskii, I.; Raikhstein, S. I.; Ward, A. G. "The structure of strontium and barium peroxides" Zeitschrift für Kristallographie, Kristallgeometrie, Kristallphysik, Kristallchemie (1935), 92, 344-54.
- ^ 나타, G. "수산화물과 수산화물의 구조. IV. 옥타하이드레이트 과산화 스트론튬" 가제타 치미카 이탈리아어(1932), 62, 444-56.
- ^ Middleburgh, Simon C.; Lagerlof, Karl Peter D.; Grimes, Robin W. (2013). "Accommodation of Excess Oxygen in Group II Monoxides". Journal of the American Ceramic Society. 96: 308–311. doi:10.1111/j.1551-2916.2012.05452.x.
- ^ Bauschlicher, Charles W. Jr.; Partridge, Harry; Sodupe, Mariona; Langhoff, Stephen R. "Theoretical study of the alkaline-earth metal superoxides BeO2 through SrO2" Journal of Physical Chemistry 1992, volume 96, pp. 9259-64. doi:10.1021/j100202a036
참고 항목


