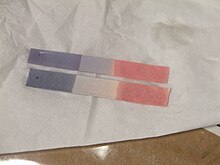
리트머스
Litmus본 기사는 해당 기사에서 독일어로 번역된 텍스트로 확장할 수 있다(2021년 2월) 중요한 번역지시는 [쇼]를 클릭한다.
|
| 무료 사전인 위키트리노리에서 리트무스를 찾아봐. |

리트머스(Litmus)는 이끼에서 추출한 여러 염료를 수용성 혼합한 것이다. 그것은 종종 필터 용지에 흡수되어 가장 오래된 형태의 pH 표시기 중 하나를 생산하는데, 이것은 물질의 산성도를 시험하는데 사용된다.
역사
리트머스(litmus)라는 단어는 옛 노르웨이의 "dye" 또는 "color"[1]라는 단어에서 유래되었다. 리트무스는 약 1300년 스페인의 의사 아르날두스 드 빌라 노바에 의해 처음으로 사용되었다.[2] 16세기 이후로는 몇몇 이끼들로부터, 특히 네덜란드에서 푸른 염료를 추출했다.
자연원
리트무스는 다른 종의 이끼에게서 발견될 수 있다. The dyes are extracted from such species as Roccella tinctoria (South American), Roccella fuciformis (Angola and Madagascar), Roccella pygmaea (Algeria), Roccella phycopsis, Lecanora tartarea (Norway, Sweden), Variolaria dealbata, Ochrolechia parella, Parmotrema tinctorum, and Parmelia. 현재 주요 공급원은 로첼라 몬테냐이(모잠비크)와 덴드로그라파 루캅회아(캘리포니아)[2]이다.
사용하다
리트무스의 주된 용도는 25°C(77°F)에서 pH 범위 4.5–8.3에 걸쳐 색 변화가 일어나는 가운데, 푸른 리트머스 종이가 산성 조건에서 붉은색으로 변하며, 기본 또는 알칼리성 조건에서 붉은 리트무스 종이가 파란색으로 변하기 때문에 용액이 산성인지 또는 기초적인지 여부를 시험하는 것이다. 중성 리트머스 종이는 보라색이다.[2] 습식 리트머스 종이는 산도나 기초성에 영향을 미치는 수용성 가스에 대한 시험에도 사용될 수 있다; 가스는 물에 녹고 그 결과 용액은 리트머스 종이에 색을 입힌다. 예를 들어, 알칼리성인 암모니아 가스는 빨간 리트머스 종이를 파란색으로 바꾼다. 모든 리트머스 종이가 pH 종이로 작용하지만, 그 반대는 사실이 아니다.
리트머스 또한 유사한 기능을 하는 수용액으로 준비될 수 있다. 산성 조건에서는 용액이 적색이고, 알칼리성 조건에서는 용액이 청색이다.
| 리트머스 (pH 표시기) | ||
| pH 4.5 이하 | pH 8.3 이상 | |
| 4.5 | ⇌ | 8.3 |
산-기초 이외의 화학 반응도 리트머스 종이에 색 변화를 일으킬 수 있다. 예를 들어, 염소 가스는 파란 리트머스 종이를 하얗게 만든다; 리트머스 염료는 차아염소산염 이온이 존재하기 때문에 표백된다[3]. 이 반응은 되돌릴 수 없기 때문에 리트무스는 이 상황에서 지표 역할을 하지 못하고 있다.
화학
리트머스 혼합물은 CAS 번호 1393-92-6으로 10~15가지 염료를 함유하고 있다. 리트무스의 모든 화학적 성분은 오르세인이라고 알려진 관련 혼합물의 성분과 같을 가능성이 높지만 비율은 다르다. 오르세인과 대조적으로 리트머스 주성분은 평균 분자량이 3300이다.[4] 리트무스의 산성 기반 지표는 7-히드록시페녹사존 색소포레에 기인한다.[5] 일부 리트머스 분수는 에리트로이트민, 아졸리트민, 스패니올리트민, 루코오르체인, 루카졸리트민 등 특정 명칭을 부여했다. 아졸릿민은 리트무스와 거의 같은 효과를 보인다.[6]
메커니즘
적색 리트머스에는 약한 이중산(diprotic acid)이 들어 있다. 그것이 기본 화합물에 노출되면 수소 이온은 첨가된 염기와 반응한다. 리트머스산으로부터 형성된 결합기층은 파란색을 띠기 때문에 젖은 붉은 리트머스 종이는 알칼리성 용액에서 파란색을 띠게 된다.
참조
- ^ "Litmus". 7 October 2021.
- ^ a b c Neupert, Manfred (January 31, 2013). "Lackmus". Römpp Lexikon Chemie (in German).
- ^ O'Leary, Donal (2000). "Chlorine". The Chemical Elements. Archived from the original on 2008-12-21.
- ^ Beecken, H.; E-M. Gottschalk; U. v Gizycki; H. Krämer; D. Maassen; H-G. Matthies; H. Musso; C. Rathjen; Ul. Zdhorszky (2003). "Orcein and Litmus". Biotechnic & Histochemistry. 78 (6): 289–302. doi:10.1080/10520290410001671362. PMID 15473576. S2CID 41944320.
- ^ H. Musso, C. Rathjen (1959). "Orcein dyes. X. Light absorption and chromophore of litmus". Chem. Ber. 92 (3): 751–3. doi:10.1002/cber.19590920331.
- ^ E.T. Wolf: Volsténdige Uversicht der Elementar-analytischen Untersuchen 조직관리자 S.450-453, Vereffentlicht 1846, Verlag E. 안톤 (독일)