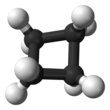
사이클로부탄
Cyclobutane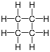 | |||
| | |||
| 이름 | |||
|---|---|---|---|
| 우선 IUPAC 이름 사이클로부탄 | |||
| 식별자 | |||
3D 모델(JSmol) | |||
| 1900183 | |||
| 체비 | |||
| 켐스파이더 | |||
| ECHA 정보 카드 | 100.005.468 | ||
| EC 번호 |
| ||
| 81684 | |||
PubChem CID | |||
| 유니 | |||
| UN 번호 | 2601 | ||
CompTox 대시보드 (EPA ) | |||
| |||
| |||
| 특성. | |||
| C4H8 | |||
| 몰 질량 | 56.150 g/140 | ||
| 외모 | 무색 가스 | ||
| 밀도 | 0.140g/cm3 | ||
| 녹는점 | -91 °C (-132 °F, 182 K) | ||
| 비등점 | 12.5 °C (54.5 °F, 285.6 K) | ||
| 위험 요소 | |||
| GHS 라벨링: | |||
  | |||
| 위험. | |||
| H220, H280 | |||
| P210, , , , , | |||
| NFPA 704(파이어 다이아몬드) | |||
| 관련 화합물 | |||
관련 알칸 | 부탄 | ||
관련 화합물 | 시클로부텐, 시클로부타디엔, 시클로프로판, 시클로펜탄 | ||
달리 명시되지 않은 한 표준 상태(25°C[77°F], 100kPa)의 재료에 대한 데이터가 제공됩니다. | |||
시클로부탄은 식(4CH)의2 시클로알칸 및 유기화합물이다.시클로부탄은 무색 가스이며 상업적으로 액화 가스로 이용 가능하다.시클로부탄의 유도체는 시클로부탄이라고 불린다.사이클로부탄 자체는 상업적, 생물학적으로 중요하지 않지만, 보다 복잡한 파생상품은 생물학과 [1]생명공학에서 중요하다.
구조.
탄소 원자 사이의 결합 각도는 상당한 응력을 가지므로 관련된 선형 또는 비변형 탄화수소(예: 부탄 또는 사이클로헥산)보다 결합 에너지가 낮다.따라서 사이클로부탄은 약 500°C 이상에서 불안정하다.
사이클로부탄에 있는 4개의 탄소 원자는 코플라어가 아닙니다.대신 링은 일반적으로 접히거나 "주름"된 형태를 [2]취합니다.이는 C-C-C 각도가 90° 미만임을 의미합니다.탄소 원자 중 하나는 다른 세 개의 탄소에 의해 형성된 평면과 25° 각도를 이룬다.이러한 방식으로 일부 일식 상호작용이 감소합니다.이 배치는 "나비"라고도 합니다.등가 주름진 구성 상호 변환:
시클로부탄(생물학 및 생명공학)
시클로부탄 모티브는 본래의 변형에도 불구하고 자연에서 발견된다.한 가지 특이한 예는 펜타시클로아남독산입니다.[3] 펜타시클로아남독산은 5개의 융합된 시클로부탄 단위로 구성된 라단입니다.이 화합물의 추정 변종은 시클로부탄의 3배입니다.이 화합물은 아질산 이온과 [4]암모니아로부터 질소와 물을 생산하는 데 관여하는 독성 히드록실아민과 히드라진으로부터 유기체를 보호하는 단단하고 매우 조밀한 막의 일부를 형성하는 박테리아에서 발견됩니다.몇몇 관련된 회향 또한 [citation needed]자연에서 발견된다.
시클로부탄포토디머(CPD)는 피리미딘의 [5][6][7]C=C 이중결합을 결합시키는 광화학반응에 의해 형성된다.두 개의 티민 사이에 형성된 티민 이합체(T-T 이합체)는 CPD 중 가장 풍부하며, CPD는 뉴클레오티드 절제 복구 효소에 의해 쉽게 복구된다.대부분의 유기체에서 그것들은 빛에 의존하는 효소 계열인 광분해효소에 의해서도 회복될 수 있다.색소건조증은 이 손상을 치료할 수 없는 유전적 질병으로 자외선에 노출되어 피부 변색과 종양이 발생한다.
카르보플라틴은 시클로부탄-1,1-디카르본산으로부터 유래한 항암제로 인기가 있다.
준비
시클로부탄의 제조에는 많은 방법이 존재한다.알케인은 자외선을 조사하면 이량화된다. 1,4-디할로부탄은 환원 금속에 의해 탈할로겐화되면 사이클로부탄으로 변환된다.
시클로부탄은 1907년 제임스 브루스와 리처드 윌스테터에 의해 [8]니켈이 존재하는 상태에서 시클로부텐을 수소화함으로써 처음 합성되었다.
「 」를 참조해 주세요.
레퍼런스
- ^ Zvi Rappoport, Joel F. Liebman, ed. (2005). The Chemistry of Cyclobutanes. PATAI'S Chemistry of Functional Groups. John Wiley & Sons. doi:10.1002/0470864028. ISBN 9780470864029.
- ^ "Cyclobutane". Encyclopedia Britannica. Retrieved 8 July 2022.
- ^ J. S. Sinninghe Damsté, M. Strous, W. I. C. Rijpstra, E. C. Hopmans, J. A. J. Geenevasen, A. C. T. van Duin, L. A. van Niftrik and M. S. M. Jetten (2002). "Linearly concatenated cyclobutane lipids form a dense bacterial membrane". Nature. 419 (6908): 708–712. Bibcode:2002Natur.419..708S. doi:10.1038/nature01128. PMID 12384695. S2CID 4373854.
{{cite journal}}: CS1 maint: 여러 이름: 작성자 목록(링크) - ^ Vincent Mascitti and E. J. Corey (2006). "Enantioselective Synthesis of Pentacycloanammoxic Acid". J. Am. Chem. Soc. 128 (10): 3118–9. doi:10.1021/ja058370g. PMID 16522072.저자들은 생합성 방식이 매우 신비롭다고 말한다.
- ^ R. B. Setlow (1966). "Cyclobutane-Type Pyrimidine Dimers in Polynucleotides". Science. 153 (3734): 379–386. Bibcode:1966Sci...153..379S. doi:10.1126/science.153.3734.379. PMID 5328566. S2CID 11210761.
- ^ Expert reviews in molecular medicine (2 December 2002). "Structure of the major UV-induced photoproducts in DNA" (PDF). Cambridge University Press. Archived from the original (PDF) on 21 March 2005. Retrieved 16 August 2009.
- ^ Christopher Mathews; K.E. Van Holde (1990). Biochemistry (2nd ed.). Benjamin Cummings Publication. p. 1168. ISBN 978-0-8053-5015-9.
- ^ Richard Willstätter; James Bruce (1907). "Zur Kenntnis der Cyclobutanreihe" [On our knowledge of the cyclobutane series]. Berichte der Deutschen Chemischen Gesellschaft. 40 (4): 3979–3999. doi:10.1002/cber.19070400407.
외부 링크
- 데이터 시트 링크