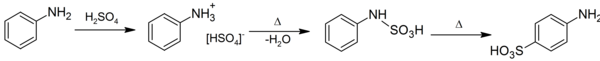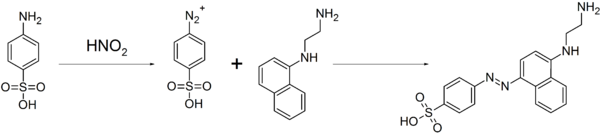술파닐산
Sulfanilic acid | |
 | |
 | |
| 이름 | |
|---|---|
| 선호 IUPAC 이름 4-아미노벤젠-1-술폰산[1] | |
| 기타 이름 | |
| 식별자 | |
3D 모델(JSmol) | |
| 체비 | |
| ECHA InfoCard | 100.004.075 |
펍켐 CID | |
| 유니 | |
CompTox 대시보드 (EPA) | |
| |
| |
| 특성. | |
| C6H7NO3S | |
| 어금질량 | 173.19 |
| 밀도 | 1.485 |
| 녹는점 | 288°C(550°F, 561K) |
| 12.51 g/L | |
| 산도(pKa) | 3.23 (H2O)[2] |
| 관련 화합물 | |
관련설폰산 | 벤제네설폰산 p-톨루엔설폰산 |
달리 명시된 경우를 제외하고, 표준 상태(25°C [77°F], 100 kPa)의 재료에 대한 데이터가 제공된다. | |
| Infobox 참조 자료 | |
Sulfanilic acid (4-aminobenzenesulfonic acid)는 HNCHSO라는3643 공식을 가진 유기 화합물이다.그것은 비백색 고체다.높은 녹는점을 설명하는 zwitterion이다.유기화학에서 흔히 볼 수 있는 구성 요소다.[3]
합성
Sulfanilic acid는 Aniline의 sulfonation에 의해 생성될 수 있다.[4]
적용들
화합물이 디아조 화합물을 쉽게 형성하기 때문에 염료와 설파제를 만드는 데 쓰인다.[3]이 성질은 N-(1-나프틸)에틸렌디아민과의 디아조늄 결합반응에 의한 질산염 및 질산염 이온의 정량분석에도 사용되어 아조 염료가 발생하였으며, 색소측정법에 의한 적색 용액의 색강도에서 질산염 또는 질산염 이온의 농도를 추론하였다.[5]
환경적 측면
넓은 용도를 반영하여, 설파닐산은 매립지의 침출수에서 발견된다.[6]그것은 약간의 아조 염료를 줄임으로써 생산된다.[7]
파생상품
참고 항목
참조
- ^ a b Nomenclature of Organic Chemistry : IUPAC Recommendations and Preferred Names 2013 (Blue Book). Cambridge: The Royal Society of Chemistry. 2014. p. 789. doi:10.1039/9781849733069-FP001. ISBN 978-0-85404-182-4.
The name ‘sulfanilic acid’ is not retained.
- ^ Haynes, William M., ed. (2016). CRC Handbook of Chemistry and Physics (97th ed.). CRC Press. p. 5–88. ISBN 978-1498754286.
- ^ a b "설파닐산"화학사전.옥스퍼드 대학 출판부, 2000년옥스퍼드 레퍼런스 온라인.옥스퍼드 대학 출판부
- ^ 지그프리드 하우프트만: Organization Chemie, 제2판, VEB Deutscher Verlag Für Grundstoff산업계, 라이프치히, 1985년, 페이지 511, ISBN 3-342-00280-8.
- ^ G. H. Jerffery; J. Bassett; J. Mendham; R. C. Denney (1989). "Colorimetry and Spectrophotometry". Vogel's Textbook of Quantitative Chemical Analysis, 5th Edition. Longman. p. 702. ISBN 0-582-44693-7.
- ^ Holm, John V.; Ruegge, Kirsten.; Bjerg, Poul L.; Christensen, Thomas H. (1995). "Occurrence and Distribution of Pharmaceutical Organic Compounds in the Groundwater Downgradient of a Landfill (Grindsted, Denmark)". Environmental Science & Technology. 29 (5): 1415–1420. doi:10.1021/es00005a039. PMID 22192041.
- ^ Nam, S. (2000). "Reduction of azo dyes with zero-valent iron". Water Research. 34 (6): 1837–1845. doi:10.1016/S0043-1354(99)00331-0.
- ^ Klaus Hunger; Peter Mischke; Wolfgang Rieper; Roderich Raue; Klaus Kunde; Aloys Engel (2005). "Azo Dyes". Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002/14356007.a03_245..