랩게프4
RAPGEF4| 랩게프4 | |||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||||||||||
| 식별자 | |||||||||||||||||||||||||
| 에일리어스 | RAPGEF4, CAMP-GEFII, CGEF2, EPAC, EPAC2, Nbla00496, RAP구아닌뉴클레오티드교환인자4 | ||||||||||||||||||||||||
| 외부 ID | OMIM: 606058 MGI: 1917723 HomoloGene: 4451 GenCards: RAPGEF4 | ||||||||||||||||||||||||
| |||||||||||||||||||||||||
| |||||||||||||||||||||||||
| |||||||||||||||||||||||||
| |||||||||||||||||||||||||
| 맞춤법 | |||||||||||||||||||||||||
| 종. | 인간 | 마우스 | |||||||||||||||||||||||
| 엔트레즈 | |||||||||||||||||||||||||
| 앙상블 | |||||||||||||||||||||||||
| 유니프로트 | |||||||||||||||||||||||||
| RefSeq(mRNA) | |||||||||||||||||||||||||
| RefSeq(단백질) | |||||||||||||||||||||||||
| 장소(UCSC) | Chr 2: 172.74 ~173.05 Mb | Chr 2: 71.81 ~72.09 Mb | |||||||||||||||||||||||
| PubMed 검색 | [3] | [4] | |||||||||||||||||||||||
| 위키데이터 | |||||||||||||||||||||||||
| |||||||||||||||||||||||||
랩구아닌뉴클레오티드교환인자(GEF)4(RAPGEF4)는 cAMP2(EPAC2)에 의해 직접 활성화되는 교환단백질이라고도 하며, 사람에게서 RAPGEF4 유전자에 [5][6][7]의해 암호화되는 단백질이다.
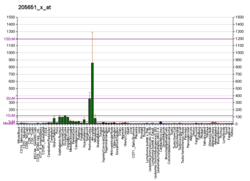
Epac2는 다양한 세포에서 주요 세컨드 메신저인 cAMP의 타깃입니다.Epac2는 RAPGEF4 유전자에 의해 코드화되어 주로 뇌,[8] 신경내분비 및 내분비 조직에서 발현된다.Epac2는 cAMP 자극 [8][9]시 Ras-like 작은 GTPase Rap에 대한 구아닌 뉴클레오티드 교환 인자로 기능한다.Epac2는 내분비 및 신경내분비세포 및 [10][11]뉴런의 다양한 cAMP 매개 세포 기능에 관여한다.
유전자 및 기록
인간 Epac2는 염색체 2q31-q32에 위치한 RAPGEF4에 의해 코드화되어 대체 프로모터 사용 및 차등 스플라이싱에 [8][12][13]의해 3개의 아이소폼(Epac2A, Epac2B, Epac2C)이 생성된다.Epac2A(원래 Epac2라고 불림)는 아미노산 1,011개를 가진 다도메인 단백질로 주로 췌장섬과 신경내분비세포와 [8]같은 뇌와 신경내분비조직에서 발현된다.Epac2A는 아미노말단조절영역과 카르복시말단촉매영역의 2가지 영역으로 구성된다.조절 영역에는 2개의 고리형 뉴클레오티드 결합 도메인(cNBD-A 및 cNBD-B)과 DEP(Disevelled, Egl-10 및 Pleckstrin) 도메인이 포함된다.Rap의 활성화를 담당하는 촉매 영역은 CDC25 호몰로지 도메인(CDC25-HD), Ras Exchange Motif(REM) 도메인 및 Ras Association(RA) [14]도메인으로 구성됩니다.Epac2B는 제1의 cNBD-A 도메인을 포함하지 않으며, Epac2C는 cNBD-A 및 DEP 도메인을 포함하지 않는다.Epac2B 및 Epac2C는 각각 부신[12] 및 [13]간에서 특이적으로 발현된다.
작용 메커니즘
결정 구조는 Epac2의 촉매 영역이 분자 내에서 cNBD-B와 상호 작용하며, cAMP가 없는 경우 조절 영역에 의해 입체적으로 마스킹되므로 촉매 영역과 Rap1 [15]간의 상호 작용을 억제합니다.Rap1B와의 콤플렉스 내에서의 cAMP 아날로그 결합형 Epac2의 결정구조는 cAMP가 cNBD-B 도메인에 결합함으로써 규제영역이 회전할 수 있는 동적인 Configuration 변화가 발생함을 나타냅니다.이러한 구성 변경은 Rap1이 촉매 영역에 액세스할 수 있도록 하고 [15][16]활성화를 가능하게 합니다.
특정 작용제
여러 Epac 선택형 cAMP 아날로그는 Epacs의 기능적 역할과 PKA의존적 시그널링 경로와는 [17]다른 Epac의존적 시그널링 경로를 명확히 하기 위해 개발되었다.퓨린 구조의 8-위치와 리보스의 2'-위치의 수정은 Epacs의 특이성에 중요한 것으로 간주된다.지금까지 Epacs에 대한 특이성이 매우 높기 때문에 8-CPT-2'-O-Me-cAMP(8-pCPT)와 그 막 투과형 8-pCPT-AM을 사용하였다.췌장β세포에서 인슐린 분비 자극을 통해 제2형 당뇨병 치료에 널리 사용되는 술포닐루레아제(SUs)도 Epac2를 [18]특이적으로 활성화하는 것으로 나타났다.
기능.
췌장β세포에서 주로 Gs결합 수용체를 통한 호르몬 및 신경 입력을 포함한 다양한 세포외 자극에 의해 활성화될 수 있는 cAMP 시그널링은 포도당 항상성을 유지하기 위한 인슐린 분비의 정상적인 조절에 중요하다.cAMP 시그널링의 활성화는 PKA의존성 [10]경로뿐만 아니라 Epac2의존성 경로로 인슐린 분비를 증폭시킨다.Epac2-Rap1 시그널링은 쉽게 방출될 [19]수 있는 풀에서 인슐린을 포함한 소포의 세포 외화를 촉진하는 데 중요하다.인슐린 과립의 Epac2 매개 세포외증에서 Epac2는 혈장막과 인슐린 과립 양쪽에 국재화된 비계단백질인 [20][21]Rim2와 상호작용하여 [22][23]세포외증의 도킹 및 프라이밍 상태를 결정한다.또한 가능한2+ Ca 센서 [24]단백질인 피콜로는 Epac2-Rim2 복합체와 상호작용하여 cAMP 유도 인슐린 [22]분비를 조절한다.Rap의 이펙터 단백질 중 하나인 포스포리파아제 C-γ(PLC-γ)는 ATP 감수성 칼륨 채널, 리아노딘 수용체, IP3 [11][25]수용체와 같은 이온 채널의 활성을 변화시켜 세포2+ 내 Ca 역학을 조절하는 것이 제안된다.뉴런에서 Epac은 Held의 척추뼈에서 글루탐산성 시냅스 및 가재 신경근 [26][27][28]접합부에서 신경전달물질 방출에 관여합니다.에팩은 또한 포유동물 [29][30]조직의 축삭 재생뿐만 아니라 신경세포 성장과 신경 분화 조절에 의한 뇌 발달에도 역할을 한다.게다가, Epac2는 시냅스 가소성을 조절하여 기억력과 학습과 같은 [31][32]높은 뇌 기능을 제어할 수 있다.심장에서 Epac1은 주로 발현되며, β-아드레날린 [33]수용체를 통한 만성 cAMP 자극에 의한 비후성 사건의 발달에 관여한다.반면 Epac2의 만성 자극은 [34][35]생쥐에서 CaMKII 의존성 확장성 석소체(SR) Ca2+ 방출을 통해 심장 부정맥의 원인이 될 수 있다.Epac2는 심장에서 [36]GLP-1 자극 심방나트륨(ANP) 분비에도 관여한다.
임상적 영향
Epac2는 다양한 세포에서 많은 생리적 기능에 관여하기 때문에 Epac2/Rap1 시그널링 메커니즘의 결함은 다양한 병리학적 상태의 발달에 기여할 수 있다.Epac2하는 쥐의 연구에 따르면Epac-mediated 신호 인슐린 분비의 상승 작용을glucagon-like peptide-1(GLP-1)과glucose-dependentinsulinotropic polypeptide,[37][38]이 Epac2 각광 받는 대상을 제안하는 등 incretins(장 호르몬enteroendocrine 세포로부터 식사 섭취에 이어발표)에서 요구하고 있다고 지적한다. tr에당뇨병의 섭취사실, 인크리틴 기반 당뇨병 치료법은 현재 전 세계적으로 임상 진료에 사용되고 있다; Epac2 선택 작용제의 개발은 새로운 항당뇨병 약물의 발견으로 이어질 수 있다.GLP-1의 유사체는 Epac2를 [36]통해 심방나트륨(ANP) 분비를 자극함으로써 혈압강하 효과를 발휘하는 것으로 나타났다.심장에서는 β아드레날린 수용체의 만성 자극이 Epac2 의존 메커니즘을 [34][35]통해 부정맥으로 진행되는 것으로 알려져 있다.뇌에서는 알츠하이머병 환자에서 Epac1의 상향조절과 Epac2 mRNA의 하향조절이 관찰되어 [39]Epacs의 역할을 시사한다.Epac2 희귀 코딩 변종은 자폐증 환자에게서 발견되며 수지상 형태학적 [40][41]이상을 일으킬 수 있다.따라서 Epac2는 다양한 질병의 병인과 병태생리학에 관여하며 유망한 치료 대상을 나타낸다.
메모들
이 기사의 2015년 버전은 외부 전문가에 의해 이중 출판 모델로 업데이트되었다.대응하는 학술 동료 리뷰 기사는 Gene에 게재되었으며 다음과 같이 인용할 수 있다. Kenji Sugawara; Tadao Shibasaki; Harumi Takahashi; Susumu Seino (18 September 2015). "Structure and functional roles of Epac2 (Rapgef4)". Gene. Gene Wiki Review Series. 575 (2 Pt 3): 577–583. doi:10.1016/J.GENE.2015.09.029. ISSN 0378-1119. PMC 6636354. PMID 26390815. Wikidata Q38590433. |
레퍼런스
- ^ a b c GRCh38: 앙상블 릴리즈 89: ENSG000091428 - 앙상블, 2017년 5월
- ^ a b c GRCm38: 앙상블 릴리즈 89: ENSMUSG000049044 - 앙상블, 2017년 5월
- ^ "Human PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ "Mouse PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ "Entrez Gene: RAPGEF4 Rap guanine nucleotide exchange factor (GEF) 4".
- ^ Kawasaki H, Springett GM, Mochizuki N, Toki S, Nakaya M, Matsuda M, Housman DE, Graybiel AM (December 1998). "A family of cAMP-binding proteins that directly activate Rap1". Science. 282 (5397): 2275–9. doi:10.1126/science.282.5397.2275. PMID 9856955.
- ^ de Rooij J, Rehmann H, van Triest M, Cool RH, Wittinghofer A, Bos JL (July 2000). "Mechanism of regulation of the Epac family of cAMP-dependent RapGEFs". J. Biol. Chem. 275 (27): 20829–36. doi:10.1074/jbc.M001113200. PMID 10777494.
- ^ a b c d Kawasaki H, Springett GM, Mochizuki N, Toki S, Nakaya M, Matsuda M, Housman DE, Graybiel AM (Dec 1998). "A family of cAMP-binding proteins that directly activate Rap1". Science. 282 (5397): 2275–9. doi:10.1126/science.282.5397.2275. PMID 9856955.
- ^ de Rooij J, Zwartkruis FJ, Verheijen MH, Cool RH, Nijman SM, Wittinghofer A, Bos JL (Dec 1998). "Epac is a Rap1 guanine-nucleotide-exchange factor directly activated by cyclic AMP". Nature. 396 (6710): 474–7. doi:10.1038/24884. PMID 9853756. S2CID 204996248.
- ^ a b Seino S, Shibasaki T (Oct 2005). "PKA-dependent and PKA-independent pathways for cAMP-regulated exocytosis". Physiological Reviews. 85 (4): 1303–42. doi:10.1152/physrev.00001.2005. PMID 16183914. S2CID 14539206.
- ^ a b Schmidt M, Dekker FJ, Maarsingh H (Apr 2013). "Exchange protein directly activated by cAMP (epac): a multidomain cAMP mediator in the regulation of diverse biological functions". Pharmacological Reviews. 65 (2): 670–709. doi:10.1124/pr.110.003707. PMID 23447132. S2CID 5918666.
- ^ a b Niimura M, Miki T, Shibasaki T, Fujimoto W, Iwanaga T, Seino S (Jun 2009). "Critical role of the N-terminal cyclic AMP-binding domain of Epac2 in its subcellular localization and function". Journal of Cellular Physiology. 219 (3): 652–8. doi:10.1002/jcp.21709. PMID 19170062. S2CID 46070429.
- ^ a b Ueno H, Shibasaki T, Iwanaga T, Takahashi K, Yokoyama Y, Liu LM, Yokoi N, Ozaki N, Matsukura S, Yano H, Seino S (Nov 2001). "Characterization of the gene EPAC2: structure, chromosomal localization, tissue expression, and identification of the liver-specific isoform". Genomics. 78 (1–2): 91–8. doi:10.1006/geno.2001.6641. PMID 11707077.
- ^ Bos JL (Dec 2006). "Epac proteins: multi-purpose cAMP targets". Trends in Biochemical Sciences. 31 (12): 680–6. doi:10.1016/j.tibs.2006.10.002. PMID 17084085.
- ^ a b Rehmann H, Das J, Knipscheer P, Wittinghofer A, Bos JL (Feb 2006). "Structure of the cyclic-AMP-responsive exchange factor Epac2 in its auto-inhibited state". Nature. 439 (7076): 625–8. doi:10.1038/nature04468. PMID 16452984. S2CID 4423485.
- ^ Rehmann H, Arias-Palomo E, Hadders MA, Schwede F, Llorca O, Bos JL (Sep 2008). "Structure of Epac2 in complex with a cyclic AMP analogue and RAP1B". Nature. 455 (7209): 124–7. doi:10.1038/nature07187. PMID 18660803. S2CID 4393652.
- ^ Chen H, Wild C, Zhou X, Ye N, Cheng X, Zhou J (May 2014). "Recent advances in the discovery of small molecules targeting exchange proteins directly activated by cAMP (EPAC)". Journal of Medicinal Chemistry. 57 (9): 3651–65. doi:10.1021/jm401425e. PMC 4016168. PMID 24256330.
- ^ Zhang CL, Katoh M, Shibasaki T, Minami K, Sunaga Y, Takahashi H, Yokoi N, Iwasaki M, Miki T, Seino S (Jul 2009). "The cAMP sensor Epac2 is a direct target of antidiabetic sulfonylurea drugs". Science. 325 (5940): 607–10. doi:10.1126/science.1172256. PMID 19644119. S2CID 8923842.
- ^ Shibasaki T, Takahashi H, Miki T, Sunaga Y, Matsumura K, Yamanaka M, Zhang C, Tamamoto A, Satoh T, Miyazaki J, Seino S (Dec 2007). "Essential role of Epac2/Rap1 signaling in regulation of insulin granule dynamics by cAMP". Proceedings of the National Academy of Sciences of the United States of America. 104 (49): 19333–8. doi:10.1073/pnas.0707054104. PMC 2148290. PMID 18040047.
- ^ Kashima Y, Miki T, Shibasaki T, Ozaki N, Miyazaki M, Yano H, Seino S (Dec 2001). "Critical role of cAMP-GEFII--Rim2 complex in incretin-potentiated insulin secretion". The Journal of Biological Chemistry. 276 (49): 46046–53. doi:10.1074/jbc.M108378200. PMID 11598134.
- ^ Ozaki N, Shibasaki T, Kashima Y, Miki T, Takahashi K, Ueno H, Sunaga Y, Yano H, Matsuura Y, Iwanaga T, Takai Y, Seino S (Nov 2000). "cAMP-GEFII is a direct target of cAMP in regulated exocytosis". Nature Cell Biology. 2 (11): 805–11. doi:10.1038/35041046. PMID 11056535. S2CID 17744192.
- ^ a b Shibasaki T, Sunaga Y, Fujimoto K, Kashima Y, Seino S (Feb 2004). "Interaction of ATP sensor, cAMP sensor, Ca2+ sensor, and voltage-dependent Ca2+ channel in insulin granule exocytosis". The Journal of Biological Chemistry. 279 (9): 7956–61. doi:10.1074/jbc.M309068200. PMID 14660679.
- ^ Yasuda T, Shibasaki T, Minami K, Takahashi H, Mizoguchi A, Uriu Y, Numata T, Mori Y, Miyazaki J, Miki T, Seino S (Aug 2010). "Rim2alpha determines docking and priming states in insulin granule exocytosis". Cell Metabolism. 12 (2): 117–29. doi:10.1016/j.cmet.2010.05.017. PMID 20674857.
- ^ Fujimoto K, Shibasaki T, Yokoi N, Kashima Y, Matsumoto M, Sasaki T, Tajima N, Iwanaga T, Seino S (Dec 2002). "Piccolo, a Ca2+ sensor in pancreatic beta-cells. Involvement of cAMP-GEFII.Rim2. Piccolo complex in cAMP-dependent exocytosis". The Journal of Biological Chemistry. 277 (52): 50497–502. doi:10.1074/jbc.M210146200. PMID 12401793.
- ^ Gloerich M, Bos JL (2010). "Epac: defining a new mechanism for cAMP action". Annual Review of Pharmacology and Toxicology. 50: 355–75. doi:10.1146/annurev.pharmtox.010909.105714. PMID 20055708. S2CID 37351100.
- ^ Gekel I, Neher E (Aug 2008). "Application of an Epac activator enhances neurotransmitter release at excitatory central synapses". The Journal of Neuroscience. 28 (32): 7991–8002. doi:10.1523/JNEUROSCI.0268-08.2008. PMC 6670779. PMID 18685024.
- ^ Sakaba T, Neher E (Jan 2001). "Preferential potentiation of fast-releasing synaptic vesicles by cAMP at the calyx of Held". Proceedings of the National Academy of Sciences of the United States of America. 98 (1): 331–6. doi:10.1073/pnas.021541098. PMC 14590. PMID 11134533.
- ^ Zhong N, Zucker RS (Jan 2005). "cAMP acts on exchange protein activated by cAMP/cAMP-regulated guanine nucleotide exchange protein to regulate transmitter release at the crayfish neuromuscular junction". The Journal of Neuroscience. 25 (1): 208–14. doi:10.1523/JNEUROSCI.3703-04.2005. PMC 6725206. PMID 15634783.
- ^ Christensen AE, Selheim F, de Rooij J, Dremier S, Schwede F, Dao KK, Martinez A, Maenhaut C, Bos JL, Genieser HG, Døskeland SO (Sep 2003). "cAMP analog mapping of Epac1 and cAMP kinase. Discriminating analogs demonstrate that Epac and cAMP kinase act synergistically to promote PC-12 cell neurite extension". The Journal of Biological Chemistry. 278 (37): 35394–402. doi:10.1074/jbc.M302179200. PMID 12819211.
- ^ Murray AJ, Shewan DA (Aug 2008). "Epac mediates cyclic AMP-dependent axon growth, guidance and regeneration". Molecular and Cellular Neurosciences. 38 (4): 578–88. doi:10.1016/j.mcn.2008.05.006. PMID 18583150. S2CID 871060.
- ^ Gelinas JN, Banko JL, Peters MM, Klann E, Weeber EJ, Nguyen PV (Jun 2008). "Activation of exchange protein activated by cyclic-AMP enhances long-lasting synaptic potentiation in the hippocampus". Learning & Memory. 15 (6): 403–11. doi:10.1101/lm.830008. PMC 2414251. PMID 18509114.
- ^ Ster J, de Bock F, Bertaso F, Abitbol K, Daniel H, Bockaert J, Fagni L (Jan 2009). "Epac mediates PACAP-dependent long-term depression in the hippocampus". The Journal of Physiology. 587 (Pt 1): 101–13. doi:10.1113/jphysiol.2008.157461. PMC 2670026. PMID 19001039.
- ^ Métrich M, Lucas A, Gastineau M, Samuel JL, Heymes C, Morel E, Lezoualc'h F (Apr 2008). "Epac mediates beta-adrenergic receptor-induced cardiomyocyte hypertrophy". Circulation Research. 102 (8): 959–65. doi:10.1161/CIRCRESAHA.107.164947. PMID 18323524.
- ^ a b Hothi SS, Gurung IS, Heathcote JC, Zhang Y, Booth SW, Skepper JN, Grace AA, Huang CL (Nov 2008). "Epac activation, altered calcium homeostasis and ventricular arrhythmogenesis in the murine heart". Pflügers Archiv. 457 (2): 253–70. doi:10.1007/s00424-008-0508-3. PMC 3714550. PMID 18600344.
- ^ a b Pereira L, Cheng H, Lao DH, Na L, van Oort RJ, Brown JH, Wehrens XH, Chen J, Bers DM (Feb 2013). "Epac2 mediates cardiac β1-adrenergic-dependent sarcoplasmic reticulum Ca2+ leak and arrhythmia". Circulation. 127 (8): 913–22. doi:10.1161/CIRCULATIONAHA.12.148619. PMC 3690126. PMID 23363625.
- ^ a b Kim M, Platt MJ, Shibasaki T, Quaggin SE, Backx PH, Seino S, Simpson JA, Drucker DJ (May 2013). "GLP-1 receptor activation and Epac2 link atrial natriuretic peptide secretion to control of blood pressure". Nature Medicine. 19 (5): 567–75. doi:10.1038/nm.3128. PMID 23542788. S2CID 17013438.
- ^ Seino S, Takahashi H, Takahashi T, Shibasaki T (Jan 2012). "Treating diabetes today: a matter of selectivity of sulphonylureas". Diabetes, Obesity & Metabolism. 14 Suppl 1: 9–13. doi:10.1111/j.1463-1326.2011.01507.x. PMID 22118705. S2CID 7446914.
- ^ Takahashi H, Shibasaki T, Park JH, Hidaka S, Takahashi T, Ono A, Song DK, Seino S (Apr 2015). "Role of Epac2A/Rap1 signaling in interplay between incretin and sulfonylurea in insulin secretion". Diabetes. 64 (4): 1262–72. doi:10.2337/db14-0576. PMID 25315008.
- ^ McPhee I, Gibson LC, Kewney J, Darroch C, Stevens PA, Spinks D, Cooreman A, MacKenzie SJ (Dec 2005). "Cyclic nucleotide signalling: a molecular approach to drug discovery for Alzheimer's disease". Biochemical Society Transactions. 33 (Pt 6): 1330–2. doi:10.1042/BST20051330. PMID 16246111.
- ^ Bacchelli E, Blasi F, Biondolillo M, Lamb JA, Bonora E, Barnby G, Parr J, Beyer KS, Klauck SM, Poustka A, Bailey AJ, Monaco AP, Maestrini E (Nov 2003). "Screening of nine candidate genes for autism on chromosome 2q reveals rare nonsynonymous variants in the cAMP-GEFII gene". Molecular Psychiatry. 8 (11): 916–24. doi:10.1038/sj.mp.4001340. PMID 14593429.
- ^ Srivastava DP, Woolfrey KM, Jones KA, Anderson CT, Smith KR, Russell TA, Lee H, Yasvoina MV, Wokosin DL, Ozdinler PH, Shepherd GM, Penzes P (2012). "An autism-associated variant of Epac2 reveals a role for Ras/Epac2 signaling in controlling basal dendrite maintenance in mice". PLOS Biology. 10 (6): e1001350. doi:10.1371/journal.pbio.1001350. PMC 3383751. PMID 22745599.