물 모델
Water model계산 화학에서는 물 모델을 사용하여 물 군집, 액체 물, 명시적 용제를 사용한 수용액을 시뮬레이션하고 열역학적으로 계산한다. 모델은 양자역학, 분자역학, 실험결과, 그리고 이러한 조합으로 결정된다. 분자의 특정 성질을 모방하기 위해, 많은 종류의 모델이 개발되었다. 일반적으로 이러한 점들은 (i) 현장이라고 불리는 상호작용 지점의 수, (ii) 모형이 강성 또는 유연성 여부, (iii) 모형에 양극화 효과를 포함하는지 여부 등 3가지 점으로 분류할 수 있다.
명시적 물 모델의 대안은 연속체 모델이라고도 불리는 암묵적 용해 모델을 사용하는 것인데, 그 예로는 COSMO 용해 모델 또는 편광 가능 연속체 모델(PCM) 또는 복합 용해 모델 등이 있다.[1]
심플 워터 모델
강성 모델은 가장 단순한 물 모델로 간주되며 비결합 교호작용에 의존한다. 이러한 모델에서 본딩 상호작용은 홀로노믹 제약조건에 의해 암묵적으로 처리된다. 정전 상호작용은 쿨롱의 법칙과 레너드-존스 전위를 이용한 분산 및 반발력을 이용하여 모델링한다.[2][3] TIP3P(3 포인트의 전달 가능한 분자간 전위) 및 TIP4P와 같은 모델의 잠재력은 다음과 같다.
여기서 정전 상수인 k는C 분자 모델링에[citation needed] 일반적으로 사용되는 단위에서 332.1 å·kcal/(mol·e²)의 값을 가지며,[4][5][6] q와i q는j 전자 전하와 관련된 부분 전하, r은ij 두 원자 또는 충전된 부위 사이의 거리, A와 B는 레너드-존스 매개변수다. 충전된 부위는 원자 또는 더미 사이트(예: 단독 쌍)에 있을 수 있다. 대부분의 물 모델에서 레너드-존스 용어는 산소 원자 사이의 상호작용에만 적용된다.
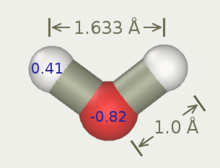
아래 그림은 3-6개 지점의 물 모델의 일반적인 모양을 보여준다. 정확한 기하학적 파라미터(OH 거리 및 HOH 각도)는 모델에 따라 다르다.
2사이트
친숙한 3-사이트 SPC 모델(아래 참조)을 기반으로 한 2-사이트 물 모델에서는 사이트 재생 분자 유체 이론을 사용하여 물의 유전체 특성을 예측하는 것으로 나타났다.[7]
3사이트
3개소 모델에는 물 분자의 세 원자에 해당하는 세 개의 상호작용 지점이 있다. 각 부위는 점 전하를 가지며, 산소 원자에 해당하는 부위도 레나드-존스 매개변수를 가진다. 3-사이트 모델은 높은 계산 효율을 달성하므로, 이것들은 분자 역학 시뮬레이션의 많은 응용에 널리 사용된다. 대부분의 모델들은 실제 물 분자와 일치하는 단단한 지오메트리를 사용한다. 예외적으로 SPC 모델은 이상적인 사면체(HOH 각도 109.47°)를 가정한다. 104.5°의 관측 각도 대신
아래 표에는 일부 3개 사이트 모델의 파라미터가 나열되어 있다.
| 팁[8] | SPC[9] | TIP3P[10] | SPC/E[11] | |
|---|---|---|---|---|
| r(OH), å | 0.9572 | 1.0 | 0.9572 | 1.0 |
| HOH, deg | 104.52 | 109.47 | 104.52 | 109.47 |
| A, 103 kcal å12/mol | 580.0 | 629.4 | 582.0 | 629.4 |
| B, kcal Ⅱ6/mol | 525.0 | 625.5 | 595.0 | 625.5 |
| q(O) | −0.80 | −0.82 | −0.834 | −0.8476 |
| q(H) | +0.40 | +0.41 | +0.417 | +0.4238 |
SPC/E 모델은 잠재적 에너지 기능에 평균 편광 보정을 추가한다.
여기서 μ는 효과적으로 편광된 물 분자의 전기 쌍극성 모멘트(SPC/E 모델의 경우 2.35D), μ는0 격리된 물 분자의 쌍극성 모멘트(실험에서 1.85D), α는i 등방성 편광성 상수로 값이 1.608×10−40 F·m이다2. 모델의 전하가 일정하기 때문에, 이 보정은 단지 총 에너지에 1.25 kcal/mol(5.22 kJ/mol)을 더하는 결과를 낳는다. SPC/E 모델은 SPC 모델보다 밀도와 확산 상수가 더 우수하다.
CHARMM 힘 필드에 구현된 TIP3P 모델은 원본의 약간 수정된 버전이다. 차이점은 레너드-존스 매개변수에 있다: TIP3P와는 달리, 모델의 CARMM 버전은 레너드-존스 매개변수를 산소 원자에 더하여 수소 원자에 배치한다. 요금은 수정되지 않는다.[12] TIP3P(Three-site model)는 특정 히트를 계산하는 데 있어 성능이 더 우수하다.[13]
유연한 SPC 물 모델
유연한 단순 충전 물 모델(또는 유연한 SPC 물 모델)은 3개소 SPC 물 모델을 재모수화한 것이다.[14][15] SPC 모델은 경직된 반면, 유연한 SPC 모델은 유연하다. 투칸과 라만의 모델에서는 O-H 스트레칭이 하모닉으로 되어 있어 역동적인 행동이 잘 묘사되어 있다. 이는 양극화를 고려하지 않고 가장 정확한 3중방 물 모델 중 하나이다. 분자역학 시뮬레이션에서 그것은 물의 정확한 밀도와 유전적 허용률을 제공한다.[16]
플렉시블 SPC는 MDynaMix와 전복 프로그램에서 구현된다.
기타 모델
4개소
4-사이트 모델은 3-사이트 모델의 HOH 각도의 이등분자를 따라 산소 근처에 1개의 더미 원자를 추가함으로써 4개의 상호작용 지점을 가진다(그림에 M으로 표시됨). 더미 원자는 음전하를 가질 뿐이다. 이 모델은 물 분자 주위의 정전기 분포를 개선한다. 이 접근법을 사용한 첫 번째 모델은 1933년에 출판된 베르날-파울러 모델이었는데,[21] 이것은 또한 가장 초기 물 모델이 될 수도 있다. 그러나 BF 모델은 물의 밀도, 기화열 등 대량 특성을 잘 재현하지 못해 역사적 관심사만 갖고 있다. 이것은 매개변수화 방법의 결과물이다; 현대적인 컴퓨터가 보급된 후에 개발된 새로운 모델들은 Metropolitanes Monte Carlo나 분자역학 시뮬레이션을 실행하고 대량 특성이 충분히 재현될 때까지 매개변수를 조정함으로써 매개변수를 분석하였다.
1983년에 처음 발표된 TIP4P 모델은 계산 화학 소프트웨어 패키지에 널리 구현되어 있으며, 생체 분자 시스템의 시뮬레이션에 자주 사용된다. 이후 TIP4P 모델은 Ewald 합계 방법과 함께 사용하기 위한 TIP4P-Ew 모델, 고체 물 얼음의 시뮬레이션을 위한 TIP4P/Ice, 그리고 응축수의 전체 위상도를 시뮬레이션하기 위한 일반적인 매개변수인 TIP4P/2005를 특정 용도에 맞게 재측정하였다.
대부분의 4-사이트 워터 모델은 자유수분자의 OH 거리와 HOH 각도를 사용한다. OPC 모델은 예외로 물 분자의 기본2v C 분자 대칭 이외에는 기하학적 제약이 가해져 있지 않다. 대신 점 전하와 그 위치는 물 분자의 전기학을 가장 잘 묘사하도록 최적화된다. OPC는 일반적으로 사용되는 강체 n-사이트 물 모델보다 더 정확하게 일련의 포괄적인 벌크 특성을 재현한다. OPC 모델은 황색 힘 필드에서 구현된다.
| BF[21] | 팁2[22] | TIP4P[10] | TIP4P-Ew[23] | TIP4P/얼음[24] | TIP4P/2005[25] | OPC[26] | TIP4P-D[27] | |
|---|---|---|---|---|---|---|---|---|
| r(OH), å | 0.96 | 0.9572 | 0.9572 | 0.9572 | 0.9572 | 0.9572 | 0.8724 | 0.9572 |
| HOH, deg | 105.7 | 104.52 | 104.52 | 104.52 | 104.52 | 104.52 | 103.6 | 104.52 |
| r(OM), å | 0.15 | 0.15 | 0.15 | 0.125 | 0.1577 | 0.1546 | 0.1594 | 0.1546 |
| A, 103 kcal å12/mol | 560.4 | 695.0 | 600.0 | 656.1 | 857.9 | 731.3 | 865.1 | 904.7 |
| B, kcal Ⅱ6/mol | 837.0 | 600.0 | 610.0 | 653.5 | 850.5 | 736.0 | 858.1 | 900.0 |
| q(M) | −0.98 | −1.07 | −1.04 | −1.04844 | −1.1794 | −1.1128 | −1.3582 | −1.16 |
| q(H) | +0.49 | +0.535 | +0.52 | +0.52422 | +0.5897 | +0.5564 | +0.6791 | +0.58 |
기타:
- q-TIP4P/F(가연성)
5개소
5개소 모델은 4면체 같은 기하학적 구조를 가진 산소 원자의 외로운 쌍을 나타내는 더미 원자(레이블 L)에 음전하를 배치한다. 이들 유형의 초기 모델은 1971년 제안된 벤-나이임과 스틸링거의 BNS 모델이었는데,[citation needed] 곧 1974년 스틸링거와 라만의 ST2 모델이 뒤를 이었다.[28] 주로 높은 계산 비용 때문에 5개 사이트 모델은 마호니와 조르겐센의 TIP5P 모델이 출판된 2000년까지는 별로 개발되지 않았다.[29] TIP5P 모델은 이전 모델과 비교했을 때 워터디머의 기하학적 구조 개선, 중성자 회절에서 실험 방사분포 기능을 더 잘 재현하는 보다 "계측" 물 구조 및 물의 최대 밀도 온도 개선으로 이어진다. TIP5P-E 모델은 TIP5P를 Ewald sums와 함께 사용하기 위해 재평가한 것이다.
| BNS[28] | ST2[28] | TIP5P[29] | TIP5P-E[30] | |
|---|---|---|---|---|
| r(OH), å | 1.0 | 1.0 | 0.9572 | 0.9572 |
| HOH, deg | 109.47 | 109.47 | 104.52 | 104.52 |
| r(OL), å | 1.0 | 0.8 | 0.70 | 0.70 |
| ㅋㅋㅋㅋㅋㅋㅋㅋㅋㅋㅋㅋㅋㅋㅋㅋㅋㅋㅋㅋㅋㅋㅋㅋㅋㅋㅋㅋㅋㅋㅋㅋㅋㅋㅋㅋㅋ | 109.47 | 109.47 | 109.47 | 109.47 |
| A, 103 kcal å12/mol | 77.4 | 238.7 | 544.5 | 554.3 |
| B, kcal Ⅱ6/mol | 153.8 | 268.9 | 590.3 | 628.2 |
| q(L) | −0.19562 | −0.2357 | −0.241 | −0.241 |
| q(H) | +0.19562 | +0.2357 | +0.241 | +0.241 |
| RL, å | 2.0379 | 2.0160 | ||
| RU, å | 3.1877 | 3.1287 |
그러나, BNS와 ST2 모델은 정전기 용어에 대해 쿨롱의 법칙을 직접 사용하는 것이 아니라, 단거리에서 스위칭 함수 S(r)에 곱하여 크기를 줄인 변형된 버전이라는 점에 유의한다.
따라서 R과L R 매개변수는U BNS와 ST2에만 적용된다.
6-사이트
원래 물/얼음 시스템을 연구하기 위해 고안된 것으로, 4-5 사이트 모델의 모든 부지를 결합한 6 사이트 모델은 나다와 반 데어 에르덴이 개발했다.[31] 주기적인 정전기 조건(Ewald Summation)에서 채용했을 때 용해 온도가[32] 매우 높았기 때문에, 나중에[33] 쿨롱 상호작용 추정에 Ewald 방법을 사용하여 최적화하여 수정된 버전이 발표되었다.
기타
- 생체 분자 시뮬레이션에서 명시적 용해 모델이 용해 행동에 미치는 영향도 광범위하게 연구되었다. 명시적 물 모델이 펼쳐지는 펩타이드의 특정 용해와 역동성에 영향을 미치는 한편, 접힌 펩타이드의 순응적 행동과 유연성은 그대로 유지되는 것으로 나타났다.[34]
- MB 모델. 물의 일부 특징을 2차원 시스템으로 재현한 메르세데스-벤츠 로고를 닮은 보다 추상적인 모델. 그것은 "실제" (즉, 3차원) 시스템의 시뮬레이션에는 사용되지 않지만, 질적 연구와 교육 목적에는 유용하다.[35]
- 굵은 결이 있는 모델. 1, 2지점 물의 모델도 개발되었다.[36] 굵은 회색 모델에서 각 부위는 여러 개의 물 분자를 나타낼 수 있다.
- 다체 모델. 교육 세트 구성을 사용하여 구축된 워터 모델은 양자 문제를 기계적으로 해결했으며, 기계 학습 프로토콜을 사용하여 잠재적 에너지 표면을 추출한다. 이러한 잠재적 에너지 표면은 응축된 위상 시스템의 물리적 특성 계산에 있어 전례 없는 수준의 정확도를 위해 MD 시뮬레이션에 주입된다.[37]
- 많은 차체 모델의[38] 또 다른 분류는 기본 전기학(예: SCME(Single Center Multipole Expansion) 모델)의 확장에 기초한다.
계산원가
물 시뮬레이션을 위한 계산 비용은 물 모델의 상호작용 지점의 수에 따라 증가한다. CPU 시간은 계산해야 하는 원자간 거리의 수에 대략 비례한다. 3-사이트 모델의 경우 각 물 분자 쌍(다른 분자의 모든 원자에 대한 한 분자의 모든 원자 또는 3 × 3)에 대해 9개의 거리가 필요하다. 4-사이트 모델의 경우 10개의 거리가 필요하다(모든 충전 사이트와 O-O 상호작용, 또는 3 × 3 + 1) 5-사이트 모델의 경우 17개 거리(4 × 4 + 1)가 필요하다. 마지막으로, 6-사이트 모델의 경우 26개 거리(5 × 5 + 1)가 필요하다.
분자 역학에서 강체 물 모델을 사용할 경우 제약 알고리즘을 사용하여 구조를 제약적으로 유지하는 것과 관련된 추가 비용이 있다(결합 길이가 제약되는 경우 시간 단계를 증가시키는 것이 종종 가능함).
참고 항목
참조
- ^ Skyner RE, McDonagh JL, Groom CR, van Mourik T, Mitchell JB (March 2015). "A review of methods for the calculation of solution free energies and the modelling of systems in solution" (PDF). Physical Chemistry Chemical Physics. 17 (9): 6174–91. Bibcode:2015PCCP...17.6174S. doi:10.1039/C5CP00288E. PMID 25660403.
- ^ Allen MP, Tildesley DJ (1989). Computer Simulation of Liquids. Clarendon Press. ISBN 978-0-19-855645-9.
- ^ Kirby BJ. Micro- and Nanoscale Fluid Mechanics: Transport in Microfluidic Devices.
- ^ Swails JM, Roitberg AE (2013). "prmtop file of {A}mber" (PDF).
- ^ Swails JM (2013). Free energy simulations of complex biological systems at constant pH (PDF). University of Florida.
- ^ Case DA, Walker RC, Cheatham III TE, Simmerling CL, Roitberg A, Merz KM, et al. (April 2019). "Amber 2019 reference manual (covers Amber18 and AmberTools19)" (PDF).
- ^ Dyer KM, Perkyns JS, Stell G, Pettitt BM (2009). "Site-renormalised molecular fluid theory: on the utility of a two-site model of water". Molecular Physics. 107 (4–6): 423–431. Bibcode:2009MolPh.107..423D. doi:10.1080/00268970902845313. PMC 2777734. PMID 19920881.
- ^ Jorgensen, William L. (1981). "Quantum and statistical mechanical studies of liquids. 10. Transferable intermolecular potential functions for water, alcohols, and ethers. Application to liquid water". Journal of the American Chemical Society. American Chemical Society (ACS). 103 (2): 335–340. doi:10.1021/ja00392a016. ISSN 0002-7863.
- ^ H. J. C. 베렌슨, J. P. M. 포스트마, W. F. 반 건스테인, J. Hermans, In Molecular Force, B에 의해 편집되었다. 풀먼(Reidel, Dordrecht, 1981), 페이지 331.
- ^ a b Jorgensen WL, Chandrasekhar J, Madura JD, Impey RW, Klein ML (1983). "Comparison of simple potential functions for simulating liquid water". The Journal of Chemical Physics. 79 (2): 926–935. Bibcode:1983JChPh..79..926J. doi:10.1063/1.445869.
- ^ Berendsen HJ, Grigera JR, Straatsma TP (1987). "The missing term in effective pair potentials". The Journal of Physical Chemistry. 91 (24): 6269–6271. doi:10.1021/j100308a038.
- ^ MacKerell AD, Bashford D, Bellott M, Dunbrack RL, Evanseck JD, Field MJ, et al. (April 1998). "All-atom empirical potential for molecular modeling and dynamics studies of proteins". The Journal of Physical Chemistry B. 102 (18): 3586–616. doi:10.1021/jp973084f. PMID 24889800.
- ^ Mao Y, Zhang Y (2012). "Thermal conductivity, shear viscosity and specific heat of rigid water models". Chemical Physics Letters. 542: 37–41. Bibcode:2012CPL...542...37M. doi:10.1016/j.cplett.2012.05.044.
- ^ Toukan K, Rahman A (March 1985). "Molecular-dynamics study of atomic motions in water". Physical Review B. 31 (5): 2643–2648. Bibcode:1985PhRvB..31.2643T. doi:10.1103/PhysRevB.31.2643. PMID 9936106.
- ^ Berendsen HJ, Grigera JR, Straatsma TP (1987). "The missing term in effective pair potentials". Journal of Physical Chemistry. 91 (24): 6269–6271. doi:10.1021/j100308a038.
- ^ Praprotnik M, Janezic D, Mavri J (2004). "Temperature Dependence of Water Vibrational Spectrum: A Molecular Dynamics Simulation Study". Journal of Physical Chemistry A. 108 (50): 11056–11062. Bibcode:2004JPCA..10811056P. doi:10.1021/jp046158d.
- ^ Ferguson, David M. (April 1995). "Parameterization and evaluation of a flexible water model". Journal of Computational Chemistry. 16 (4): 501–511. doi:10.1002/jcc.540160413. Retrieved 28 July 2021.
- ^ MG 모델.
- ^ Kumagai N, Kawamura K, Yokokawa T (1994). "An Interatomic Potential Model for H2O: Applications to Water and Ice Polymorphs". Molecular Simulation. Informa UK Limited. 12 (3–6): 177–186. doi:10.1080/08927029408023028. ISSN 0892-7022.
- ^ Burnham CJ, Li J, Xantheas SS, Leslie M (1999). "The parametrization of a Thole-type all-atom polarizable water model from first principles and its application to the study of water clusters (n=2–21) and the phonon spectrum of ice Ih". The Journal of Chemical Physics. 110 (9): 4566–4581. Bibcode:1999JChPh.110.4566B. doi:10.1063/1.478797.
- ^ a b Bernal JD, Fowler RH (1933). "A Theory of Water and Ionic Solution, with Particular Reference to Hydrogen and Hydroxyl Ions". The Journal of Chemical Physics. 1 (8): 515. Bibcode:1933JChPh...1..515B. doi:10.1063/1.1749327.
- ^ Jorgensen (1982). "Revised TIPS for simulations of liquid water and aqueous solutions". The Journal of Chemical Physics. 77 (8): 4156–4163. Bibcode:1982JChPh..77.4156J. doi:10.1063/1.444325.
- ^ Horn HW, Swope WC, Pitera JW, Madura JD, Dick TJ, Hura GL, Head-Gordon T (May 2004). "Development of an improved four-site water model for biomolecular simulations: TIP4P-Ew". The Journal of Chemical Physics. 120 (20): 9665–78. Bibcode:2004JChPh.120.9665H. doi:10.1063/1.1683075. PMID 15267980.
- ^ Abascal JL, Sanz E, García Fernández R, Vega C (June 2005). "A potential model for the study of ices and amorphous water: TIP4P/Ice". The Journal of Chemical Physics. 122 (23): 234511. Bibcode:2005JChPh.122w4511A. doi:10.1063/1.1931662. PMID 16008466.
- ^ Abascal JL, Vega C (December 2005). "A general purpose model for the condensed phases of water: TIP4P/2005". The Journal of Chemical Physics. 123 (23): 234505. Bibcode:2005JChPh.123w4505A. doi:10.1063/1.2121687. PMID 16392929.
- ^ Izadi S, Anandakrishnan R, Onufriev AV (November 2014). "Building Water Models: A Different Approach". The Journal of Physical Chemistry Letters. 5 (21): 3863–3871. arXiv:1408.1679. Bibcode:2014arXiv1408.1679I. doi:10.1021/jz501780a. PMC 4226301. PMID 25400877.
- ^ Piana S, Donchev AG, Robustelli P, Shaw DE (April 2015). "Water dispersion interactions strongly influence simulated structural properties of disordered protein states". The Journal of Physical Chemistry B. 119 (16): 5113–23. doi:10.1021/jp508971m. PMID 25764013.
- ^ a b c Stillinger FH, Rahman A (1974). "Improved simulation of liquid water by molecular dynamics". The Journal of Chemical Physics. 60 (4): 1545–1557. Bibcode:1974JChPh..60.1545S. doi:10.1063/1.1681229.
- ^ a b Mahoney MW, Jorgensen WL (2000). "A five-site model for liquid water and the reproduction of the density anomaly by rigid, nonpolarizable potential functions". The Journal of Chemical Physics. 112 (20): 8910–8922. Bibcode:2000JChPh.112.8910M. doi:10.1063/1.481505.
- ^ Rick SW (April 2004). "A reoptimization of the five-site water potential (TIP5P) for use with Ewald sums". The Journal of Chemical Physics. 120 (13): 6085–93. Bibcode:2004JChPh.120.6085R. doi:10.1063/1.1652434. PMID 15267492.
- ^ Nada, H. (2003). "An intermolecular potential model for the simulation of ice and water near the melting point: A six-site model of H2O". The Journal of Chemical Physics. 118 (16): 7401. Bibcode:2003JChPh.118.7401N. doi:10.1063/1.1562610.
- ^ Abascal JL, Fernández RG, Vega C, Carignano MA (October 2006). "The melting temperature of the six site potential model of water". The Journal of Chemical Physics. 125 (16): 166101. Bibcode:2006JChPh.125p6101A. doi:10.1063/1.2360276. PMID 17092145.
- ^ Nada H (December 2016). "2O and a molecular dynamics simulation". The Journal of Chemical Physics. 145 (24): 244706. Bibcode:2016JChPh.145x4706N. doi:10.1063/1.4973000. PMID 28049310.
- ^ Florová P, Sklenovský P, Banáš P, Otyepka M (November 2010). "Explicit Water Models Affect the Specific Solvation and Dynamics of Unfolded Peptides While the Conformational Behavior and Flexibility of Folded Peptides Remain Intact". Journal of Chemical Theory and Computation. 6 (11): 3569–79. doi:10.1021/ct1003687. PMID 26617103.
- ^ Silverstein KA, Haymet AD, Dill KA (1998). "A Simple Model of Water and the Hydrophobic Effect". Journal of the American Chemical Society. 120 (13): 3166–3175. doi:10.1021/ja973029k.
- ^ Izvekov S, Voth GA (October 2005). "Multiscale coarse graining of liquid-state systems". The Journal of Chemical Physics. AIP Publishing. 123 (13): 134105. Bibcode:2005JChPh.123m4105I. doi:10.1063/1.2038787. PMID 16223273.
- ^ Medders GR, Paesani F (March 2015). "Infrared and Raman Spectroscopy of Liquid Water through "First-Principles" Many-Body Molecular Dynamics". Journal of Chemical Theory and Computation. 11 (3): 1145–54. doi:10.1021/ct501131j. PMID 26579763.
- ^ Cisneros GA, Wikfeldt KT, Ojamäe L, Lu J, Xu Y, Torabifard H, et al. (July 2016). "Modeling Molecular Interactions in Water: From Pairwise to Many-Body Potential Energy Functions". Chemical Reviews. 116 (13): 7501–28. doi:10.1021/acs.chemrev.5b00644. PMC 5450669. PMID 27186804.
- ^ Wikfeldt KT, Batista ER, Vila FD, Jónsson H (October 2013). "A transferable H2O interaction potential based on a single center multipole expansion: SCME". Physical Chemistry Chemical Physics. 15 (39): 16542–56. arXiv:1306.0327. doi:10.1039/c3cp52097h. PMID 23949215.