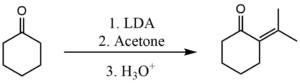자가 응축
Self-condensation자가 응축은 알돌 응결에서 카르보닐 그룹을 포함하는 화학 화합물이 전기와 핵 화합물 역할을 모두 하는 유기적 반응이다.전기와 핵이 다른 종인 혼합 알돌 응결과는 반대로 대칭 알돌 응결이라고도 한다.
예를 들어 아세톤의 두 분자는 이온교환수지가 있는 곳에서 산화비만 단일 화합물에 응축된다.[1]
- 2 CH3COCH3 → (CH3)2C=CH(CO)CH3 + H2O
합성 용도의 경우, 이것은 일반적으로 바람직하지 않지만 자발적이고 선호하는 알돌 응축의 부작용이며, 이를 방지하기 위한 특별한 예방 조치가 필요하다.
자가 응결 방지
많은 경우, 자기 응축은 원치 않는 부작용이다.따라서 화학자들은 교차 알돌 반응을 할 때 이런 일이 일어나지 않도록 여러 가지 방법을 채택해 왔다.
보다 반응성이 높은 전기 시설과 양도할 수 없는 파트너의 사용
수성 NaOH가 있는 곳에서 아세토페논과 벤츠알데히드를 합친다면, 오직 하나의 제품만 형성된다.
이는 벤츠알데히드에는 굴절 가능한 양성자가 없어 에놀레이트를 형성할 수 없고 벤츠알데히드는 용액에 있는 어떤 비염색 아세토페논보다 훨씬 전기영양성이 뛰어나기 때문에 발생한다.따라서 아세토페논으로 형성된 에놀레이트는 항상 다른 아세토페논 분자 위에 있는 벤츠알데히드를 우선적으로 공격할 것이다.[2]
에놀레이트 이온을 정량적으로 만들기
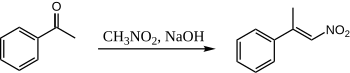
수용성 NaOH를 사용하여 니트로메탄과 아세토페논을 결합하면 다음 중 하나의 제품만 형성된다.
여기서 아세토페논은 결코 스스로 응결할 기회를 얻지 못하는데, 니트로메탄은 훨씬 더 산성적이어서 니트로가 양적으로 "에놀레이트"가 만들어지기 때문이다.아세토페논과 니트로메탄 사이의 응축에 대한 알려진 절차는 없다.
두 케톤 사이의 자가 응결 방지에도 유사한 과정을 사용할 수 있다.그러나 이 경우 사용된 베이스는 더욱 강력해질 필요가 있다.사용되는 공통 베이스는 리튬디이소프로필아미드(LDA)이다.여기서는 아세톤과 사이클로헥사논 사이의 교차 응결을 수행하기 위해 사용된다.[3]
LDA를 사용하는 감응 단계는 매우 빨라서 형성된 에놀레이트(Enolate)는 시클로헥사논의 어떤 미작동 분자와도 반응할 기회를 얻지 못한다.그러면 에놀레이트(enolate)는 아세톤과 빠르게 반응한다.
실릴 에톨 에테르 형성
알데히드로부터 에놀레이트 이온을 만들려고 할 때 LDA를 사용하는 것은 작동하지 않을 것이다.그들은 매우 반응적이어서 자기 응결이 일어날 것이다.이를 극복하는 한 가지 방법은 알데히드를 트리메틸릴 염화물과 트리메틸아민 같은 염기성분을 이용하여 실릴 에놀에테르로 만든 다음 알돌결로 하는 것이다.여기서 이 전술은 아세트알데히드와 벤츠알데히드의 응축에 사용된다.결로를 촉진하기 위해서는 TiCl과4 같은 루이스 산을 사용해야 한다.[4]
참조
- ^ Sulfonic acid Ion Exchange 수지 N. Lorette; J. Org를 이용한 Ketone 응축. 화학; 1957; 22(3); 346-347.
- ^ 클레이든, 조나단.유기 화학옥스포드 대학 출판부, 뉴욕 옥스포드, 689-720페이지. ISBN978-0-19-850346-0
- ^ 클레이든, 조나단.유기 화학옥스포드 대학 출판부, 뉴욕 옥스포드, 689-720페이지.ISBN 978-0-19-850346-0
- ^ 클레이든, 조나단.유기 화학옥스포드 대학 출판부, 뉴욕 옥스포드, 689-720페이지.ISBN 978-0-19-850346-0