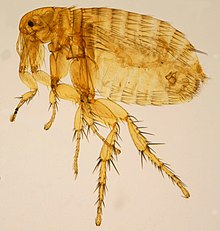
리케치아티푸스
Rickettsia typhi리케치아 티푸스는 작고, 호기성, 의무적인 세포 내,[1] 막대 모양의 그램 음성 박테리아입니다.R. premazekii와 [2]함께 리케치아속 발진티푸스군에 속한다.R.[3] 발진티푸스는 전염성 발진티푸스에 의해 오랫동안 그림자가 드리워졌을지도 모르기 때문에 불확실한 역사를 가지고 있다.이 박테리아는 생물학적 격납 수준 2/3 [1][4]유기체로 인식된다.R. 발진티푸스는 벼룩에 의해 전염되는 질병으로 [3]전 세계에 분포하는 사람에게서 발생하는 발진티푸스인 쥐 발진티푸스의 원인 물질로 가장 잘 알려져 있다.모든 리케츠성 유기체와 마찬가지로, R. 발진티푸스는 발열, 두통, 통증, [5][6]발진 등의 비특이적인 가벼운 증상을 보이는 쥐 발진티푸스를 일으키는 동물성 물질이다.R. 티푸스를 포함한 동물 저장고에서 인간으로 R. 티푸스가 전염되는 두 가지 주기가 있습니다: 가장 잘 연구되고 흔한 전형적인 쥐-벼룩 순환과 고양이, 개, 주머니쥐, 양, 그리고 그들의 [7]벼룩을 포함할 수 있는 2차 시기 순환입니다.
R. 티푸스는 한때 전 세계적으로 리케츠병의 가장 일반적인 원인 중 하나였지만, 그 이후 해충 방제 프로그램의 [8][9][10]시행으로 사례 보고가 감소했습니다.이 미생물은 병원균의 [8][9]숙주인 쥐와 벼룩이 풍부한 따뜻한 기후와 해안 항구에 집중되어 있다.티푸스는 벼룩에 물려 감염된 배설물과 [8][11]조직과 접촉함으로써 유능한 벼룩과 포유류 숙주 사이에서 전염된다.
Rickettial 종의 진단에는 [8]혈청학에 기초한 전통적인 진단과 함께 몇 가지 실험실 테스트가 있습니다.그러나 실시간 PCR과 마이크로면역형광과 같은 새로운 실험실 기술을 사용하여 리케시아 티푸스 종 수준까지 [9]리케시아를 더 빠르게 식별할 수 있습니다.
| 리케치아티푸스 | |
|---|---|
| 과학적 분류 | |
| 도메인: | 박테리아 |
| 문: | 슈도모나도타속 |
| 클래스: | 알파프로테오박테리아 |
| 주문: | 리케치아레스 |
| 패밀리: | 리케치아과 |
| 속: | 리케치아 |
| 종군: | 발진티푸스군 |
| 종류: | 티푸스 |
| 이항명 | |
| 리케치아티푸스 (월바흐와 토드, 1920) 필립, 1943년 | |
역사와 분류법
20세기 초 유행성 발진티푸스는 세계 곳곳에 만연했다.그것은 높은 사망률, 높은 독성과 관련이 있으며 [12]이를 통해 전염되는 것으로 생각되었다.이 기간 동안 덜 심각하고 추적할 수 없는 사례들이 [12]나타나기 시작했다.이러한 경우는 발열, 발진, 두통, 근골격계 및 위장의 [13]징후가 특징이었다.역학자인 Kenneth F Maxy는 이를 인식하고 R. prowazekii 외에 또 다른 발진티푸스의 존재에 대해 의문을 제기하고 격리하기 시작했는데,[12] 그는 1926년에 발표된 기사에서 이것을 자세히 설명했다.맥시는 이 새로운 형태의 발진티푸스를 전파하는 또 다른 절지동물 벡터의 존재를 추측했는데, 이것은 나중에 R. [12]발진티푸스로 밝혀지게 된다.발진티푸스 그룹 멤버인 R. promazekii에 [14]비해 R. 발진티푸스는 역사적으로 진단을 받은 것으로 생각된다.R. 발진티푸스의 발견은 R. 발진티푸스와 R. promazekii를 [2]포함하는 발진티푸스 그룹 Rickettia의 탄생으로 이어졌다.리케치아 종은 일반적으로 반점열 그룹, 발진티푸스 그룹,[2] 관목 발진티푸스 그룹 등 세 그룹으로 나뉜다.
세포형태 및 운동성
리케치아 티푸스는 작고, 호기성, 의무적인 세포 내,[1] 막대 모양의, 그램 음성 박테리아입니다.R. 티푸스는 생물 격납 레벨 2/3 유기체로 인식되는 동물성 박테리아입니다(작업 [1][15]중인 조직에 따라 다름).필수 세포 내 병원체로서 R. 티푸스는 분리하기가 어려울 수 있으며 대부분의 다른 [16]유기체에서 볼 수 있는 표준 도금 방법을 사용하여 배양할 수 없습니다.R. 티푸스는 운동성이며, 방향성과 속도에 대한 제어가 거의 없이 액틴 기반의 운동성을 통해 움직임을 만들어 내고, 종종 원형 [17]패턴으로 움직이는 것을 볼 수 있다.
독성
리케티아 티푸스는 벼룩 매개성 질병 유기체로 [18]전 세계에 널리 분포되어 있다.R. 티푸스가 동물 저수지에서 인간으로 전염되는 데는 두 가지 주기가 있습니다: 전형적인 쥐벼룩 순환과 고양이, 개, 주머니쥐, 양,[7] 그리고 그들의 벼룩과 관련된 주경 순환입니다.
전형적인 쥐-벼룩-쥐 사이클
R. 발진티푸스는 쥐(Rattus 랫투스 또는 Rattus norvegicus)와 쥐벼룩(Xenopysla [19]cheopis) 사이에서 순환하지만 다른 설치류와 그 외부 기생충도 [20]자연에서 발진티푸스를 유지하는 역할을 한다.쥐벼룩은 R. 발진티푸스의 주요 매개체이지만, P. H. 휴머너스, 폴립팩스 이, 그리고 쥐의 흡혈 진드기는 자연적 또는 [19][3]실험적으로 R. 발진티푸스를 얻을 수 있는 것으로 보고되었다.
쥐벼룩에서 R. 티푸스의 전염은 수혈 중 또는 수혈 후에 리케시아가 함유된 벼룩 배설물과 접촉하거나 벼룩에 [14]물린 후 영향을 받습니다.리케치아이는 벡터나 쥐의 적합성에 해로운 영향을 미치지 않으며, 진정한 상호 [21]관계를 보여줍니다.감염된 벼룩은 R. 티푸스를 평생 유지할 수 있으며, 많은 수의 민감한 [21]숙주를 감염시킬 수 있는 잠재력을 제공합니다.
가정 주기
지금까지 전염의 주기적인 동물성 주기에 대한 연구는 많지 않았으며, 대부분은 고양이에게 초점을 맞추고 있다.
R. 티푸스는 고양이와 사람을 [22]쉽게 물 수 있는 벼룩종인 고양이 벼룩인 Ctenocephalides felis에 존재할 수 있는 것으로 나타났다.지금까지 고양이로부터 인간 R. 발진티푸스에 대한 직접적인 감염은 없었으며, 대신 같은 [23][24]지리적 위치에서 인간 발진티푸스에 관련된 높은 감염률의 고양이들 사이의 연관성은 있었다.
R. 티푸스 [23]전염 주기에 주머니쥐뿐만 아니라 개와 [25]양과 같은 다른 가축들도 관여할 수 있다는 증거도 있지만, 현재 연구는 제한적이다.
병인 발생
리케치아 스펜서R. 티푸스를 포함한 혈액을 통해 퍼져서 혈관에 있는 내피를 감염시킨다.이는 혈관 염증, 혈관 건전성 손상, 혈관 투과성 저하로 이어지며, 이를 총칭하여 '리케치아 혈관염'이라고 한다.
질병
사람의 쥐발진티푸스(내혈성 발진티푸스)
리케티아 발진티푸스는 사람에게서 쥐 발진티푸스의 원인물질로 [26]전 세계에 분포한다.그것은 주로 설치류의 벼룩에 의해 전염되는 급성 열성 질환으로, 일반적으로 도시 쥐(Rattus rattus와 Rattus norvegicus)[26]가 많은 도시와 항구와 관련이 있다.인간은 [20][27]쥐가 들끓는 질병 종말 지역을 방문할 때 감염된 벼룩이나 벼룩 배설물을 피부에 직접 주입하거나 흡입함으로써 감염에 감염된다.대부분의 환자들은 열이 있고, 많은 환자들은 발진과 [26]두통이 있지만, 뇌, 폐, 간, 신장 및 심장 내피 [28][29]감염을 포함한 광범위한 다계통 질환으로 이어질 수 있다.이러한 징후와 증상들은 다른 리케치아이를 포함한 다른 질병들에 의해 발생하는 것과 비슷하기 때문에,[27] 쥐 발진티푸스는 임상적으로 진단하기가 어렵다.비균일적, 비특이적 증상뿐만 아니라 질병의 급성 단계에서 효과적인 진단 테스트가 부족하여 [1]적절한 치료가 지연된다.쥐 발진티푸스는 임상적으로 경미할 수 있지만, 심각하고 심지어 치명적인 사례가 [21]보고되었다.쥐 발진티푸스 감염의 심각성은 나이, 인종, 그리고 진단 [21]지연과 관련이 있다.독시사이클린은 비록 감염된 사람들의 99%가 특별한 [1]치료 없이도 몇 주 안에 병을 치료할 수 있지만,[26] 병의 진행을 단축시키는 것으로 보여지기 때문에 선택되는 항생제이다.
역학
지리적, 시간적 분포
리케시아 발진티푸스는 포유류와 [30]벼룩의 쥐 발진티푸스 감염을 일으키는 작고 그램 음성 세포 내 박테리아이다.뮤린 발진티푸스는 한때 세계에서 [8][9][10]가장 흔한 리케츠병 중 하나였으며, 남극을 제외한 전 세계의 [14][11]거의 모든 대륙에서 R. 발진티푸스의 원인물질을 분리했다.이 박테리아는 널리 분포하고 있을 뿐만 아니라 연중 온난한 기후를 자랑하며 [8][9][14]연안에 포근해 있는 지역에 특히 많이 분포하고 있다.이러한 선호는 벼룩과 야생동물 숙주의 생존에 유리한 기후 조건 때문에 리케치아 생물을 [8][10][9][14]환경 내 저수지로 유지할 수 있는 더 많은 풍요로움과 능력 때문이다.항구는 감염된 설치류와 그들의 외부기생충이 [14]선박의 국제적인 이동을 통해 유입될 수 있기 때문에 R. 티푸스에게는 예외적인 항구이다.이들 항구는 그 후 주요 [14]교역로를 따라 있는 인근 도시로 병원체를 옮길 수 있다.R. 티푸스 감염의 급증은 벼룩 개체수가 특히 [8][14]많은 봄부터 가을 초까지 보고된다.
역사적으로,[8][9][10][14] 미국에서 매년 수천 건의 쥐 발진티푸스 사례가 보고되었지만, 1940년대에 도시 주택에서 [8][14]리케트 전염에 책임이 있는 벼룩과 설치류 저수지를 제거하는 해충 방제 프로그램이 시행되면서 발병률이 갑자기 감소하였다.현재 쥐 발진티푸스 감염은 더 산발적이고 드물게 발생하며 미국에서는 [9][14]연간 100명 미만의 환자가 보고되고 있다.그럼에도 불구하고, R. 티푸스는 여전히 공중 보건에 상당한 중요성을 지닌 박테리아로 간주되고 있으며, 미국 남부, 남유럽, 아시아,[8][9][10][14] 아프리카, 그리고 호주에서 일반적으로 발병 사례가 보고되고 있다.R. 발진티푸스는 비특이적이고 가벼운 임상 증상(열, 두통, 전신통증, 발진)[9][10][14][25] 때문에 종종 과소 보고되고 오진되기 때문에 실제로 측정치보다 높은 것으로 추정된다.진단되지 않은 감염이 보고된 환자 수보다 4:1 [14]더 많을 것으로 예측된다.최근의 연구는 브라질 아마존에서 일하는 환자의 임상 사례를 제시했고, 환자가 이 박테리아에 특정한 항체를 제시했기 때문에 아마도 리케치아 티푸스에 의해 야기된 것으로 보이는 불특정 열성 질환을 나타냈다.이는 R. 티푸스의 지리적 분포가 [31]예상보다 넓을 수 있음을 보여준다.
호스트 범위 및 전송
R. 티푸스 미생물은 벼룩 숙주의 중간구트 상피 세포와 포유류의 [30]혈관 구조를 따라 늘어선 내피 세포에 의무적으로 존재한다.이 박테리아의 수명은 고전적으로 동양쥐벼룩(Xensymmella cheopis)[8][9][10][14]과 검은쥐(Rattus rattus)와 갈색쥐(Rattus norveicus)를 포함한다.이 세계적으로 분산된 호스트들 특히 많은 이유 때문에 이 rickettsiae 전송에:Xcheopis 포유류의 호스트의 인간을 포함한 다양한 종류의 박테리아를 전송할 수 있은 엄청나게 넓은 숙주 범위는 로사 Rattus의[14]명 Rtyphi 2분열의 eukary 내에 거대한 라운드를 거칠 수 있게 해 능통하다.otic세포와 벼룩 [14]벡터를 감염시킬 수 있는 박테리아 수를 증가시킨다.쥐와 그들의 벼룩 외에도, 고양이와 그들의 벼룩, 주머니쥐, 말쥐, 스컹크, 집쥐 그리고 그들의 [25]벼룩,[8][14] 그리고 거의 개를 포함한 다른 숙주들도 자연적으로 극미기생물을 옮기는 것이 관찰되었습니다.고양이와 주머니쥐들은 그들의 비호감성 외부 기생충과 [10][14]인간과의 긴밀한 연관성 때문에 도시 환경에서 쥐 발진티푸스를 위한 꽤 중요한 저장소로 여겨진다.
이 박테리아는 감염된 쥐(또는 다른 포유동물 숙주)로부터 혈액을 통해 민감한 쥐 벼룩(또는 다른 절지동물 벡터)으로 전염되며,[8][14][11] 감염된 벼룩에서 감염된 쥐의 배설물이나 벡터의 조직과 직접 접촉하여 다른 민감한 쥐에게 전염된다.절지동물 대변과의 접촉을 통한 전염은 열린 상처, 호흡기(호흡기) 또는 포유동물 [14]숙주의 결막을 통해 이루어질 수 있다.절지동물 [14]벡터에서 특정 잠복기를 거친 후에도 벼룩에 물려 전염될 수 있다는 증거가 있다.암컷 벼룩은 또한 대뇌전달을 [8][14]통해 자손에게 감염을 옮길 수 있다.R. 티푸스는 숙주의 수명이나 [14]생식력에 아무런 영향을 미치지 않는 무증상적인 감염만 일으키기 때문에 이러한 곤충과 비인간 숙주와 진정한 공생 상태에 있는 것으로 보인다.R. 티푸스 박테리아는 전염성이 다양하기 때문에 풍토 지역에서 [14]그 수를 지속시키는 데 매우 성공적이다.
동물성 전위
모든 리케치아에 종들과 마찬가지로, R. 티푸스는 인간이 비정상적인 막다른 숙주 역할을 하는 동물성 물질이기 때문에, 박테리아의 전염과 라이프 [14][32]사이클에서 생태학적 역할을 하지 않는다.인간은 실내 환경에서 벼룩과 쥐 R. 티푸스 매개체를 통해 가장 흔하게 감염되며, 일반적으로 무거운 설치류와 벼룩 [14]개체군을 둘러싼 직업이나 생활 환경에서 개인에게 영향을 미칩니다.쥐 발진티푸스 질환은 일반적으로 가벼운 질환으로 간주되며 치료되지 않은 [10]환자의 경우 치사율이 4%이다.질병이 [10][14]진행됨에 따라 종종 입원이 필요한 노인 환자들에게 있어서 적절한 쥐 발진티푸스 감시가 특히 중요하다.
진단 및 식별
Rickettial 종의 진단에 사용할 수 있는 실험실 테스트에는 쉘 바이알 검사, PCR 기반 검출, 면역 검출, 순환 내피 세포 및 혈청 진단 테스트(예: Weil-Felix 검사, CF 검사, ELISA, 마이크로 면역 산화효소, 블롯 및 웨스턴 면역 검사)[6]가 포함됩니다.
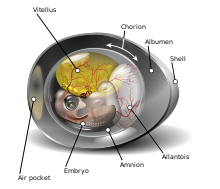
전통적으로, 리케시아의 진단은[33] 혈청학에 기초했지만, 혈청학적 검사는 증상이 시작된 후 진단적으로 유의한 R. tyhpi의 [34]티터가 나타나기까지 약 15일이 소요됩니다.그래서 환자가 회복되거나 [6]사망한 후에 종종 진단이 확인된다.R. 티푸스는 무균 상태에서는 자랄 수 없으며, 조직이나 배아 [16]샘플에서 자라야 합니다.엄격한 생리적 조건이 충족되더라도 숙주 세포질의 환경을 모방한 배지에서 배양되면 병원체 활성은 [16]오래가지 못한다.R. 티푸스를 키우는 일반적인 방법은 배아 알의 [16]노른자 주머니를 통해서이다.
실시간 PCR과 마이크로면역 형광과 같은 실험실 기술을 사용하여 리케시아를 [35][5]종 수준까지 식별할 수 있습니다.미세면역형광은 R.[10] 티푸스에 의한 감염을 확인하기 위해 풍토 지역에서 종종 사용되는 매우 민감한 검사이다.실시간 PCR을 사용하면 혈청학적 [35]테스트보다 빨리 R. 티푸스의 검출과 확인을 할 수 있습니다.막단백질 ompB 및 prsA 유전자 조각은 R.[36] 티푸스에 대한 qPCR에서 식별 가능한 마커로 나타났다.
R. prowazekii와의 차별화
R. 티푸스와 R. prowazekii의 증상은 매우 유사할 수 있으며, R. 티푸스 감염은 보통 덜 심각하다.R. 발진티푸스와 발진티푸스 그룹 멤버 R. prowazeki는 매우 유사한 게놈으로 구성되어 있으며, R. prowazekii에 [1]삽입된 12,000개의 염기쌍에 의해 R. prowazeki와 구별할 수 있다.발진티푸스 그룹 멤버를 구별하는 방법은 다양하다.한 가지 방법은 제한 단편 길이 다형성(RFLP)을 통해, 각 [37]종마다 고유한 염기서열을 가진 옴피 유전자와 관련 효소를 기반으로 두 종을 구분할 수 있다.혈청학적 방법도 유용합니다.간접 형광 항체 분석과 웨스턴 블롯 분석을 함께 활용하면 종 [38]간 신뢰할 수 있는 분화가 이루어지는 것으로 나타났다.혈청 교차 흡착제 분석만으로도 두 종 간의 교차 반응이 [38]일반적이기 때문에 분화를 위한 신뢰할 수 있는 방법이다.
참고 문헌
- ^ a b c d e f g McLeod, Michael P.; Qin, Xiang; Karpathy, Sandor E.; Gioia, Jason; Highlander, Sarah K.; Fox, George E.; McNeill, Thomas Z.; Jiang, Huaiyang; Muzny, Donna; Jacob, Leni S.; Hawes, Alicia C. (2004-09-01). "Complete Genome Sequence of Rickettsia typhi and Comparison with Sequences of Other Rickettsiae". Journal of Bacteriology. 186 (17): 5842–5855. doi:10.1128/JB.186.17.5842-5855.2004. ISSN 0021-9193. PMC 516817. PMID 15317790.
- ^ a b c Mansueto, Pasquale; Vitale, Giustina; Cascio, Antonio; Seidita, Aurelio; Pepe, Ilenia; Carroccio, Antonio; di Rosa, Salvatore; Rini, Giovam Battista; Cillari, Enrico (2011-09-06). "New Insight into Immunity and Immunopathology of Rickettsial Diseases". Clinical and Developmental Immunology. 2012: 967852. doi:10.1155/2012/967852. PMC 3170826. PMID 21912565.
- ^ a b c Azad, A. F.; Traub, R. (October 1989). "Experimental transmission of murine typhus by Xenopsylla cheopis flea bites". Medical and Veterinary Entomology. 3 (4): 429–433. doi:10.1111/j.1365-2915.1989.tb00251.x. ISSN 0269-283X. PMID 2519693. S2CID 24176171.
- ^ Rauch, Jessica; Eisermann, Philip; Noack, Bernd; Mehlhoop, Ute; Muntau, Birgit; Schäfer, Johannes; Tappe, Dennis (July 2018). "Typhus Group Rickettsiosis, Germany, 2010–20171". Emerging Infectious Diseases. 24 (7): 1213–1220. doi:10.3201/eid2407.180093. ISSN 1080-6040. PMC 6038764. PMID 29912688.
- ^ a b Schriefer, M E; Sacci, J B; Dumler, J S; Bullen, M G; Azad, A F (1994). "Identification of a novel rickettsial infection in a patient diagnosed with murine typhus". Journal of Clinical Microbiology. 32 (4): 949–954. doi:10.1128/jcm.32.4.949-954.1994. ISSN 0095-1137. PMC 267160. PMID 8027348.
- ^ a b c Scola, B. La; Raoult, D. (1997-11-01). "Laboratory diagnosis of rickettsioses: current approaches to diagnosis of old and new rickettsial diseases". Journal of Clinical Microbiology. 35 (11): 2715–2727. doi:10.1128/jcm.35.11.2715-2727.1997. ISSN 0095-1137. PMC 230049. PMID 9350721.
- ^ a b c Sahni, Sanjeev K; Rydkina, Elena (2009-03-30). "Host-cell interactions with pathogenic Rickettsia species". Future Microbiology. 4 (3): 323–339. doi:10.2217/fmb.09.6. ISSN 1746-0913. PMC 2775711. PMID 19327117.
- ^ a b c d e f g h i j k l m n o Eremeeva, Marina E.; Dasch, Gregory A. (2012-01-01), Long, Sarah S. (ed.), "179 - Other Rickettsia Species", Principles and Practice of Pediatric Infectious Diseases (Fourth Edition), London: Content Repository Only!, pp. 930–938.e4, ISBN 978-1-4377-2702-9, retrieved 2020-10-06
- ^ a b c d e f g h i j k Whiteford, Sarah F.; Taylor, Jeffery P.; Dumler, J. Stephen (2001-03-01). "Clinical, Laboratory, and Epidemiologic Features of Murine Typhus in 97 Texas Children". Archives of Pediatrics & Adolescent Medicine. 155 (3): 396–400. doi:10.1001/archpedi.155.3.396. ISSN 1072-4710. PMID 11231808.
- ^ a b c d e f g h i j k Schriefer, M. E.; Sacci, J. B.; Dumler, J. S.; Bullen, M. G.; Azad, A. F. (1994-04-01). "Identification of a novel rickettsial infection in a patient diagnosed with murine typhus". Journal of Clinical Microbiology. 32 (4): 949–954. doi:10.1128/JCM.32.4.949-954.1994. ISSN 0095-1137. PMC 267160. PMID 8027348.
- ^ a b c Abdad, Mohammad Yazid; Abdallah, Rita Abou; Fournier, Pierre-Edouard; Stenos, John; Vasoo, Shawn (2018-08-01). "A Concise Review of the Epidemiology and Diagnostics of Rickettsioses: Rickettsia and Orientia spp". Journal of Clinical Microbiology. 56 (8). doi:10.1128/JCM.01728-17. ISSN 0095-1137. PMC 6062794. PMID 29769278.
- ^ a b c d Maxcy, Kenneth F. (1926). "An Epidemiological Study of Endemic Typhus (Brill's Disease) in the Southeastern United States: With Special Reference to Its Mode of Transmission". Public Health Reports. 41 (52): 2967–2995. doi:10.2307/4578110. JSTOR 4578110.
- ^ Whiteford, Sarah F.; Taylor, Jeffery P.; Dumler, J. Stephen (2001-03-01). "Clinical, Laboratory, and Epidemiologic Features of Murine Typhus in 97 Texas Children". Archives of Pediatrics & Adolescent Medicine. 155 (3): 396–400. doi:10.1001/archpedi.155.3.396. ISSN 1072-4710. PMID 11231808.
- ^ a b c d e f g h i j k l m n o p q r s t u v w x y z aa ab Azad, A F (January 1990). "Epidemiology of Murine Typhus". Annual Review of Entomology. 35 (1): 553–570. doi:10.1146/annurev.en.35.010190.003005. ISSN 0066-4170. PMID 2105686.
- ^ Rauch, Jessica; Eisermann, Philip; Noack, Bernd; Mehlhoop, Ute; Muntau, Birgit; Schäfer, Johannes; Tappe, Dennis (July 2018). "Typhus Group Rickettsiosis, Germany, 2010–20171". Emerging Infectious Diseases. 24 (7): 1213–1220. doi:10.3201/eid2407.180093. ISSN 1080-6040. PMC 6038764. PMID 29912688.
- ^ a b c d Liu, Dongyou (2015-01-01). "Rickettsia". Molecular Medical Microbiology: 2043–2056. doi:10.1016/B978-0-12-397169-2.00111-6. ISBN 9780123971692.
- ^ Heinzen, Robert A. (2003). "Rickettsial Actin-Based Motility". Annals of the New York Academy of Sciences. 990 (1): 535–547. Bibcode:2003NYASA.990..535H. doi:10.1111/j.1749-6632.2003.tb07424.x. ISSN 1749-6632. PMID 12860687. S2CID 84913142.
- ^ Azad, A. F.; Radulovic, S.; Higgins, J. A.; Noden, B. H.; Troyer, J. M. (1997). "Flea-borne rickettsioses: ecologic considerations". Emerging Infectious Diseases. 3 (3): 319–327. doi:10.3201/eid0303.970308. ISSN 1080-6040. PMC 2627639. PMID 9284376.
- ^ a b TRAUB, R; R, TRAUB; JR, WISSEMAN CL; AZAD, ABDULRAHMAN FARHANG (1978). "The ecology of murine typhus-a critical review". The Ecology of Murine Typhus. A Critical Review. 75 (4): 237–317. PMID 705902.
- ^ a b Eremeeva, Marina E.; Warashina, Wesley R.; Sturgeon, Michele M.; Buchholz, Arlene E.; Olmsted, Gregory K.; Park, Sarah Y.; Effler, Paul V.; Karpathy, Sandor E. (October 2008). "Rickettsia typhi and R. felis in Rat Fleas (Xenopsylla cheopis), Oahu, Hawaii". Emerging Infectious Diseases. 14 (10): 1613–1615. doi:10.3201/eid1410.080571. ISSN 1080-6040. PMC 2609893. PMID 18826827.
- ^ a b c d Gillespie, Joseph J.; Ammerman, Nicole C.; Beier-Sexton, Magda; Sobral, Bruno S.; Azad, Abdu F. (2009-03-01). "Louse- and flea-borne rickettsioses: biological and genomic analyses". Veterinary Research. 40 (2): 12. doi:10.1051/vetres:2008050. ISSN 0928-4249. PMC 2695025. PMID 19036234.
- ^ Nogueras, Maria Mercedes; Pons, Immaculada; Ortuño, Ana; Miret, Jaime; Pla, Julia; Castellà, Joaquim; Segura, Ferran (2013-08-06). "Molecular Detection of Rickettsia typhi in Cats and Fleas". PLOS ONE. 8 (8): e71386. Bibcode:2013PLoSO...871386N. doi:10.1371/journal.pone.0071386. ISSN 1932-6203. PMC 3735526. PMID 23940746.
- ^ a b Adjemian, Jennifer; Parks, Sharyn; McElroy, Kristina; Campbell, Jill; Eremeeva, Marina E.; Nicholson, William L.; McQuiston, Jennifer; Taylor, Jeffery (2010). "Murine Typhus in Austin, Texas, USA, 2008 - Volume 16, Number 3—March 2010 - Emerging Infectious Diseases journal - CDC". Emerging Infectious Diseases. 16 (3): 412–7. doi:10.3201/eid1603.091028. PMC 3322020. PMID 20202415.
- ^ Sorvillo, Frank J.; Gondo, Barbara; Emmons, Richard; Ryan, Patrick; Waterman, Stephen H.; Tilzer, Arthur; Andersen, Ellen M.; Murray, Robert A.; Barr, A. Ralph (1993-02-01). "A Suburban Focus of Endemic Typhus in Los Angeles County: Association with Seropositive Domestic Cats and Opossums". The American Journal of Tropical Medicine and Hygiene. 48 (2): 269–273. doi:10.4269/ajtmh.1993.48.269. ISSN 0002-9637. PMID 8447530.
- ^ a b c Nogueras, María-Mercedes; Pons, Immaculada; Pla, Júlia; Ortuño, Anna; Miret, Jaime; Sanfeliu, Isabel; Segura, Ferran (2013-04-12). "The role of dogs in the eco-epidemiology of Rickettsia typhi, etiological agent of Murine typhus". Veterinary Microbiology. 163 (1–2): 97–102. doi:10.1016/j.vetmic.2012.11.043. ISSN 1873-2542. PMID 23290118.
- ^ a b c d Civen, Rachel; Ngo, Van (2008-03-15). "Murine Typhus: An Unrecognized Suburban Vectorborne Disease". Clinical Infectious Diseases. 46 (6): 913–918. doi:10.1086/527443. ISSN 1058-4838. PMID 18260783.
- ^ a b Henry, Katherine M.; Jiang, Ju; Rozmajzl, Patrick J.; Azad, Abdu F.; Macaluso, Kevin R.; Richards, Allen L. (2007-02-01). "Development of quantitative real-time PCR assays to detect Rickettsia typhi and Rickettsia felis, the causative agents of murine typhus and flea-borne spotted fever". Molecular and Cellular Probes. 21 (1): 17–23. doi:10.1016/j.mcp.2006.06.002. ISSN 0890-8508. PMID 16893625.
- ^ Walker, D. H.; Feng, H. M.; Ladner, S.; Billings, A. N.; Zaki, S. R.; Wear, D. J.; Hightower, B. (October 1997). "Immunohistochemical diagnosis of typhus rickettsioses using an anti-lipopolysaccharide monoclonal antibody". Modern Pathology. 10 (10): 1038–1042. ISSN 0893-3952. PMID 9346184.
- ^ Walker, David H.; Parks, Francis M.; Betz, Thomas G.; Taylor, Jeffery P.; Muehlberger, Joan W. (1989-06-01). "Histopathology and Immunohistologic Demonstration of the Distribution of Rickettsia typhi in Fatal Murine Typhus". American Journal of Clinical Pathology. 91 (6): 720–724. doi:10.1093/ajcp/91.6.720. ISSN 0002-9173. PMID 2499181.
- ^ a b Blanton, Lucas S.; Dumler, J. Stephen; Walker, David H. (2015-01-01), Bennett, John E.; Dolin, Raphael; Blaser, Martin J. (eds.), "192 - Rickettsia typhi (Murine Typhus)", Mandell, Douglas, and Bennett's Principles and Practice of Infectious Diseases (Eighth Edition), Philadelphia: Content Repository Only!, pp. 2221–2224.e2, ISBN 978-1-4557-4801-3, retrieved 2020-09-10
- ^ Minervino, Antonio H.H.; Labruna, Marcelo B.; Dias, Salatiel R.; Costa, Francisco B.; Martins, Thiago F.; da Silva, Phablo N.S.; Faccini-Martínez, Álvaro A. (September 2020). "Typhus Group Rickettsiosis, Brazilian Amazon". Emerging Infectious Diseases. 26 (9): 2294–2296. doi:10.3201/eid2609.201305. ISSN 1080-6040. PMC 7454102. PMID 32818424.
- ^ Walker, D. H.; Fishbein, D. B. (1991-05-01). "Epidemiology of rickettsial diseases". European Journal of Epidemiology. 7 (3): 237–245. doi:10.1007/BF00145672. ISSN 1573-7284. PMID 1884775. S2CID 1675131.
- ^ "Rickettsia typhi (Murine typhus)- Infectious Disease and Antimicrobial Agents". www.antimicrobe.org. Retrieved 2020-09-23.
- ^ Dumler, J. S. (1991-09-11). "Clinical and laboratory features of murine typhus in south Texas, 1980 through 1987". JAMA: The Journal of the American Medical Association. 266 (10): 1365–1370. doi:10.1001/jama.266.10.1365. ISSN 0098-7484.
- ^ a b Giulieri, Stefano; Jaton, Katia; Cometta, Alain; Trellu, Laurence T.; Greub, Gilbert (2012-02-01). "Development of a duplex real time PCR for the detection of Rickettsia spp. and typhus group rickettsia in clinical samples". FEMS Immunology & Medical Microbiology. 64 (1): 92–97. doi:10.1111/j.1574-695X.2011.00910.x. ISSN 0928-8244. PMID 22098502.
- ^ Papp, Stefanie; Rauch, Jessica; Kuehl, Svenja; Richardt, Ulricke; Keller, Christian; Osterloh, Anke (February 2017). "Comparative evaluation of two Rickettsia typhi-specific quantitative real-time PCRs for research and diagnostic purposes". Medical Microbiology and Immunology. 206 (1): 41–51. doi:10.1007/s00430-016-0480-z. ISSN 0300-8584. PMID 27696011. S2CID 1682815.
- ^ Peniche-Lara, Gaspar; Zavala-Velazquez, Jorge; Dzul-Rosado, Karla; Walker, D.H.; Zavala-Castro, Jorge (2013). "Simple Method to Differentiate among Rickettsia Species". Journal of Molecular Microbiology and Biotechnology. 23 (3): 203–208. doi:10.1159/000348298. ISSN 1660-2412. PMC 4714558. PMID 23595041.
- ^ a b La Scola, Bernard; Rydkina, Lena; Ndihokubwayo, Jean-Bosco; Vene, Sirkka; Raoult, Didier (2000-07-01). "Serological Differentiation of Murine Typhus and Epidemic Typhus Using Cross-Adsorption and Western Blotting". Clinical Diagnostic Laboratory Immunology. 7 (4): 612–616. doi:10.1128/CDLI.7.4.612-616.2000. ISSN 1098-6588. PMC 95923. PMID 10882661.