페탈렌
Pentalene | |
 | |
| 이름 | |
|---|---|
| 선호 IUPAC 이름 페탈렌[1] | |
| 기타 이름 바이클룩타테트라엔 | |
| 식별자 | |
3D 모델(JSmol) | |
| 체비 | |
| 켐스파이더 | |
펍켐 CID | |
CompTox 대시보드 (EPA) | |
| |
| |
| 특성. | |
| C8H6 | |
| 어금질량 | 102.102 g·message−1 |
달리 명시된 경우를 제외하고, 표준 상태(25°C [77°F], 100 kPa)의 재료에 대한 데이터가 제공된다. | |
| Infobox 참조 자료 | |
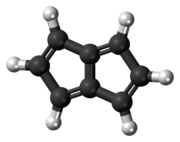
페탈렌은 두 개의 융합 사이클로펜타디엔 고리로 구성된 다순환 탄화수소다.[2] 그것은 화학 공식86 CH를 가지고 있다. n이 정수인 4n π 전자를 가지고 있기 때문에 반자율적이다. 이러한 이유로, 그것은 -100 °C의 낮은 온도에서도 희미해진다.[3][4] 파생상품 1,3,5-트리-테르트-부틸펜탈린은 1973년에 합성되었다.[5] 테르트 부틸 대체 물질 때문에 이 화합물은 열적으로 안정적이다. 예를 들어 벤조펜탈렌과 디벤조펜탈렌 화합물에서 벤조펜탈렌은 벤조판화에 의해서도 안정될 수 있다.[2]
딜리튬 페탈레니드는 1997년 페탈렌이 나오기 훨씬 전인 1962년에 격리되었다.[6] 디히드롭탈렌(디시클로펜타디엔 이소머의 용해효소)과 n-부틸리튬의 반응으로 준비돼 안정적인 소금을 형성한다. 그 구조물에 따라 양성자 NMR은 2대 1 비율로 2개의 신호를 보여준다. 두 개의 전자를 추가하면 반자율성이 제거된다; 그것은 평면 10㎛ 전자 방향족종이 되고 따라서 사이클로크타테트라엔(COT) 다이니온 CH의882− 자전거 아날로그가 된다.
다이니언은 또한 두 개의 융합 사이클로펜타디에닐 링으로 간주될 수 있으며, 여러 개의 금속-금속 결합을 포함하는 복합체와 센터 간의 전자 통신 수준이 극도로 높은 항바이메탈릭을 포함하여 많은 유형의 단핵 및 바이메탈 복합체를 안정시키기 위해 유기물 화학에서 리간드로 사용되어 왔다.[7]
참고 항목
참조
- ^ International Union of Pure and Applied Chemistry (2014). Nomenclature of Organic Chemistry: IUPAC Recommendations and Preferred Names 2013. The Royal Society of Chemistry. p. 209. doi:10.1039/9781849733069. ISBN 978-0-85404-182-4.
- ^ a b Hopf, Henning (2013). "Pentalenes-From Highly Reactive Antiaromatics to Substrates for Material Science". Angewandte Chemie International Edition. 52 (47): 12224–6. doi:10.1002/anie.201307162. PMID 24127399.
- ^ Carey, Francis A.; Sundberg, Richard J. (1984). Advanced Organic Chemistry: Part A Structure and Mechanisms (2nd ed.). New York, NY: Plenum Press. ISBN 0-306-41198-9.
- ^ Bally T.; Chai S.; Neuenschwander M.; Zhu Z. (1997). "Pentalene: Formation, Electronic, and Vibrational Structure" (PDF). J. Am. Chem. Soc. 119 (8): 1869–1875(7). doi:10.1021/ja963439t. Archived from the original (reprint) on 2007-03-15. Retrieved 2007-07-06.
- ^ Hafner, K.; Süss, H. U. (1973). "1,3,5-Tri-tert-Butylpentalene. A Stabilized Planar 8π-Electron System". Angew. Chem. Int. Ed. Engl. 12 (7): 575–577. doi:10.1002/anie.197305751.
- ^ Katz, Thomas J.; Rosenberger, Michael. (1962). "The Pentalenyl Dianion". Journal of the American Chemical Society. 84 (5): 865. doi:10.1021/ja00864a038.
- ^ Summerscales, Owen T.; Cloke, F. Geoffrey N. (2006). "The organometallic chemistry of pentalene". Coordination Chemistry Reviews. 250 (9–10): 1122. doi:10.1016/j.ccr.2005.11.020.