오존-산소 사이클
Ozone–oxygen cycle이 글은 검증을 위해 인용구가 추가로 필요하다.– · · 책· · (2010년 9월)(이 템플릿 |
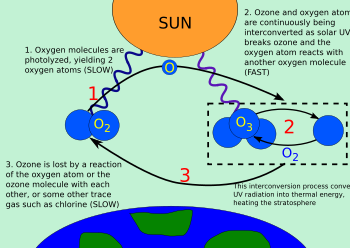
오존-산소 주기는 오존이 지구의 성층권에서 지속적으로 재생되어 자외선(UV)을 열로 변환시키는 과정이다. 1930년 시드니 채프먼은 관련된 화학을 해결했다. 이 과정은 일반적으로 대기 과학자들에 의해 채프먼 사이클이라고 불린다.
오존 생성의 대부분은 열대 상층 성층권과 중층권에서 발생한다. 지구상에서 하루에 생산되는 오존의 총량은 약 4억 미터톤이다. 오존의 지구 질량은 약 30억 미터 톤으로 비교적 일정하며, 이는 태양이 매일 오존층의 약 12%를 생산한다는 것을 의미한다.[1]
화학
| 다음에 대한 시리즈 일부 |
| 바이오게화학주기 |
|---|
 |
- 생성: 산소 분자는 고주파 UV 빛(UV-B, UV-C 이상의 상단 끝)에 의해 두 개의 산소 원자로 분할(사진화)된다(그림 참조).
- O2 + ℎν(<242 nm) → 2 O
- 그러면 각 산소 원자는 산소 분자와 빠르게 결합하여 오존 분자를 형성한다.
- O + O2 → O3
- 오존-산소 주기: 위의 반응에 의해 형성된 오존 분자는 UV-C와 UV-B 사이에 적절한 파장을 가진 방사선을 흡수한다. 3원자 오존 분자는 이원자 분자 산소와 자유 산소 원자가 된다(그림 참조).
- O3 + ℎν(240–310 nm) → O2 + O
- 생성된 원자 산소는 오존을 개혁하기 위해 다른 산소 분자와 빠르게 반응한다.
- O + O2 + A → O3 + A
- 여기서 A는 에너지와 운동량이2 보존되지 않기 때문에 반응에 필요한 N이나 O와2 같은 다른 분자나 원자를 의미한다. 여분의 운동에너지로 나타나는 반응의 과잉 에너지가 있다. 이 두 반응은 오존-산소 주기를 형성하는데, O와 O가2 결합할 때 방출되는 화학적 에너지가 분자 운동 에너지로 변환된다. 전체적인 효과는 침투하는 UV-B 빛을 오존의 순손실 없이 열로 변환하는 것이다. 이 사이클은 오존층을 안정적 균형으로 유지시키는 동시에 대부분의 생명체에게 해로운 자외선으로부터 낮은 대기를 보호한다. 또한 성층권의 두 가지 주요 열원 중 하나이다(또2 하나는 O가 O 원자로 광학화되었을 때 방출되는 운동에너지다).
- 제거: 산소 원자와 오존 분자가 만나면 두 개의 산소 분자를 형성하기 위해 재결합한다.
- O3 + O → 2 O2
- 그리고 두 산소 원자가 만나면, 그들은 하나의 산소 분자를 형성하기 위해 반응한다.
- 2 O → O2
성층권 오존의 전체 양은 태양 복사 생성과 제거 사이의 균형에 의해 결정된다. 자유 O 원자의 농도가 매우 낮기 때문에 제거 속도가 느리다.
방금 언급한 반응 외에 가장 중요한 특정 활성산소(OH), 질소산화물(NO)과 염소(Cl)와 브롬(Br) 원자가 재결합 반응을 촉진시켜 촉매제가 존재하지 않을 경우보다 얇은 오존층으로 이어진다.
OH와 NO의 대부분은 자연적으로 성층권에 존재하지만, 인간의 활동, 특히 클로로플루오로카본스(CFCs)와 할로겐의 배출은 Cl과 Br 농도를 크게 증가시켜 오존 파괴로 이어지고 있다. 각 Cl 또는 Br 원자는 성층권에서 제거되기 전에 수만 가지의 분해 반응을 촉진시킬 수 있다.
외부 링크
참조
- ^ "Chapter 5: Stratospheric Photochemistry". Stratospheric Ozone: An Electronic Textbook. Archived from the original on 2011-07-27. Retrieved 2011-06-16.