헤미아미날
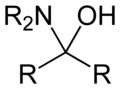
Hemiaminal헤미아미날(hemiaminal, 또한 카르비놀라민)은 히드록실 그룹과 아민이 동일한 탄소 원자에 부착된 기능 그룹 또는 화학 화합물의 유형이다: -C(OH)(NR2)-. R은 수소 또는 알킬 그룹일 수 있다. 헤미아민은 알킬리미노-데옥소-비스브리에 의한 아민과 카보닐로부터 이미인 형성의 매개체다.[1] 헤미아민은 수족관과 보석 다이올의 혼합물로 볼 수 있다. 그것들은 아미노 알코올의 특별한 경우다.
아민 전구체에 따른 분류
암모니아 첨가

알데히드에 암모니아를 첨가하여 형성된 인덕트는 오랫동안 연구되어 왔다.[2] 일차 아미노 그룹과 동일한 탄소 원자에 결합된 히드록실 그룹을 모두 포함하는 화합물은 드물다. 그것들은 작동되지만 암모니아와 알데히드, 케톤 등의 반응에서 매개체로 거의 관찰되지 않는다. 이러한 드문 기능성의 한 예는 암모니아와 헥사플루오로아세톤, (CF3)2C(OH)NH의2 첨가물이다.[3]
C 대체 파생상품은 알데히드 및 암모니아 반응을 통해 얻는다.[4]
- 3 RCHO + 3 NH3 → (RCHNH)3 + 3 HO2
기본 아민 추가
N 대체 파생상품은 다소 안정적이다. 이러한 N,N',N'-삼분해 헥사히드로-1,3,5-트리아진은 1,3,5-트리메틸-1,3,5-트리자시클로헥산까지의 경로에 의해 도해된 아민과 포름알데히드의 응축에서 발생한다.
- 3 CHO2 + 3 HNMe2 → (CHNMe2)3 + 3 HO2
1차 아민이나 암모니아에서 생성된 유도체는 보통 불안정하지만, 헤미아민은 충치에 갇혔다.[5]
2차 아민 추가: 카르비놀라민(헤미아민) 및 비사미노메탄
가장 간단한 반응 중 하나는 포름알데히드와 디메틸아민의 응결을 수반한다. 이 반응은 먼저 카르비놀아민(헤미아미날)과 비스(디메틸아미노)메탄(Me = CH3):[6][7]
- 메NH2 + CHO2 → 메엔쇼오22
- MeNH2 + MeNCHOH22 → MeNCHNMe222 + HO2
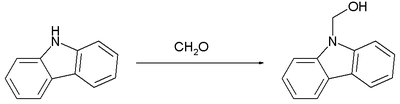
포름알데히드와 카바졸의 반응은 약하게 기초적인 것으로서 비슷하게 진행된다.[8]
다시 이 카르비놀은 메틸렌 연계 bis(카르바졸)로 쉽게 전환된다.
헤미아미날 에테르
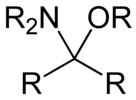
헤미아미날 에테르에는 다음과 같은 구조가 있다: R:-C(NR')2 (OR")-R⁗. 글리코사이아민들은 주기적인 뇌하수체 에테르들의 예들이다.
- 헤미아미나에테르
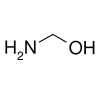
포름알데히드와 암모니아 반응의 중간 물질인 메탄올아민
Bis(hydroxymethyl)urea는 상업적으로 유용한 헤미아민이다.
격리성, 반복성 뇌하수체의 특이한 예: 암모니아와 헥사플루오로아세톤 유도체
총합성에 사용
헤미아미날 형성은 [9]삭렉톡신의 비대칭 총합성의 핵심 단계다.
이 반응 단계에서 알켄군은 우선 염화 오스뮴(III)과 옥소네(사성촉매) 및 탄산나트륨(기초)의 작용에 의해 중간 아실로 산화된다.
참고 항목
참조
- ^ Urbansky, Edward T. (2000). "Carbinolamines and Geminal Diols in Aqueous Environmental Organic Chemistry". Journal of Chemical Education. 77 (12): 1644. Bibcode:2000JChEd..77.1644U. doi:10.1021/ed077p1644.
- ^ Justus Liebig "Uber die er Oxydation des Alkohols" Annalen der Pharmicalie 1835, 14, 페이지 133–167. doi:10.1002/jlac.18350140202
- ^ W. J. Middleton, H. D. Carlson (1970). "Hexafluoroacetone imine". Org. Syntheses. 50: 81–3. doi:10.15227/orgsyn.050.0081..
- ^ Nielsen, Arnold T.; Atkins, Ronald L.; Moore, Donald W.; Scott, Robert; Mallory, Daniel; LaBerge, Jeanne M. (1973). "Structure and Chemistry of the Aldehyde Ammonias. 1-Amino-1-Alkanols, 2,4,6-Trialkyl-1,3,5-Hexahydrotriazines, and N,N-Dialkylidene-1,1-Diaminoalkanes". J. Org. Chem. 38 (19): 3288–3295. doi:10.1021/jo00959a010.
- ^ Iwasawa, T.; Hooley, R. J.; Rebek, J. (2007). "Stabilization of Labile Carbonyl Addition Intermediates by a Synthetic Receptor". Science. 317 (5837): 493–496. Bibcode:2007Sci...317..493I. doi:10.1126/science.1143272. PMID 17656719. S2CID 37292853.
- ^ Hellmann Heinrich, Günter Opitz (1960). Aminoalkylierung. Weinheim.
- ^ Rogers, F. E.; Rapiejko, R. J. (1974). "Thermochemistry of Carbonyl Addition Reactions. II. Enthalpy of Addition of Dimethylamine to Formaldehyde". The Journal of Physical Chemistry. 78 (6): 599–603. doi:10.1021/j100599a008.
- ^ Carbazol-9-yl-methanol Milata Viktora, Kada Rudolfa, Lokaj J¨nb Molbank 2004, M354 개방형 액세스 간행물 [1] 웨이백머신에 2018-09-26 보관
- ^ Fleming, James J.; McReynolds, Matthew D.; Du Bois, J. (2007). "(+)-Saxitoxin: A First and Second Generation Stereoselective Synthesis". Journal of the American Chemical Society. 129 (32): 9964–9975. doi:10.1021/ja071501o. PMID 17658800.
| 위키미디어 커먼즈에는 헤미아말스와 관련된 미디어가 있다. |