에리스트로포이에티오르포피리아
Erythropoietic protoporphyria| 에리스트로포이에티오르포피리아 | |
|---|---|
| 기타 이름 | EPP[1] |
 | |
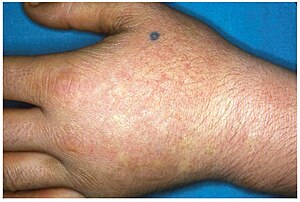
| EPP의 만성 피부병변 | |
| 전문 | 내분비내과, 피부과 |
| 위험요소 | 고통과 짜증 |
Erythropoietic prooppolphyria(또는 흔히 EPP라고 불리는)는 포르피리아의 일종으로, 중증도에 따라 다르며 매우 고통스러울 수 있다.페로켈라타아제 효소의 결핍으로 발생하여 적혈구(에로시테스), 혈장, 피부, 간에서 비정상적으로 높은 수준의 프로토폴피린으로 이어진다.[2]심각도는 개인마다 크게 다르다.
X-Linked 지배적인 프로토폴피피리아로 알려진 임상적으로 유사한 형태의 포르피리아가 2008년에 확인되었다.[3]
프리젠테이션
EPP는 보통 유년기에 가장 일반적인 표현 방식을 피부의 급성 광감성으로 제시한다.그것은 태양에 노출된 부위에 영향을 주고 난치성 경향이 있다.태양에 몇 분만 노출되면 명예, 홍반, 붓기, 통증을 유발한다.[4]장시간 노출되면 2도 화상을 입을 수 있다.반복적인 노출 후, 환자들은 감초화, 과대포화, 피부의 흉터가 나타날 수 있다.[5][6]
EPP는 보통 어린 시절에 처음 나타나며, 가장 자주 팔, 손, 발의 얼굴과 상단 표면과 다리의 노출된 표면에 영향을 미친다.대부분의 환자들은, 만약 EPP가 그렇게 심하지 않다면, 성 발달과 유지 과정에서 남성과 여성 호르몬 수치가 상승하는 사춘기가 시작되는 증상을 나타낸다.유아기에 더 심각한 EPP가 나타날 수 있다.EPP는 환자가 유리 뒤에 있더라도 햇빛에 노출되어 유발될 수 있다.심지어 완전한 보호 마스크를 사용한 아크 용접으로 인한 UV 배출도 EPP를 유발하는 것으로 알려져 있다.또한 EPP는 3세에서 6세 사이에 나타날 수 있다.
햇볕에 장시간 노출되면 손, 얼굴, 발의 부종이 올 수 있는데, 물집과 페테치아는 드물다.피부가 두꺼워지는 것은 때때로 시간이 지남에 따라 발생할 수 있다.
EPP를 가진 사람들은 또한 담석을 개발하는데 더 많은 위험에 처해있다.[7]한 연구는 EPP 환자들이 비타민 D 결핍을 앓고 있다는 것을 지적했다.[8]
간기능부전
프로포폴피린은 EPP 환자의 5~20%에서 간 내 독성 수준으로 축적돼 간 기능 부전으로 이어진다.EPP와 관련된 간섬유의 스펙트럼은 넓다.담낭염, 경미한 실질성 간질환, 진행성 간세포질환, 말기 간질환 등이 포함된다.[5]
간기능저하 진단표시가 부족해 어느 환자가 간기능저하를 겪을지 예측하기 어렵고, 간기능저하 메커니즘도 제대로 파악되지 않는다.유럽의 한 회고적 연구는 1983년과 2008년 사이에 간 이식을 받은 31명의 EPP 환자를 발견했는데, 수술용 조명 필터에 의해 보호받지 못한 환자의 25%에서 광산화 반응이 나타났다.같은 연구는 이식된 장기에서 69%의 질병이 재발했다는 것을 지적했다.1987년과 2009년 사이에 EPP를 위한 5개의 영국 간 이식이 확인되었다.현재까지 간 기능 장애를 관리하기 위한 효과적인 치료법이 확인되지 않은 EPP 환자에게는 빈번한 간 검사를 권고한다.[9]
임신
EPP 감광성 증상은 임신과 생리 중에 일부 여성 환자에서 감소하는 것으로 보고되지만 이러한 현상은 일관되지 않고 메커니즘을 이해하지 못한다.[10]
유전학
대부분의 EPP의 경우 신진대사의[2] 선천적인 오류의 결과지만 일부 환자의 대사 결함은 획득될 수 있다.[11]18번 염색체의 긴 팔에서 페로켈라타아제를 암호화하는 유전자의 돌연변이가 대부분의 사례에서 발견된다.페로첼라타아제(FECH)는 제철의 삽입을 프로토폴폴피린 IX 링에 촉진시켜 헤메를 형성한다.EPP는 열성적 및 지배적 상속 패턴과 불완전한 침투로 인한 높은 수준의 알레르기가성 이질성을 나타낸다.대부분의 이형체들은 무증상이다.FECH 활성도가 정상의 30% 미만인 경우가 아니면 증상이 발생하지 않지만, 대다수의 환자에게는 이러한 낮은 수준이 존재하지 않는다.[12]
병리학
hem을 합성하는 세포는 골수(80%)와 간세포(20%)에서 주로 홍반/소반구체(erythroblasts/reticulocity)가 많다.FECH의 결핍은 플라즈마에서 알부민에 결합하고 그 후에 간추출을 하는 프로토폴피린 분비를 증가시킨다.일반적으로 간세포에서 대부분의 양성포폴피린은 담즙으로 분비된다. 나머지는 헤메로 변형을 겪는다.담즙의 일부 프로토폴피린은 장내 순환의 결과로 간으로 되돌아간다; 장에 남아 있는 프로토폴피린은 배설 과정을 거친다.프로토폴포피린은 용해되지 않기 때문에 신장 배설에는 사용할 수 없다.EPP에서, 프로토폴피린에서 헤메로의 비정상적인 바이오트랜스 형성은 간세포에 프로토폴피린이 축적되는 결과를 초래한다.[13]
FECH 결핍은 홍반, 혈장, 피부, 간에서 프로토폴피린 농도의 증가와 관련이 있기 때문에, 피부에서 프로토폴피린 보유는 급성 광감성을 유발한다.혈액이 피부 혈관을 통해 순환할 때 플라즈마 및 홍반에서 프로토폴피린에 의해 자외선과 가시광선(피크 민감도 500~625nm[14] 이하)이 흡수된 결과 활성산소가 형성되고 홍반이 불안정해지고 피부 손상이 유도된다.[5]
장골포피린의 간 배설이 현저하게 증가하면 담석현상과 산화스트레스를[13] 통해 간을 손상시킬 수 있다 - 중증도가[15][16] 다양한 간경화 질환에 걸리기 쉽다.
진단
EPP는 일반적으로 피부의 급성 광감도의 존재에 의해 의심되며 634 nm의 플라스마 형광 피크를 감지하면 확인할 수 있다.또한 대변에서 프로토폴피린 수치가 증가하거나 홍반에서 프리 프로토폴피린 과다를 입증하는 것도 유용하다.[17]
선택된 가족 구성원의 한 알레일 또는 아미노레불린산 신타아제 2 기능상실 돌연변이에 대한 FECH 돌연변이의 선별은 특히 유전자 상담에 유용할 수 있다.
간 조직검사는 담도관측과 관문 대식세포 내에서 갈색 색소로 관찰될 수 있는 간세포에 프로토폴피린 침전물이 존재하여 EPP에서 간질환을 확인한다.거시적으로 볼 때, 권상 간은 프로토폴피피린 퇴적물로 인해 검은색을 가질 수 있다.편광된 빛을 사용하여 비레프링 결정성 색소 퇴적물의 특징적인 몰타 십자형을 발견한다.우드의 램프 아래 있는 간 조직을 검사해 보면 프로토폴피린에 의한 붉은 형광이 나타난다.간 조직검사는 간질환 예후 추정에 도움이 되지 않는다.[15]
치료
이 질환에 대한 치료법은 없지만, 증상은 대개 주간 태양과 일부 인공 조명에 대한 노출을 제한함으로써 관리될 수 있다.대부분의 유형의 인공조명은 문제가 있는 파장에서 빛을 발산하는데, 형광등은 최악의 범죄자다.색온도는 색온도가 높을수록 보라색(380~450nm)이 더 많이 방출되기 때문에 어떤 빛이 가장 해로운지 보여주는 좋은 지표일 수 있다.소프트 화이트 레인지(2700~3000K)의 백열등과 LED 조명은 가장 문제가 적은 빛을 낸다.또한 낮은 와트수 전구를 선택하면 전체 빛의 출력을 줄일 수 있다.
가시 스펙트럼의 빛에서 광감도가 발생하기 때문에 대부분의 자외선 차단제는 거의 쓸모가 없다(비나노 아연 산화물은 290[18]~400nm와 700nm까지 일부 보호를 제공한다).UPF 값을 가진 의류는 자외선 차단(최대 400nm)을 기준으로만 등급이 매겨지고 가시 스펙트럼으로부터의 보호에는 해당되지 않지만 자외선 차단 의류도 매우 유용할 수 있다.일부 자외선 차단 의류 제조업체는 쿨리바사의 ZnO 썬텍트 라인과 같은 직물에 산화아연을 사용해 가시광선으로부터 보호한다.[19]
일부 환자들은 자외선에 단시간 동안 정기적으로 노출되어 점차 멜라닌의 보호막을 형성한다.[citation needed]
최대 450nm까지 자외선과 가시광선을 차단하는 윈도우 필름은 환자의 자동차와 홈 윈도우에 적용하면 증상 완화를 제공할 수 있다.그러한 예로는 500nm 범위를 통해 보호할 수 있는 Madico Amber 81이 있다.
파란색 차단 스크린 보호기는 텔레비전, 전화, 태블릿, 컴퓨터 스크린에 의해 야기되는 증상들을 완화시키는 데 도움을 줄 수 있다.
EPP는 포르피리아 중 가장 덜 심각한 것으로 여겨진다.간기능저하가 없는 한 생명을 위협하는 병은 아니다.
승인된 치료법
호주계 크리누벨제약이 개발한 아프리카멜라노타이드(Afamelanotide)는 2014년 12월 유럽에서 EPP를 가진 성인의 광독성 치료 또는 예방 승인을 받았다.[20]
라벨이 없는 사용
EPP 환자들은 몇 가지 약물을 라벨에 붙이지 않고 사용한다.
- 우르소데옥시콜산(Ursodeoxycholic acid)은 양성포폴피린의 담도 분비를 촉진하기 위해 투여하는 담즙산이다.EPP에서의 그것의 사용 결과는 논쟁의 여지가 있다.그러나 담즙의 구성을 바꾸고, 소수 담즙산의 세포독성 효과로부터 간세포들을 보호하며, 몇 가지 뚜렷한 메커니즘에 의해 담도 분비를 자극하는 것으로 알려져 있다.[21][22]
- 헤마틴은 골수에서 과잉 프로토폴피린 생성을 감소시키는 것으로 보인다.간 이식 후 위기가 발생하는 EPP(3~4mg/kg iv) 환자에게 투여했다.[23]
- 플라스마페레시스 또한 혈장의 프로토폴피린 수치를 감소시킬 수 있지만, 급성 질환을 치료하는데 사용되는 것은 논란의 여지가 있다.[24]
- 콜로페트라민은 장에서 프로토폴피린과 결합하여 장내 순환을 방해함으로써 프로토폴피린의 순환 수치를 감소시키는 구강 투여 수지다.그것은 보통 다른 치료 접근법과 함께 사용된다.[25]
- 활성탄은 콜레스토레라민과 마찬가지로 장내의 프로토폴피피린과 결합하여 흡수를 막는다.그것은 싸고 쉽게 구할 수 있다.그것은 순환하는 프로토폴피피린 수치를 줄이는 데 효과적인 것 같다.[26]
골수이식, 간 이식, 아세틸시스틴, 체외 알부민 투석, 자궁 철분, 적혈구 수혈 등이 EEP 치료의 대안이다.
처방전 없이 살 수 있는 약
일부 처방전 없이 살 수 있는 약은 다음과 같은 도움을 줄 수 있다.
- 프로페린은 헤마틴과 유사하게 작용하는 구강 헤메 보충제다.
- B. 미분비(그람 양성의 토양 프로바이오틱스)는 페로켈라타아제를 생성하는데,[27] 이것은 장에 있는 프로토폴피린 일부를 헤메로 변환시킬 수 있을지도 모른다.
- 베타 카로틴은, 최근 카로틴 치료의 메타 분석은 그 효과에 의문을 제기하고 있다.[28]
역학
사례 보고서는 EPP가 전세계적으로 널리 퍼져 있음을 시사한다.유병률은 7만5천분의 1에서 20만분의[29] 1로 추정되었지만, 질병에 대한 이해도 향상과 진단 개선으로 인해 EPP의 유병률이 증가하고 있을 수 있다는 점에 주목했다.[30]전 세계적으로 약 5,000–1만 명의 사람들이 EPP를 가지고 있다.[medical citation needed]EPP는 어린이들에게 가장 흔한 형태의 포르피리아로 여겨진다.[31]스웨덴의 유병률은 1:18만 명으로 발표되었다.[32]
역사
Erythropoietic prooppyria는 Kosenow와 Treibs에[33] 의해 1953년에 처음 설명되었고 1960년에 런던에 있는 St John's 피부과 연구소에서 Magnus 등이 완성했다.[34]
참고 항목
참조
- ^ "Orphanet: Autosomal erythropoietic protoporphyria". orpha.net. Retrieved 17 April 2019.
- ^ a b Casanova-González, María José; Trapero-Marugán, María; Jones, E. Anthony; Moreno-Otero, Ricardo (2010-09-28). "Liver disease and erythropoietic protoporphyria: a concise review". World Journal of Gastroenterology. 16 (36): 4526–4531. doi:10.3748/wjg.v16.i36.4526. ISSN 2219-2840. PMC 2945483. PMID 20857522.
- ^ Seager, M. J.; Whatley, S. D.; Anstey, A. V.; Millard, T. P. (2014). "X-linked dominant protoporphyria: A new porphyria". Clinical and Experimental Dermatology. 39 (1): 35–7. doi:10.1111/ced.12202. PMID 24131146. S2CID 1971165.
- ^ Wensink, D.; Langendonk, J. G.; Overbey, J. R.; Balwani, M.; Van Broekhoven, E. J. E.; Wagenmakers, M. a. E. M.; Wilson, J. H. P.; Wheeden, K.; Naik, H.; Desnick, R. J. (September 2021). "Erythropoietic protoporphyria: time to prodrome, the warning signal to exit sun exposure without pain-a patient-reported outcome efficacy measure". Genetics in Medicine: Official Journal of the American College of Medical Genetics. 23 (9): 1616–1623. doi:10.1038/s41436-021-01176-z. ISSN 1530-0366. PMID 33941881.
- ^ a b c Tsuboi, Hiromi; Yonemoto, Kohzoh; Katsuoka, Kensei (2007-11-01). "Erythropoietic protoporphyria with eye complications". The Journal of Dermatology. 34 (11): 790–794. doi:10.1111/j.1346-8138.2007.00386.x. ISSN 0385-2407. PMID 17973823. S2CID 23093030.
- ^ Poh-Fitzpatrick, M. B. (1986-06-01). "Molecular and cellular mechanisms of porphyrin photosensitization". Photo-Dermatology. 3 (3): 148–157. ISSN 0108-9684. PMID 3529055.
- ^ Bonkovsky, Herbert L.; Rudnick, Sean R. (December 2020). "Erythropoietic Protoporphyria and X-Linked Protoporphyria - Hormonal and Metabolic Disorders". Merck Manuals Consumer Version. Merck Sharp & Dohme Corp. Retrieved 11 January 2021.
- ^ Spelt, JM; De Rooij, FW; Wilson, JH; Zandbergen, AA (2010). "Vitamin D deficiency in patients with erythropoietic protoporphyria". Journal of Inherited Metabolic Disease. 33 Suppl 3: S1–4. doi:10.1007/s10545-008-1037-0. PMID 24137761. S2CID 22847583.
- ^ "Erythropoietic Protoporphyria (EPP) and X-Linked Protoporphyria (XLP)". American Porphyria Foundation. Retrieved 2022-01-26.
- ^ Wahlin, S.; Marschall, H.-U.; Fischler, B. (2013). "Maternal and fetal outcome in Swedish women with erythropoietic protoporphyria". British Journal of Dermatology. 168 (6): 1311–5. doi:10.1111/bjd.12242. PMID 23738640. S2CID 37761662.
- ^ Blagojevic, Daniel; Schenk, Thomas; Haas, Oskar; Zierhofer, Brigitte; Konnaris, Christophoros; Trautinger, Franz (2009). "Acquired erythropoietic protoporphyria". Annals of Hematology. 89 (7): 743–4. doi:10.1007/s00277-009-0859-7. PMID 19902211. S2CID 36170513.
- ^ Kong, Xiao-Fei; Ye, Jing; Gao, De-Yong; Gong, Qi-Ming; Zhang, Dong-Hua; Lu, Zhi-Meng; Lu, Yi-Ming; Zhang, Xin-Xin (2008-02-01). "Identification of a ferrochelatase mutation in a Chinese family with erythropoietic protoporphyria". Journal of Hepatology. 48 (2): 375–379. doi:10.1016/j.jhep.2007.09.013. ISSN 0168-8278. PMID 18160121.
- ^ a b Holme, S. Alexander; Worwood, Mark; Anstey, Alexander V.; Elder, George H.; Badminton, Michael N. (2007-12-01). "Erythropoiesis and iron metabolism in dominant erythropoietic protoporphyria". Blood. 110 (12): 4108–4110. doi:10.1182/blood-2007-04-088120. ISSN 0006-4971. PMID 17804693.
- ^ Magnus, I. A. (February 1968). "Photobiological Aspects of Porphyria". Proceedings of the Royal Society of Medicine. 61 (2): 196–198. doi:10.1177/003591576806100233. PMC 1902233. PMID 5688974.
- ^ a b Lecha, Mario; Puy, Hervé; Deybach, Jean-Charles (2009-01-01). "Erythropoietic protoporphyria". Orphanet Journal of Rare Diseases. 4: 19. doi:10.1186/1750-1172-4-19. ISSN 1750-1172. PMC 2747912. PMID 19744342.
- ^ Bruguera, M.; Herrero, C. (2005-12-01). "[Liver disease in erythropoietic protoporphyria]". Gastroenterología y Hepatología. 28 (10): 632–636. doi:10.1016/s0210-5705(05)71529-6. ISSN 0210-5705. PMID 16373015.
- ^ Anstey, A. V.; Hift, R. J. (2007-07-01). "Liver disease in erythropoietic protoporphyria: insights and implications for management". Gut. 56 (7): 1009–1018. doi:10.1136/gut.2006.097576. ISSN 0017-5749. PMC 1994365. PMID 17360790.
- ^ "Zinc Oxide - Physical UVA+UVB sunscreen/sunblock agent". smartskincare.com. Retrieved 2019-04-02.
- ^ "Sun Protective Clothing". The Skin Cancer Foundation. Retrieved 2022-01-26.
- ^ "Union Register of medicinal products". European Commission. Retrieved 8 December 2020.
- ^ Pirlich, M.; Lochs, H.; Schmidt, H. H. (2001-12-01). "Liver cirrhosis in erythropoietic protoporphyria: improvement of liver function with ursodeoxycholic acid". The American Journal of Gastroenterology. 96 (12): 3468–3469. ISSN 0002-9270. PMID 11774991.
- ^ Paumgartner, Gustav; Beuers, Ulrich (2002-09-01). "Ursodeoxycholic acid in cholestatic liver disease: mechanisms of action and therapeutic use revisited". Hepatology. 36 (3): 525–531. doi:10.1053/jhep.2002.36088. ISSN 0270-9139. PMID 12198643. S2CID 28282761.
- ^ Potter, C.; Tolaymat, N.; Bobo, R.; Sharp, H.; Rank, J.; Bloomer, J. (1996-11-01). "Hematin therapy in children with protoporphyric liver disease". Journal of Pediatric Gastroenterology and Nutrition. 23 (4): 402–407. doi:10.1097/00005176-199611000-00006. ISSN 0277-2116. PMID 8956175.
- ^ Tung, B. Y.; Farrell, F. J.; McCashland, T. M.; Gish, R. G.; Bacon, B. R.; Keeffe, E. B.; Kowdley, K. V. (1999-09-01). "Long-term follow-up after liver transplantation in patients with hepatic iron overload". Liver Transplantation and Surgery. 5 (5): 369–374. doi:10.1002/lt.500050503. ISSN 1074-3022. PMID 10477837.
- ^ McCullough, A. J.; Barron, D.; Mullen, K. D.; Petrelli, M.; Park, M. C.; Mukhtar, H.; Bickers, D. R. (1988-01-01). "Fecal protoporphyrin excretion in erythropoietic protoporphyria: effect of cholestyramine and bile acid feeding". Gastroenterology. 94 (1): 177–181. doi:10.1016/0016-5085(88)90627-0. ISSN 0016-5085. PMID 3335288.
- ^ Gorchein, A.; Foster, G. R. (1999-03-01). "Liver failure in protoporphyria: long-term treatment with oral charcoal". Hepatology. 29 (3): 995–996. doi:10.1002/hep.510290314. ISSN 0270-9139. PMID 10189233.
- ^ Hansson, M.; Hederstedt, L. (1994-02-15). "Purification and characterisation of a water-soluble ferrochelatase from Bacillus subtilis". European Journal of Biochemistry. 220 (1): 201–208. doi:10.1111/j.1432-1033.1994.tb18615.x. ISSN 0014-2956. PMID 8119288.
- ^ Minder, EI; Schneider-Yin, X; Steurer, J; Bachmann, LM (2009). "A systematic review of treatment options for dermal photosensitivity in erythropoietic protoporphyria". Cellular and Molecular Biology. 55 (1): 84–97. PMID 19268006.
- ^ Arceci, Robert.; Hann, Ian M.; Smith, Owen P. (2006). Pediatric hematolog. Malden, Mass.: Blackwell Pub. ISBN 978-1-4051-3400-2.[페이지 필요]
- ^ Elder, George; Harper, Pauline; Badminton, Michael; Sandberg, Sverre; Deybach, Jean-Charles (2012). "The incidence of inherited porphyrias in Europe". Journal of Inherited Metabolic Disease. 36 (5): 849–57. doi:10.1007/s10545-012-9544-4. PMID 23114748. S2CID 20442163.
- ^ Michaels, BD; Del Rosso, JQ; Mobini, N; Michaels, JR (2010). "Erythropoietic protoporphyria: A case report and literature review". The Journal of Clinical and Aesthetic Dermatology. 3 (7): 44–8. PMC 2921755. PMID 20725556.
- ^ Wahlin, S.; Floderus, Y.; Stål, P.; Harper, P. (2011). "Erythropoietic protoporphyria in Sweden: Demographic, clinical, biochemical and genetic characteristics". Journal of Internal Medicine. 269 (3): 278–88. doi:10.1111/j.1365-2796.2010.02236.x. PMID 20412370.
- ^ Kosenow, W; Treibs, A (1953). "Light hypersensitivity and porphyrinemia". Zeitschrift für Kinderheilkunde. 73 (1): 82–92. doi:10.1007/BF00438257. PMID 13103364. S2CID 46459771.
- ^ Magnus, I; Jarrett, A; Prankerd, TA; Rimington, C (1961). "Erythropoietic protoporphyria. A new porphyria syndrome with solar urticaria due to protoporphyrinæmia". The Lancet. 278 (7200): 448–51. doi:10.1016/S0140-6736(61)92427-8. PMID 13765301.