경화(화학)
Curing (chemistry)경화는 폴리머 화학 및 프로세스 엔지니어링에서 사용되는 화학 공정으로 폴리머 사슬의 가교로 폴리머 재료의 강화 또는 경화를 생성합니다.열경화성 폴리머의 제조와 강하게 관련지어져 있어도, 「경화」라는 [1]용어는, 예를 들면, PVC 플라스티졸등의 액체로부터 고체 제품을 얻는 모든 공정에서 사용할 수 있다.
양생 공정
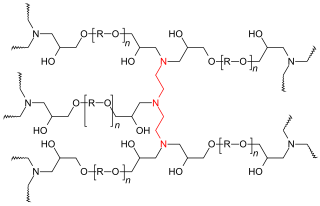
경화공정에서는 경화제를 혼입 또는 혼입하지 않은 단일 모노머와 올리고머가 반응하여 3차원 고분자 네트워크를 [2]형성한다.
다양한 구조를 가진 분자의 반응의 첫 번째 부분에서 분자의 분지가 형성되며, 그 분자량은 반응의 범위에 따라 시간이 지남에 따라 증가하여 네트워크 크기가 시스템의 크기와 같아진다.그 시스템은 용해성을 잃었고 점도는 무한해지는 경향이 있다.나머지 분자는 다른 교차 링크를 생성하는 네트워크와 반응할 때까지 거시적 네트워크와 공존하기 시작합니다.가교밀도는 시스템이 화학반응이 [2]끝날 때까지 증가합니다.
열, 방사선, 전자 빔 또는 화학 첨가물에 의해 경화를 시작할 수 있습니다.IUPAC에서 인용한 내용: "화학 경화제와의 [3]혼합이 필요할 수도 있고 필요하지 않을 수도 있습니다."따라서 (i) 화학첨가물에 의해 유도되는 경화(경화제, 경화제라고도 함)와 (ii)첨가물이 없는 경우의 경화(curing)의 두 가지 종류가 있다.중간 케이스는 경화를 유도하기 위해 외부 자극(빛, 열, 방사선)이 필요한 수지와 첨가제의 혼합물을 포함합니다.
경화 방법은 수지와 용도에 따라 달라집니다.경화에 의해 유발되는 수축에 특히 주의를 기울인다.일반적으로 작은 수축값(2-3%)이 바람직하다.[1]
첨가물에 의한 경화
에폭시 수지는 보통 경화제라고 불리는 첨가제를 사용하여 경화됩니다.폴리아민은 종종 사용된다.아민기가 에폭시드 고리를 연다.
고무에서 경화는 가교제의 첨가에 의해서도 유도된다.그 결과 발생하는 과정을 유황 가황이라고 합니다.황은 분해되어 폴리머 사슬의 단면 사이에 폴리황화물 가교(브릿지)를 형성합니다.가교 정도는 재료의 [5]강성과 내구성 및 기타 특성을 결정합니다.
페인트와 니스에는 일반적으로 오일 건조제가 함유되어 있으며, 보통 금속 비누로 구성되는 불포화 건조 오일의 가교 연계를 촉진합니다.페인트를 "건조"라고 표현하면 실제로는 가교로 경화됩니다.산소 원자는 고무의 가황에서 황이 수행하는 역할과 유사한 가교 역할을 한다.
무첨가 경화
콘크리트의 경우 경화에는 규산염 가교 형성이 수반된다.이 과정은 첨가물에 의해 유도되지 않는다.
많은 경우, 수지는 용액 또는 열활성 촉매와의 혼합물로 제공되며, 가교를 유도하지만 가열 시에만 제공됩니다.예를 들어 일부 아크릴계 수지는 과산화디벤조일로 제조된다.혼합물을 가열하면 과산화물이 유리기로 변환되어 아크릴산염에 추가되어 가교 작용을 시작합니다.
일부 유기 수지는 열로 경화된다.열이 가해짐에 따라 가교 개시 전에 수지의 점도가 저하되고, 그 결과 구성 올리고머가 상호 연결됨에 따라 점도가 높아진다.이 과정은 올리고머 사슬의 3차원 네트워크가 형성될 때까지 계속됩니다. 이 단계를 겔화라고 합니다.수지의 가공성 측면에서 이는 중요한 단계입니다. 젤화 전에는 시스템이 비교적 이동성이 높고, 이동성이 매우 제한적인 후에는 수지와 복합 재료의 미세 구조가 고정되며, 추가적인 경화를 위한 심각한 확산 한계가 생깁니다.따라서 수지의 유리화를 달성하기 위해서는 일반적으로 겔화 후 공정 온도를 높여야 합니다.
자외선에 의해 촉매가 활성화될 때, 그 과정은 UV [6]경화라고 불립니다.
모니터링 방법
예를 들어, 경화 모니터링은 복합 재료의 제조 공정을 제어하기 위한 필수 구성요소입니다.공정의 마지막에 액체가 되는 물질은 고체입니다.점도는 공정 중에 변화하는 가장 중요한 특성입니다.
치료 모니터링은 다양한 물리적 또는 화학적 특성을 모니터링하는 데 의존합니다.
레올로지 분석
경화 공정에서 점도의 변화, 즉 반응의 정도를 감시하는 간단한 방법은 탄성률의 [7]변화를 측정하는 것입니다.
경화 중 시스템의 탄성 계수를 측정하기 위해 레오미터를 [7]사용할 수 있습니다.동적 기계적 분석을 통해 저장 계수(G')와 손실 계수(G')를 측정할 수 있습니다.G'와 G"의 시간 변화는 경화 [7]반응의 정도를 나타낼 수 있다.
그림 4와 같이 "유도 시간"이 지나면 기울기가 급변하면서 G'와 G'가 증가하기 시작한다.특정 지점에서 서로 교차하고, 그 후 G'와 G'의 비율이 감소하며, 모듈리는 고원을 이루는 경향이 있다.그들이 고원에 도달하면 반응은 끝난다.[2]
시스템이 액체 상태일 경우 저장 계수는 매우 낮습니다. 시스템이 액체 상태처럼 작동합니다.그런 다음 반응이 계속되며 시스템은 고체처럼 반응하기 시작합니다. 즉, 저장 계수가 증가합니다.
는 [8]다음과 같이 정의할 수 있습니다.
경화 정도는 0(반응 시작 시)부터 시작하여 1(반응 종료 시)까지 증가합니다.곡선의 기울기는 시간에 따라 변하며 반응의 절반 정도에서 최대값을 갖는다.
열분석
가교 중에 발생하는 반응이 발열성일 경우 가교 속도는 공정 중에 방출되는 열과 관련될 수 있다.생성되는 결합의 수가 많을수록 반응에서 방출되는 열도 커집니다.반응이 끝나면 열이 더 이상 방출되지 않습니다.열류 측정을 위해 차동 스캔 열량 측정을 [9]사용할 수 있습니다.
가교 중에 형성된 각 결합이 동일한 양의 에너지를 방출한다고 가정할 때 경화도 {\는 [9]다음과 같이 정의할 수 있습니다.
서Q(\ Q는 특정 까지 방출되는 열 {는 순간 열 비율, T는 반응이 [9]종료될 때(\에서 방출되는 총 열량입니다.
또한 이 경우 경화도는 0(결합이 생성되지 않음)에서 1(반응이 더 이상 발생하지 않음)로 시간이 변화하고 [9]반응의 절반 정도로 최대값이 됩니다.
유전율 분석
종래의 유전율 측정은, 통상적으로 유전체 센서(용량 프로브)의 병렬판 구성으로 행해지며, 액체로부터 고무, 고체 상태에 이르는 전 사이클에 걸쳐 수지 경화를 감시할 수 있다.복잡한 수지 혼합 경화에서 섬유 성능 내에서 위상 분리를 모니터링할 수 있습니다.동일한 속성은 유전체 기술의 최신 개발, 즉 마이크로 유전체 측정에도 속합니다.
여러 버전의 유전체 센서가 시판되고 있습니다.치료 모니터링 애플리케이션에 사용하기에 가장 적합한 형식은 표면에 감지 그리드가 있는 평평한 디지털 간 용량 구조입니다.설계(특히 내구성 있는 기판)에 따라 어느 정도 재사용성이 있는 반면, 플렉시블 기판 센서는 대부분의 수지 시스템에서 내장형 센서로 사용할 수 있습니다.
분광 분석
경화 프로세스는 다양한 파라미터의 변화를 측정하여 모니터링할 수 있습니다.
- FTIR 및 Raman과 같은 스펙트럼 분석 방법을 사용한 특정 반응성 수지종의 농도.
- 수지의 굴절률 또는 형광(굴절 특성)
- 파이버 브래그 그레이팅(FBG) 센서를 사용하여 내부 수지 변형률(기계적 특성).
초음파 분석
초음파 치료 모니터링 방법은 다음을 측정하여 전파 초음파의 특성 변화와 구성 요소의 실시간 기계적 특성 간의 관계를 기반으로 합니다.
- 초음파 비행 시간(통과 및 펄스 감지 모드 모두)
- 충격 들뜸과 레이저 유도 표면 음파 속도 측정을 이용한 고유 주파수.
「 」를 참조해 주세요.
레퍼런스
- ^ a b Pham, Ha Q.; Marks, Maurice J. (2012). "Epoxy Resins". Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002/14356007.a09_547.pub2.
- ^ a b c Chambon, Francois; Winter, H. Henning (November 1987). "Linear Viscoelasticity at the Gel Point of a Crosslinking PDMS with Imbalanced Stoichiometry". Journal of Rheology. 31 (8): 683–697. doi:10.1122/1.549955.
- ^ "curing". IUPAC Goldbook.
- ^ Ulrich Poth (2002). "Drying Oils and Related Products". Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002/14356007.a09_055.
{{cite encyclopedia}}: CS1 maint: 작성자 파라미터 사용(링크) - ^ James E. Mark, Burak Erman (eds.) (2005). Science and technology of rubber. p. 768. ISBN 978-0-12-464786-2.
{{cite book}}:author=범용명(도움말)이 있습니다. - ^ 그레고리 T. 캐롤, 니콜라스 J.Turro and Jeffrey T. Koberstein (2010) 콜로이드 및 인터페이스 과학 저널, Vol. 351, 페이지 556-560 doi:10.1016/j.jcis.2010.070에 의한 박형 고분자 필름의 패턴닝 듀팅.
- ^ a b c Macosko, Christopher W. (1994). Rheology : principles, measurements, and applications. VCH. p. 568. ISBN 978-0-471-18575-8.
- ^ a b Harkous, Ali; Colomines, Gaël; Leroy, Eric; Mousseau, Pierre; Deterre, Rémi (April 2016). "The kinetic behavior of Liquid Silicone Rubber: A comparison between thermal and rheological approaches based on gel point determination". Reactive and Functional Polymers. 101: 20–27. doi:10.1016/j.reactfunctpolym.2016.01.020.
- ^ a b c d e Hong, In-Kwon; Lee, Sangmook (January 2013). "Cure kinetics and modeling the reaction of silicone rubber". Journal of Industrial and Engineering Chemistry. 19 (1): 42–47. doi:10.1016/j.jiec.2012.05.006.
- Osswald, Tim A.; Menges, Georg (2003). Materials science of polymers for engineers. Hanser Verlag. pp. 334–335. ISBN 978-1-56990-348-3.
- Glöckner, Patrick (2009). Radiation Curing. Vincentz Network. pp. 11–16. ISBN 978-3-86630-907-4.
- I. Partridge와 G.Maistros, '공정 제어를 위한 유전체 경화 모니터링', 17장, 제5권, 복합재료 백과사전(2001), 엘세비어 사이언스, 런던, 413페이지
- P.Ciriscioli와 G.Springer, 'Smart Autoclave curse in Composite', (1991), Technomic Publishing, Lancaster, PA.







 특정
특정  순간 열 비율,
순간 열 비율,  반응이
반응이 


