셔틀 촉매
Shuttle catalysis셔틀 촉매는 공여 분자의 화학적 실체가 수용체 [1]분자로 전달되는 촉매 반응을 설명하는 데 사용됩니다.이러한 반응에서, 각 반응물의 화학 결합의 수는 변하지만, 화학 결합의 유형과 총 수는 반응 과정에서 일정하게 유지됩니다.발열로 인해 실질적으로 되돌릴 수 없는 많은 유기 반응과 달리 셔틀 촉매 하에서 작동하는 반응은 종종 [2]가역적입니다.그러나 평형의 위치는 르 샤틀리에의 원리를 통해 제품 쪽으로 움직일 수 있습니다.이러한 평형 이동의 원동력은 일반적으로 가스/침전의 형성, 높은 기저 상태 에너지 반응물의 사용 또는 안정화된 생성물의 형성 또는 반응물의 [3]과잉 등가물입니다.
셔틀 엔티티의 재배치는 종종 관심 화합물을 기능화하거나 기능을 해제하는 역할을 하는 전이 금속 촉매에 의해 매개됩니다.이 프로세스의 장점은 독성이 있거나 반응성이 있는 원시 화학 물질을 처리하는 프로세스를 제외한다는 것입니다.그러나 이러한 반응은 일련의 기본 단계를 통해 온화한 조건에서 반응물 사이에 셔틀된 실체를 효율적으로 전달할 수 있는 촉매 시스템의 개발을 필요로 합니다.
적용들
전이 수소화
전이 수소화는 위험한 가압2 [4]H를 필요로 하지 않고 다양한 기능 그룹을 줄이기 위해 광범위하게 연구되었습니다.
전달 가수 분해
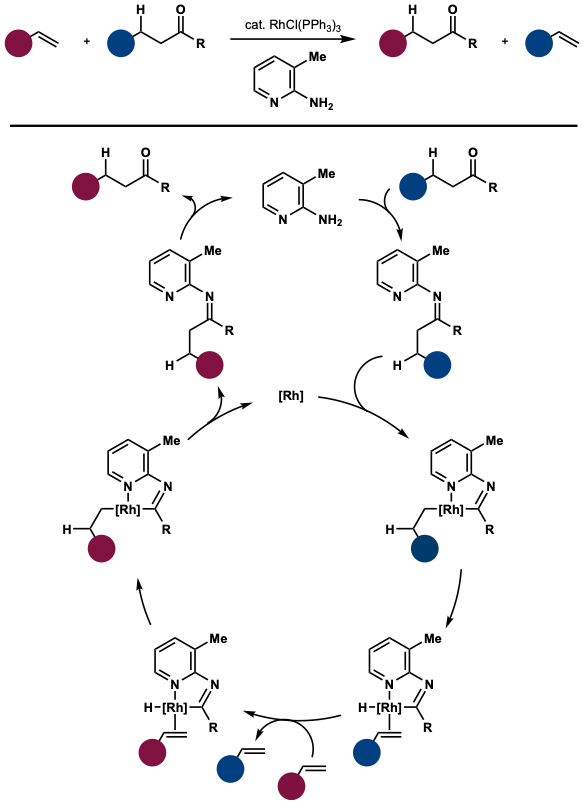
1999년, 전철호와 이혁은 셔틀 [5]촉매를 통한 하이드로아실화의 첫 번째 사례를 보고했습니다.이 예에서 3-메틸-2-아미노피리딘은 아실기를 활성화하고 로듐 촉매에 배위하여 C-C 결합 분열을 촉진하여 결국 케톤에서 알켄으로의 알데히드 이동을 가능하게 했습니다.이 반응의 원동력은 알켄의 과잉 존재와 휘발성 에틸렌의 안정적인 스티렌/추출물 형성입니다.이 방법은 전통적인 하이드로아실화 과정에서 아세트알데히드와 같은 독성 및 자체 반응성 알데히드를 사용할 필요가 없습니다.
전달 하이드로포름화
하이드로포밀화는 고전적인 전이 금속 촉매 반응이며 산업 환경에서 널리 사용되어 왔습니다.그러나 이 반응의 단점은 H/CO의2 위험한 혼합물이 필요하다는 것입니다.이러한 이유로 H/CO 가스를 비위험 알데히드로 대체하는2 프로세스가 모색되고 있습니다.
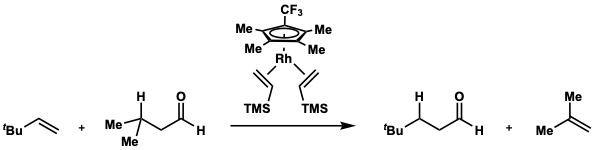
1999년, 크리스찬 P.Lenges와 Maurice Brookhart는 로듐([6][7]I) 촉매를 사용하여 3,3-디메틸-1-부텐으로의 H/CO 전달에 적합한2 대용물로 isovaleraldehyde를 보고했습니다.
이 과정의 역방향은 2015년 Vy M. Dong과 동료들에 의해 촉매제로 만들어졌습니다.[8][9]그들은 상응하는 알켄을 얻기 위해 알데히드에 대해 탈수로포르밀화를 수행했습니다.이러한 변환을 위해, 그들은 노르보르넨 또는2 노르보르나디엔을 H/CO 수용체로 사용하여 변형률 방출을 통한 반응성을 촉진했습니다.
전이 수소화 수소화
독성이 있는 하이드로시아니드(HCN) 가스 또는 아세톤시아노히드린과 같은 대용물의 사용을 대체하기 위해, Bill Morandi와 동료들은 셔틀 [10]촉매를 사용하는 하이드로시아니네이션 전략을 개발했습니다.이 예에서, 그들은 다양한 알켄의 하이드로시아네이트 반응을 제공하기 위해 니켈/알루미늄 공동 촉매 조건 하에서 아이소발레로니트릴을 HCN 대용물로 사용합니다.이소발레로니트릴을 사용하면 HCN 농도를 신중하게 제어할 수 있으며 휘발성 이소부틸렌의 형성이 반응의 원동력이 됩니다.
다른이들
아렌,[11] CO/HCl,[12] HMgBr,[13] HZn2,[14] HO2,[15] 카벤,[16] 실릴렌,[17] 설페늄을[18] 포함한 다른 화학 물질도 이 촉매 플랫폼에 따라 폐쇄되었습니다.
레퍼런스
- ^ Bhawal, Benjamin N.; Morandi, Bill (2017). "Shuttle Catalysis—New Strategies in Organic Synthesis". Chemistry – A European Journal. 23 (50): 12004–12013. doi:10.1002/chem.201605325. ISSN 1521-3765. PMID 28125163.
- ^ Bhawal, Benjamin N.; Morandi, Bill (2016-11-04). "Catalytic Transfer Functionalization through Shuttle Catalysis". ACS Catalysis. 6 (11): 7528–7535. doi:10.1021/acscatal.6b02333.
- ^ Bhawal, Benjamin N.; Morandi, Bill (2019). "Catalytic Isofunctional Reactions—Expanding the Repertoire of Shuttle and Metathesis Reactions". Angewandte Chemie International Edition. 58 (30): 10074–10103. doi:10.1002/anie.201803797. hdl:20.500.11850/320484. ISSN 1521-3773. PMID 30192427. S2CID 52169579.
- ^ Shimizu, Hideo; Nagasaki, Izuru; Matsumura, Kazuhiko; Sayo, Noboru; Saito, Takao (2007-12-01). "Developments in Asymmetric Hydrogenation from an Industrial Perspective". Accounts of Chemical Research. 40 (12): 1385–1393. doi:10.1021/ar700101x. ISSN 0001-4842. PMID 17685581.
- ^ Jun, Chul-Ho; Lee, Hyuk (1999-02-01). "Catalytic Carbon−Carbon Bond Activation of Unstrained Ketone by Soluble Transition-Metal Complex". Journal of the American Chemical Society. 121 (4): 880–881. doi:10.1021/ja983197s. ISSN 0002-7863.
- ^ Lenges, Christian P.; Brookhart, Maurice (1999). "Isomerization of Aldehydes Catalyzed by Rhodium(I) Olefin Complexes". Angewandte Chemie International Edition. 38 (23): 3533–3537. doi:10.1002/(SICI)1521-3773(19991203)38:23<3533::AID-ANIE3533>3.0.CO;2-E. ISSN 1521-3773. PMID 10602233.
- ^ Lenges, Christian P.; Brookhart, Maurice (1999). "Durch Rhodium(I)-Olefinkomplexe katalysierte Isomerisierung von Aldehyden". Angewandte Chemie (in German). 111 (23): 3746–3750. doi:10.1002/(SICI)1521-3757(19991203)111:23<3746::AID-ANGE3746>3.0.CO;2-B. ISSN 1521-3757.
- ^ "The Dong Research Group - About Professor Vy M. Dong". www.chem.uci.edu. Retrieved 2021-06-12.
- ^ Murphy, Stephen K.; Park, Jung-Woo; Cruz, Faben A.; Dong, Vy M. (2015-01-02). "Rh-catalyzed C–C bond cleavage by transfer hydroformylation". Science. 347 (6217): 56–60. doi:10.1126/science.1261232. ISSN 0036-8075. PMC 4445961. PMID 25554782.
- ^ Fang, Xianjie; Yu, Peng; Morandi, Bill (2016-02-19). "Catalytic reversible alkene-nitrile interconversion through controllable transfer hydrocyanation". Science. 351 (6275): 832–836. doi:10.1126/science.aae0427. ISSN 0036-8075. PMID 26912891. S2CID 29949044.
- ^ Lutz, Marius D. R.; Gasser, Valentina C. M.; Morandi, Bill (2021-04-08). "Shuttle arylation by Rh(I) catalyzed reversible carbon–carbon bond activation of unstrained alcohols". Chem. 7 (4): 1108–1119. doi:10.1016/j.chempr.2021.02.029. ISSN 2451-9294.
- ^ Fang, Xianjie; Cacherat, Bastien; Morandi, Bill (2017-11-05). "CO- and HCl-free synthesis of acid chlorides from unsaturated hydrocarbons via shuttle catalysis". Nature Chemistry. 9 (11): 1105–1109. doi:10.1038/nchem.2798. ISSN 1755-4349. PMID 29064496.
- ^ Bhawal, Benjamin N.; Morandi, Bill (2019). "Catalytic Isofunctional Reactions—Expanding the Repertoire of Shuttle and Metathesis Reactions". Angewandte Chemie International Edition. 58 (30): 10074–10103. doi:10.1002/anie.201803797. hdl:20.500.11850/320484. ISSN 1521-3773. PMID 30192427. S2CID 52169579.
- ^ Vettel, Stephan; Vaupel, Andrea; Knochel, Paul (1996-01-01). "Nickel-Catalyzed Preparations of Functionalized Organozincs". The Journal of Organic Chemistry. 61 (21): 7473–7481. doi:10.1021/jo960808v. ISSN 0022-3263. PMID 11667677.
- ^ Maffioli, Sonia I.; Marzorati, Ettore; Marazzi, Alessandra (2005-11-01). "Mild and Reversible Dehydration of Primary Amides with PdCl2 in Aqueous Acetonitrile". Organic Letters. 7 (23): 5237–5239. doi:10.1021/ol052100l. ISSN 1523-7060. PMID 16268547.
- ^ Gassman, Paul G.; Johnson, Thomas H. (1976-09-01). "Cyclopropane-olefin cross metathesis". Journal of the American Chemical Society. 98 (19): 6058–6059. doi:10.1021/ja00435a058. ISSN 0002-7863.
- ^ Ćiraković, Jelena; Driver, Tom G.; Woerpel, K. A. (2002-08-01). "Metal-Catalyzed Silacyclopropanation of Mono- and Disubstituted Alkenes". Journal of the American Chemical Society. 124 (32): 9370–9371. doi:10.1021/ja020566i. ISSN 0002-7863. PMID 12167021.
- ^ Adam, Waldemar; Bargon, Rainer M.; Schenk, Wolfdieter A. (2003-04-01). "Direct Episulfidation of Alkenes and Allenes with Elemental Sulfur and Thiiranes as Sulfur Sources, Catalyzed by Molybdenum Oxo Complexes". Journal of the American Chemical Society. 125 (13): 3871–3876. doi:10.1021/ja029292p. ISSN 0002-7863. PMID 12656621.