DNA 복제 응력
DNA replication stressDNA 복제 스트레스는 유전자가 다양한 스트레스에 노출되는 세포의 상태를 말한다.복제 스트레스에 기여하는 이벤트는 DNA 복제 중에 발생하며 복제 포크가 중단될 수 있다.[1]
복제 스트레스에 기여하는 이벤트는 다음과 같은 경우가 많다.[2]
- 리보뉴클레오타이드의 미분포
- 특이한 DNA 구조
- 복제와 전사 간의 충돌
- 필수 복제 요소의 부족
- 흔하게 연약한 장소
- 과다압박 또는 온코겐의 구성활성화
- 크로마틴의 접근 불가능
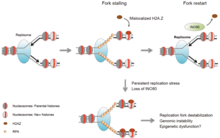
ATM과 ATR은 복제 스트레스를 완화하는데 도움을 주는 단백질이다.[3]구체적으로 DNA 손상에 의해 모집되고 활성화되는 키나제들이다.[1][2]이러한 규제 단백질이 이를 안정화시키지 못하면 정체된 복제 포크가 붕괴될 수 있다.[4]이 경우 손상된 DNA 끝을 수리하기 위해 포크의 재조립이 시작된다.[4]
복제 포크
복제 포크는 DNA 복제 활동에 영향을 미치는 단백질 그룹으로 구성된다.복제 포크가 멈추려면 셀이 일정 수의 정지된 포크와 구속 길이를 가져야 한다.서로 연결된 헬리코아제와 폴리머아제 활성의 Stlacking 때문에 복제포크가 특별히 일시 중지된다.이러한 상황에서는 포크 보호 단지(FPC)를 모집하여 이러한 연계를 유지하도록 돕는다.[5]
포크의 구조를 정지하고 유지하는 것 외에도 단백질 인산화 작용은 복제 재시동을 위한 신호 캐스케이드를 생성할 수 있다.FPC의 일부인 Mrc1 단백질은 캐스케이드 전체에 걸쳐 키나아제와 상호 작용하여 체크포인트 신호를 전송한다.(복제 스트레스로 인해) 이러한 키나아스가 손실되면 ssDNA가 초과 생성되는데, 이는 복제를 다시 시작하는 데 필요하다.[6]
복제 블록 제거
DNA 연동 ICL(Interstrand cross-links)은 복제 포크 진행을 차단하여 복제 스트레스를 유발한다.이 막힘은 DNA 가닥 분리의 실패와 복제 포크의 정체로 이어진다.ICL의 수리는 순차 절개 및 동음이의 재조합을 통해 수행할 수 있다.척추동물 세포에서 ICL 함유 크로마틴 템플릿의 복제는 90개 이상의 DNA 수리 및 게놈 유지 요인의 모집을 유발한다.[7]정체된 복제 포크에 모집된 단백질을 분석한 결과 복제 응력 반응에 관련된 특정 DNA 수리 인자의 집합이 밝혀졌다.[7]이들 단백질 중 SLF1과 SLF2는 SMC5/6 DNA 수리 단백질 복합체를 RAD18과 물리적으로 연계하는 것으로 밝혀졌다.SMC5/6 단지는 균질 재조합에 채용되며, RAD18과의 연계를 통해 DNA 손상 현장의 보편화 제품에 SMC5/6를 채용할 수 있을 것으로 보인다.
복제 결합 복구
복제 포크 진행을 유지하기 위해 손상된 DNA를 환지체와 협조하여 처리하는 메커니즘은 복제 결합 수리의 예로 간주된다.위에서 제시한 DNA간 상호연결을 보수하는 것 외에 중복된 층으로 운영되는 복수의 DNA 수리 공정을 손상 특성 및 위치에 따라 결함 현장에 모집할 수 있다.이러한 수리 프로세스에는 (1) 잘못 조립된 베이스 제거, (2) 잘못 조립된 리보핵화물의 제거, (3) 복제 중합효소를 차단하는 손상된 베이스(예: 산화 또는 메틸화 베이스), (4) DNA-단백질 교차 링크 제거, (5) 이중 스트랜드 및 파손의 제거가 포함된다.[8]이러한 복구 경로는 정지된 복제 포크 성능 저하를 방지하고 손상된 포크를 다시 시작할 수 있도록 기능할 수 있지만, 부족한 경우 복제 스트레스를 유발할 수 있다.
인과
복제 스트레스는 게놈에 정기적으로 도입되는 다양한 내생적 스트레스와 외생적 스트레스로부터 유도된다.[9]이러한 스트레스에는 DNA 손상, 염색질의 과도한 압축(재식 접근 방지), 온코겐의 과잉 표현 [10]또는 복제하기 어려운 게놈 구조가 포함되지만 이에 국한되지는 않는다.[1][2]복제 스트레스는 게놈 불안정, 암, 노화로 이어질 수 있다.[11][12]조정되지 않은 복제-전송 충돌과 계획되지 않은 R-루프 축적이 중요한 기여 요인이다.[13]
특정 이벤트
게놈 불안정을 초래하는 사건은 유사 이전의 세포 주기, 특히 S 단계에서 발생한다.이 단계에 대한 교란은 다가오는 유사분열 단계에 대해 부정확한 염색체 분리와 같은 부정적인 영향을 발생시킬 수 있다.[9]S상 손상의 원인이 되는 두 가지 과정은 종양 억제기 활성화와 불활성화다.이들 둘은 모두 G1 단계에서 S 단계로 이행하는 속도를 높여 DNA 복제 성분의 양이 불충분하게 되는 것으로 나타났다.이러한 손실은 DNA 손상 대응(DDR)에 기여할 수 있다.복제 스트레스는 발암에 대한 지표적인 특성이 될 수 있는데, 발암에는 일반적으로 DNA 수리 시스템이 결여되어 있다.[14][15]G1 단계의 생리학적으로 짧은 기간 또한 초기 배아 발달 동안 빠르게 복제되는 조제자들의 전형이다.[16]
암의 응용
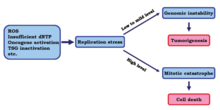
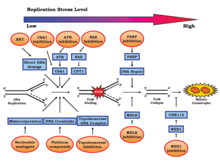
정상복제 스트레스는 낮은 수준에서 약한 수준으로 발생하며 유전적 불안정성을 유도하여 종양과 암의 진행을 유발할 수 있다.[17]그러나 높은 수준의 복제 스트레스는 암세포를 죽이는 것으로 나타났다.
한 연구에서, 연구원들은 높은 수준의 복제 스트레스를 암세포에 유발하는 영향을 알아내기 위해 노력했다.결과는 체크포인트의 추가 손실로 복제 스트레스가 더 높은 수준으로 증가한다는 것을 보여주었다.이러한 변화로 인해, 암세포의 DNA 복제가 미완성되거나 미완성 단계에 접어들 때 부정확할 수 있으며, 이는 결국 미완성 대재앙을 통해 세포사멸을 초래할 수 있다.[14]
또 다른 연구는 복제 스트레스가 APOBEC3B 활동에 어떤 영향을 미치는지 조사했다.APOBEC3(아폴리포프로테아닌BmRNA 편집효소, 촉매 폴리펩타이드 유사 3)는 암 게놈을 다양한 암 형태로 돌연변이를 일으키는 것으로 관찰됐다.이 연구의 결과는 인공신호 신호의 약화나 DNA 복제 스트레스 강화가 발암 가능성을 변화시킬 수 있고, 치료적으로 조작될 수 있다는 것을 보여준다.[18]
참조
- ^ a b c Mazouzi A, Velimezi G, Loizou JI (November 2014). "DNA replication stress: causes, resolution and disease". Experimental Cell Research. 329 (1): 85–93. doi:10.1016/j.yexcr.2014.09.030. PMID 25281304.
- ^ a b c Zeman MK, Cimprich KA (January 2014). "Causes and consequences of replication stress". Nature Cell Biology. 16 (1): 2–9. doi:10.1038/ncb2897. PMC 4354890. PMID 24366029.
- ^ "Reactome Activation of ATR in response to replication stress". www.reactome.org. Retrieved 2017-04-09.
- ^ a b Allen C, Ashley AK, Hromas R, Nickoloff JA (February 2011). "More forks on the road to replication stress recovery". Journal of Molecular Cell Biology. 3 (1): 4–12. doi:10.1093/jmcb/mjq049. PMC 3030971. PMID 21278446.
- ^ "Replication Fork, Fork Protection Complex Learn Science at Scitable". www.nature.com. Retrieved 2017-04-09.
- ^ "Stalled DNA Replication Fork Learn Science at Scitable". www.nature.com. Retrieved 2017-04-09.
- ^ a b Räschle M, Smeenk G, Hansen RK, Temu T, Oka Y, Hein MY, et al. (May 2015). "DNA repair. Proteomics reveals dynamic assembly of repair complexes during bypass of DNA cross-links". Science. 348 (6234): 1253671. doi:10.1126/science.1253671. PMC 5331883. PMID 25931565.
- ^ Cortez D (June 2019). "Replication-Coupled DNA Repair". Molecular Cell. 74 (5): 866–876. doi:10.1016/j.molcel.2019.04.027. PMC 6557297. PMID 31173722.
- ^ a b "Replication Stress in Mammalian Cells and Its Consequences for Mitosis (PDF Download Available)". ResearchGate. Retrieved 2017-02-11.
- ^ King, David; Li, Xiao Dun; Almeida, Gilberto S.; Kwok, Colin; Gravells, Polly; Harrison, Daniel; Burke, Saoirse; Hallsworth, Albert; Jamin, Yann; George, Sally; Robinson, Simon P.; Lord, Christopher J.; Poon, Evon; Yeomanson, Daniel; Chesler, Louis; Bryant, Helen E. (24 September 2019). "MYCN expression induces replication stress and sensitivity to PARP inhibition in neuroblastoma". Oncotarget. 11 (23): 2141–2159. doi:10.18632/oncotarget.27329. PMC 7289530. PMID 32577161.
- ^ Burhans WC, Weinberger M (2007). "DNA replication stress, genome instability and aging". Nucleic Acids Research. 35 (22): 7545–56. doi:10.1093/NAR/GKM1059. PMC 2190710. PMID 18055498.
- ^ Fragkos M, Naim V (April 2017). "Rescue from replication stress during mitosis". Cell Cycle. 16 (7): 613–633. doi:10.1080/15384101.2017.1288322. PMC 5397263. PMID 28166452.
- ^ Brambati A, Colosio A, Zardoni L, Galanti L, Liberi G (2015-04-28). "Replication and transcription on a collision course: eukaryotic regulation mechanisms and implications for DNA stability". Frontiers in Genetics. 6: 166. doi:10.3389/fgene.2015.00166. PMC 4412130. PMID 25972894.
- ^ a b Zhang J, Dai Q, Park D, Deng X (August 2016). "Targeting DNA Replication Stress for Cancer Therapy". Genes. 7 (8): 51. doi:10.3390/genes7080051. PMC 4999839. PMID 27548226.
- ^ Cescon DW, Haibe-Kains B (September 2016). "DNA replication stress: a source of APOBEC3B expression in breast cancer". Genome Biology. 17 (1): 202. doi:10.1186/s13059-016-1069-y. PMC 5045630. PMID 27716362.
- ^ Wei JY, Bulkley BH, Schaeffer AH, Greene HL, Reid PR (July 1978). "Mitral-valve prolapse syndrome and recurrent ventricular tachyarrhythmias: a malignant variant refractory to conventional drug therapy". Annals of Internal Medicine. 89 (1): 6–9. doi:10.1523/JNEUROSCI.15-09-06046.1995. PMC 6577667. PMID 666188.
- ^ Taylor EM, Lindsay HD (January 2016). "DNA replication stress and cancer: cause or cure?" (PDF). Future Oncology. 12 (2): 221–37. doi:10.2217/fon.15.292. PMID 26616915. S2CID 20261656.
- ^ Kanu N, Cerone MA, Goh G, Zalmas LP, Bartkova J, Dietzen M, et al. (September 2016). "DNA replication stress mediates APOBEC3 family mutagenesis in breast cancer". Genome Biology. 17 (1): 185. doi:10.1186/s13059-016-1042-9. PMC 5025597. PMID 27634334.