알프레드 베르너
Alfred Werner알프레드 베르너(Alfred Werner, 1866년 12월 12일 ~ 1919년 11월 15일)는 스위스의 화학자로 ETH 취리히의 학생이자 취리히 대학의 교수였다. 그는 전환 금속 복합체의 팔면 구성을 제안하여 1913년 노벨 화학상을 수상하였다. 베르너는 현대 조정 화학의 기초를 닦았다. 그는 노벨상을 수상한 최초의 무기 화학자였고 1973년 이전에는 유일한 화학자였다.[1]
전기
베르너는 1866년 알자스의 멀하우스(당시 프랑스의 일부였으나 1871년 독일에 합병되었다)에서 태어났다. 그는 로마 가톨릭 신자로 자랐다.[2] 그는 파운드리 노동자 장아담 베르너와 그의 두 번째 부인 살로메 지네트 베르너의 넷째이자 마지막 아이로 부유한 가정에서 태어났다.[2] 그는 취리히에 있는 스위스연방연구소(Polytechnikum)에서 화학을 공부하기 위해 스위스로 갔으나 1909년까지 이 연구소가 박사학위를 부여할 권한이 없었기 때문에 베르너는 1890년 취리히 대학에서 정식으로 박사학위를 받았다.[2] 파리에서 박사 후 연구를 마치고 스위스연방연구소로 돌아와 가르쳤다(1892년). 1893년 취리히 대학으로 옮겨가 1895년 교수가 되었다. 1894년에 그는 스위스 시민이 되었다.[2]
작년에는 일반적이고 진보적이며 퇴행성 동맥경화증을 앓고 있었는데, 특히 뇌는 수년간 과음과 과로로 악화되었다. 그는 취리히의 한 정신병원에서 사망했다.[2]
리서치
조정화학
1893년 베르너는 중앙 전이 금속 원자가 중성 또는 음이온 리간드로 둘러싸인 복잡한 이온을 포함한 조정 화합물에 대한 정확한 구조를 최초로 제안했다.
예를 들어 코발트는 CoCl3•6NH라는3 공식을 가지고 "복잡한" 헥사민코발트(III) 염화물을 형성한다고 알려져 있었지만, 점이 나타내는 연관성의 성질은 신비스러웠다. 베르너는 8면체의 정점에 있는3+ 6개의3 NH로 둘러싸인 코이온을 가진 [Co(NH3)]6Cl3 구조를 제안했다. 3Cl은− 자유이온으로 분리되는데, 베르너가 수용액에서 화합물의 전도도를 측정하고, 또한 질산은을 이용한 강수를 이용한 염화 음이온 분석으로 확인하였다. 후에 자기 감수성 분석은 CoCl3•6NH의3 화학적 성질에 대한 베르너의 제안을 확인하는 데도 사용되었다.
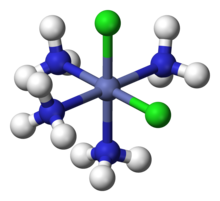
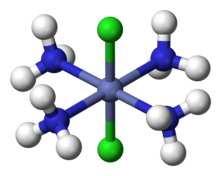
두 종류 이상의 리간드를 가진 단지의 경우 베르너는 관찰된 등소체의 수를 설명하는 데 성공했다. 예를 들어, 그는 두 개의 테트램민 이소머인 "Co(NH3)4Cl3"과 한 개의 녹색과 한 개의 보라색의 존재를 설명했다. Werner는 이 두 가지가 [Co(NH3)4Cl2]Cl의 기하학적 등사체라고 제안했으며, 하나의 Cl− 이온은 전도도 측정에 의해 확인된 것처럼 분리되었다. Co 원자는 8면체의 정점에 있는 4개의3 NH와 2개의 Cl 리간드로 둘러싸여 있다. 녹색 이소머는 정점 반대편에 있는 두 개의 클 리간드와 "트랜스"이고, 보라색은 인접한 정점에 있는 두 개의 클과 "시스"이다.
베르너는 광학 이소머로 콤플렉스도 준비했으며, 1914년 헥솔로 알려진 탄소가 부족한 합성 치랄 화합물로는 최초로 [Co(NH3)(4OH)]23Br을6 보고했다.
용기의 성질
베르너 이전에 화학자들은 원소의 용맹을 다른 종류의 결합을 구분하지 않고 그 결합의 수로 정의했다. 그러나, [Co(NH3)]6Cl과3 같은 콤플렉스에서 베르너는 Co-Cl 채권이 장거리에서는 "기본" 3에 해당하고, Co-NH3 채권은 "2차"에 해당하거나 더 짧은 거리에서 6의 약한 발명에 해당한다고 판단했다. 이차적 용기는 그가 중앙 금속 원자와 직접 연결된 분자의 수(여기서3 NH의 수)로 정의한 조정 번호를 가리켰다. 다른 콤플렉스에서 그는 4 또는 8의 조정 번호를 발견했다.
이러한 견해와 다른 유사한 견해에 대해 1904년 리처드 아베그는 원소의 최대 긍정성과 부정성의 차이는 종종 8이라고 말하는 아베그의 법칙으로 알려진 것을 공식화했다. 이 규칙은 1916년 후반에 길버트 N에 사용되었다. 루이스는 입체 원자 이론에서 "옥텟 규칙"을 공식화했다.
현대 용어로는 베르너의 1차 용기는 산화 상태에 해당하며, 그의 2차 용기는 조정 번호라고 한다. Co-Cl 본드(위의 예에서)는 현재 이오닉으로 분류되며, 각 Co-N 본드는 루이스 산과3+ 루이스 베이스 NH3 사이의 좌표 공밸런트 결합이다.
작동하다
참조
- W. Gregory Jackson; Josephine A. McKeon; Silvia Cortez (2004). "Alfred Werner's Inorganic Counterparts of Racemic and Mesomeric Tartaric Acid: A Milestone Revisited". Inorg. Chem. 43 (20): 6249–6254. doi:10.1021/ic040042e. PMID 15446870.
- Kristin Bowman-James (2005). "Alfred Werner Revisited: The Coordination Chemistry of Anions". Acc. Chem. Res. 38 (8): 671–678. doi:10.1021/ar040071t. PMID 16104690.
- ^ https://www.nobelprize.org/nobel_prizes/chemistry/laureates/1913/werner-bio.html 노벨상, 2012년 12월 1일 회수
- ^ Jump up to: a b c d e "Alfred Werner - Swiss chemist". britannica.com. Retrieved 14 April 2018.
외부 링크
- 1913년 12월 11일 노벨 강연회를 포함한 알프레드 베르너 Nobelprize.org
- 1913년 노벨 화학상 - 분자 내 원자의 연결에 관한 그의 연구에 대한 짧은 기사로서 그는 이전의 연구에 새로운 빛을 던졌고 특히 무기 화학 분야에서 새로운 연구 분야를 열었다.