헥솔
Hexol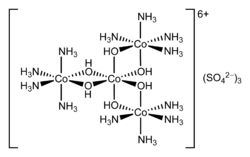 | |
 | |
| 이름 | |
|---|---|
| IUPAC 이름 트리스[tetrammine-μ-dihydroxocobalt(III)]코발트(III) 이온 | |
| 식별자 | |
3D 모델(JSmol) | |
| |
| |
| 특성. | |
| Co4H42N12O18S3 | |
| 어금질량 | 830.31 g·190−1 |
| 물에 조금 녹는다. | |
달리 명시된 경우를 제외하고, 표준 상태(25°C [77°F], 100 kPa)의 재료에 대한 데이터가 제공된다. | |
| Infobox 참조 자료 | |
헥솔은 조정 콤플렉스 {[Co(NH3)(4OH)]23Co}6+의 다양한 염류의 명칭이다. 이 염들은 최초의 합성 비탄소 함유 치랄 화합물로서 역사적 의의가 있다.[2] 황산염은 {[Co(NH3)(423OH)]Co}(SO4)(3HO2)라는 공식을 가지고 있다.x[3]
준비 및 광학 분해능
헥솔의 염분은 비록 그 구조를 인정한 것은 베르너지만,[4] 요르겐센에 의해 처음 설명되었다.[5] 소금은 암모니아와 같은 묽은 염기(base)로 [Co(NH3)(4HO2)]23+를 가열한 후 황산염의 침전을 통해 제조된다.[1]
- 4 [Co(NH32)]423+ → {[Co(NH3)(4OH)]23Co}6+ + 4NH4+ + 2H+ + 2 HO2
조건에 따라 9-하이드레이트, 6-하이드레이트, 4-하이드레이트를 얻는다. 이 소금들은 짙은 갈색의 자외선 혹은 검은 표의 결정체로 존재한다. 그 소금들은 물에 용해도가 낮다. 농축 염산으로 처리하면 헥솔이 시스디아쿼테트람미네코발트(III) 황산염으로 전환된다. 묽은 황산을 끓일 때, 헥솔은 산소와 질소의 진화에 따라 분해된다.[1]
광학 분해능
역사적인 일련의 실험에서 {[Co(NH3)(4OH)]23Co}6+은(는) D-(+)-bromocamphorsulfonate염 소금의 분수 결정으로 해결되었다.[5] 보다 효율적인 해상도는 bis(타르트라토) diantimonate(III) 음이온을 포함한다. 육각 육각은 2640°[6]의 높은 특정 회전을 가진다. D3 포인트 그룹에 속한다.
"두 번째 육각형"
베르너는 또한 그가 선형 테트라머로 잘못 식별한 두 번째 아치랄 헥솔(프레미의 소금 생산에서 나온 작은 부산물)을 묘사했다. 두 번째 헥솔은 (각 이온에 6개의 코발트 센터를 포함하고 있으며) 4차핵이 아니다.[7] 포인트 그룹은 C이고2h, 공식은 [Co
6(NH
3)(
14OH)
8O]6+
인
2 반면, 헥솔의 포인트 그룹은 [Co
4(NH
3)(
12OH)]
66+
이다.
참조
- ^ a b c Kauffman, George B.; Pinnell, Robert P. (1960). "Tris[tetrammine-μ-dihydroxo-cobalt(III)]cobalt(III) Sulfate 4-Hydrate". Tris[Tetrammine-μ-Dihydroxo-Cobalt(III)] Cobalt(III) Sulfate 4-Hydrate. Inorganic Syntheses. Vol. 6. pp. 176–179. doi:10.1002/9780470132371.ch56. ISBN 9780470132371.
- ^ Miessler, G. L. and Tarr, D. A. 무기화학, 3부, Pearson/Prentice Hall 출판사, ISBN 0-13-035471-6.
- ^ Ernst, Karl-Heinz; Berke, Heinz (2011). "Optical Activity and Alfred Werner's Coordination Chemistry". Chirality. 23 (3): 187–189. doi:10.1002/chir.20912. PMID 20928897.
- ^ Jørgensen, S. M. (1898). "Zur Konstitution der Kobalt-, Chrom- und Rhodiumbasen". Zeitschrift für Anorganische Chemie. 16: 184–197. doi:10.1002/zaac.18980160116.
- ^ a b Werner, A. (1907). "Über mehrkernige Metallammoniake" [Poly-nucleated Metal-amines]. Ber. Dtsch. Chem. Ges. (in German). 40 (2): 2103–2125. doi:10.1002/cber.190704002126.
- ^ Yasui, Takaji; Ama, Tomoharu; Kauffman, George B. (1992). "Resolution of the Dodecaamminehexa-μ-Hydroxo-Tetracobalt(III) Ion". Inorganic Syntheses. Inorganic Syntheses. Vol. 29. pp. 169–174. doi:10.1002/9780470132609.ch41. ISBN 9780470132609.
- ^ Jackson, W. Gregory; McKeon, Josephine A.; Zehnder, Margareta; Neuberger, Markus; Fallab, Silvio (2004). "The rediscovery of Alfred Werner's second hexol". Chemical Communications (20): 2322–2323. doi:10.1039/B408277J. PMID 15490001.
외부 링크
- 1997년 9월 헥솔 분자 웹사이트
- 국가 오염 물질 목록 – 코발트 팩트 시트