HSD17B1
HSD17B1| HSD17B1 | |||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||||||||||
| |||||||||||||||||||||||||
| 식별자 | |||||||||||||||||||||||||
| 별칭 | HSD17B1, EDH17B2, EDHB17, HSD17, SDR28C1, hydroxysteroid (17-beta) dehydrogenase 1, hydroxysteroid 17-beta dehydrogenase 1, E2DH, 17-beta-HSD, 20-alpha-HSD, Hsd17b1 | ||||||||||||||||||||||||
| 외부 ID | OMIM: 109684 MGI: 105077 HomoloGene: 37303 GeneCard: HSD17B1 | ||||||||||||||||||||||||
| |||||||||||||||||||||||||
| |||||||||||||||||||||||||
| |||||||||||||||||||||||||
| |||||||||||||||||||||||||
| 직교체 | |||||||||||||||||||||||||
| 종 | 인간 | 마우스 | |||||||||||||||||||||||
| 엔트레스 | |||||||||||||||||||||||||
| 앙상블 | |||||||||||||||||||||||||
| 유니프로트 | |||||||||||||||||||||||||
| RefSeq(mRNA) | |||||||||||||||||||||||||
| RefSeq(단백질) | |||||||||||||||||||||||||
| 위치(UCSC) | Cr 17: 42.55 – 42.56Mb | Chr 11: 100.97 – 100.97Mb | |||||||||||||||||||||||
| PubMed 검색 | [3] | [4] | |||||||||||||||||||||||
| 위키다타 | |||||||||||||||||||||||||
| |||||||||||||||||||||||||
17β-히드록시스테로이드 탈수소효소 1(17β-HSD1)은 인간에서 HSD17B1 유전자에 의해 인코딩되는 효소다.[5][6][7]이 효소는 안드로겐과 에스트로겐의 C17 히드록시/케토군을 산화 또는 감소시켜 이러한 성 스테로이드의 효능을 조절할 수 있다.
함수
이 효소는 에스트론(E1)과 에스트라디올(E2)의 상호 변환과 안드로스테디온과 테스토스테론의 상호 변환을 담당한다.
- 17β-에스트라디올 + NADP+ + ⇌에스트론 + NADPH + H+
- 테스토스테론 + NADP+ + Androstenedione + NADPH+ + H
인간 17β-HSD1 이소자임은 안드로겐 위에 있는 에스트로겐에 대해 매우 구체적이지만 설치류 이소자임은 덜 구체적이다.[8]
디스커버리
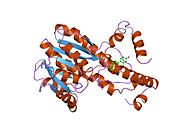
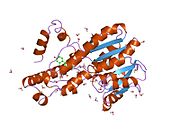
인간 17β-HSD1은 17β-HSD 계열의 첫 번째 효소로서 복제되어 그 염기서열이 식별되었다.[9][10]그것의 3차원 구조는 또한 인간 스테로이드 변환 효소의 첫 번째 예다.[11]
구조
이 효소는 로스만 접이식이라고 알려진 특징적인 3층(αβα) 샌드위치를 함유한 쇼트 체인 탈수소효소 영역을 함유하고 있다.인간 효소는 327개의 아미노산을 함유하고 있으며 34.5kDa의 동일한 하위유닛 2개를 가진 호모디머로 존재한다. N-단자 쇼트체인 탈수소효소 영역에는 NADP+/NADPH 공동 인자 결합 부위가 포함되어 있다.좁고 소수성 C-단자 영역에는 스테로이드 기질을 위한 결합 포켓이 포함되어 있다.
임상적 유의성
에스트라디올은 디하이드로테스토스테론(DHT)이 유방암 성장을 억제하는 동안 자극을 준다.또한 17β-HSD1 수치는 에스트라디올과 양의 상관관계가 있고 유방암 세포의 DHT 수치와 부정적으로 상관관계가 있다.따라서 17β-HSD1은 유방암 치료의 가능한 약물 표적을 나타낸다.[13]
참고 항목
메모들
이 글의 2016년 버전은 외부 전문가가 이중 출판 모델로 업데이트했다.해당 학술적 동료 검토 기사는 진에 게재되었으며, 다음과 같이 인용할 수 있다. Wanhong He; Misra Gauri; Tang Li; Ruixuan Wang; Sheng-Xiang Lin (19 April 2016). "Current knowledge of the multifunctional 17β-hydroxysteroid dehydrogenase type 1 (HSD17B1)". Gene. Gene Wiki Review Series. 588 (1): 54–61. doi:10.1016/J.GENE.2016.04.031. ISSN 0378-1119. PMC 6649686. PMID 27102893. Wikidata Q38814423. |
참조
- ^ a b c GRCh38: 앙상블 릴리스 89: ENSG00000108786 - 앙상블, 2017년 5월
- ^ a b c GRCm38: 앙상블 릴리스 89: ENSMUSG000019301 - 앙상블, 2017년 5월
- ^ "Human PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ "Mouse PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ Luu-The V, Labrie C, Simard J, Lachance Y, Zhao HF, Couët J, Leblanc G, Labrie F (Feb 1990). "Structure of two in tandem human 17 beta-hydroxysteroid dehydrogenase genes". Molecular Endocrinology. 4 (2): 268–75. doi:10.1210/mend-4-2-268. PMID 2330005.
- ^ Persson B, Kallberg Y, Bray JE, Bruford E, Dellaporta SL, Favia AD, Duarte RG, Jörnvall H, Kavanagh KL, Kedishvili N, Kisiela M, Maser E, Mindnich R, Orchard S, Penning TM, Thornton JM, Adamski J, Oppermann U (Mar 2009). "The SDR (short-chain dehydrogenase/reductase and related enzymes) nomenclature initiative". Chemico-Biological Interactions. 178 (1–3): 94–8. doi:10.1016/j.cbi.2008.10.040. PMC 2896744. PMID 19027726.
- ^ "Entrez Gene: HSD17B1 Hydroxysteroid (17-beta) dehydrogenase 1".
- ^ Saloniemi T, Jokela H, Strauss L, Pakarinen P, Poutanen M (2012). "The diversity of sex steroid action: novel functions of hydroxysteroid (17β) dehydrogenases as revealed by genetically modified mouse models". The Journal of Endocrinology. 212 (1): 27–40. doi:10.1530/JOE-11-0315. PMID 22045753.
- ^ Luu The V, Labrie C, Zhao HF, Couët J, Lachance Y, Simard J, Leblanc G, Côté J, Bérubé D, Gagné R (Aug 1989). "Characterization of cDNAs for human estradiol 17 beta-dehydrogenase and assignment of the gene to chromosome 17: evidence of two mRNA species with distinct 5'-termini in human placenta". Molecular Endocrinology. 3 (8): 1301–9. doi:10.1210/mend-3-8-1301. PMID 2779584.
- ^ a b Peltoketo H, Isomaa V, Mäentausta O, Vihko R (Oct 1988). "Complete amino acid sequence of human placental 17 beta-hydroxysteroid dehydrogenase deduced from cDNA". FEBS Letters. 239 (1): 73–7. doi:10.1016/0014-5793(88)80548-9. PMID 2846351. S2CID 32468574.
- ^ Ghosh D, Pletnev VZ, Zhu DW, Wawrzak Z, Duax WL, Pangborn W, Labrie F, Lin SX (May 1995). "Structure of human estrogenic 17 beta-hydroxysteroid dehydrogenase at 2.20 A resolution". Structure. 3 (5): 503–13. doi:10.1016/S0969-2126(01)00183-6. PMID 7663947.
- ^ Lin SX, Yang F, Jin JZ, Breton R, Zhu DW, Luu-The V, Labrie F (Aug 1992). "Subunit identity of the dimeric 17 beta-hydroxysteroid dehydrogenase from human placenta". The Journal of Biological Chemistry. 267 (23): 16182–7. PMID 1322895.
- ^ Aka JA, Mazumdar M, Chen CQ, Poirier D, Lin SX (Apr 2010). "17beta-hydroxysteroid dehydrogenase type 1 stimulates breast cancer by dihydrotestosterone inactivation in addition to estradiol production". Molecular Endocrinology. 24 (4): 832–45. doi:10.1210/me.2009-0468. PMC 5417535. PMID 20172961.
추가 읽기
- Blomquist CH (Dec 1995). "Kinetic analysis of enzymic activities: prediction of multiple forms of 17 beta-hydroxysteroid dehydrogenase". The Journal of Steroid Biochemistry and Molecular Biology. 55 (5–6): 515–24. doi:10.1016/0960-0760(95)00200-6. PMID 8547176. S2CID 21487072.
- Lin SX, Shi R, Qiu W, Azzi A, Zhu DW, Dabbagh HA, Zhou M (Mar 2006). "Structural basis of the multispecificity demonstrated by 17beta-hydroxysteroid dehydrogenase types 1 and 5". Molecular and Cellular Endocrinology. 248 (1–2): 38–46. doi:10.1016/j.mce.2005.11.035. PMID 16480815. S2CID 19087697.
- Peltoketo H, Isomaa V, Vihko R (Oct 1992). "Genomic organization and DNA sequences of human 17 beta-hydroxysteroid dehydrogenase genes and flanking regions. Localization of multiple Alu sequences and putative cis-acting elements". European Journal of Biochemistry. 209 (1): 459–66. doi:10.1111/j.1432-1033.1992.tb17310.x. PMID 1327779.
- Winqvist R, Peltoketo H, Isomaa V, Grzeschik KH, Mannermaa A, Vihko R (Oct 1990). "The gene for 17 beta-hydroxysteroid dehydrogenase maps to human chromosome 17, bands q12-q21, and shows an RFLP with ScaI". Human Genetics. 85 (5): 473–6. doi:10.1007/BF00194219. PMID 1977681. S2CID 38282181.
- Luu-The V, Labrie C, Zhao HF, Couët J, Lachance Y, Simard J, Côté J, Leblanc G, Lagacé L, Bérubé D (1990). "Purification, cloning, complementary DNA structure, and predicted amino acid sequence of human estradiol 17 beta-dehydrogenase". Annals of the New York Academy of Sciences. 595: 40–52. doi:10.1111/j.1749-6632.1990.tb34281.x. PMID 2197970. S2CID 37554424.
- Baker ME (May 1989). "Human placental 17 beta-hydroxysteroid dehydrogenase is homologous to NodG protein of Rhizobium meliloti". Molecular Endocrinology. 3 (5): 881–4. doi:10.1210/mend-3-5-881. PMID 2547159.
- Tremblay Y, Ringler GE, Morel Y, Mohandas TK, Labrie F, Strauss JF, Miller WL (Dec 1989). "Regulation of the gene for estrogenic 17-ketosteroid reductase lying on chromosome 17cen----q25". The Journal of Biological Chemistry. 264 (34): 20458–62. PMID 2584224.
- Luu The V, Labrie C, Zhao HF, Couët J, Lachance Y, Simard J, Leblanc G, Côté J, Bérubé D, Gagné R (Aug 1989). "Characterization of cDNAs for human estradiol 17 beta-dehydrogenase and assignment of the gene to chromosome 17: evidence of two mRNA species with distinct 5'-termini in human placenta". Molecular Endocrinology. 3 (8): 1301–9. doi:10.1210/mend-3-8-1301. PMID 2779584.
- Peltoketo H, Isomaa V, Mäentausta O, Vihko R (Oct 1988). "Complete amino acid sequence of human placental 17 beta-hydroxysteroid dehydrogenase deduced from cDNA". FEBS Letters. 239 (1): 73–7. doi:10.1016/0014-5793(88)80548-9. PMID 2846351. S2CID 32468574.
- Nicolas JC, Harris JI (Jan 1973). "Human placental 17 -oestradiol dehydrogenase. Sequence of a tryptic peptide containing an essential cysteine". FEBS Letters. 29 (2): 173–6. doi:10.1016/0014-5793(73)80554-X. PMID 4719204. S2CID 44967040.
- Burns DJ, Engel LL, Bethune JL (Jul 1972). "Amino acid composition and subunit structure. Human placental 17 -estradiol dehydrogenase". Biochemistry. 11 (14): 2699–703. doi:10.1021/bi00764a023. PMID 5045524.
- Murdock GL, Chin CC, Offord RE, Bradshaw RA, Warren JC (Oct 1983). "Human placental estradiol 17 beta-dehydrogenase. Identification of a single histidine residue affinity-labeled by both 3-bromoacetoxyestrone and 12 beta-bromoacetoxy-4-estrene-3,17-dione". The Journal of Biological Chemistry. 258 (19): 11460–4. PMID 6578212.
- Andersson S, Geissler WM, Patel S, Wu L (Jun 1995). "The molecular biology of androgenic 17 beta-hydroxysteroid dehydrogenases". The Journal of Steroid Biochemistry and Molecular Biology. 53 (1–6): 37–9. doi:10.1016/0960-0760(95)00039-3. PMID 7626483. S2CID 54417090.
- Tremblay MR, Auger S, Poirier D (May 1995). "Synthesis of 16-(bromoalkyl)-estradiols having inhibitory effect on human placental estradiol 17 beta-hydroxysteroid dehydrogenase (17 beta-HSD type 1)". Bioorganic & Medicinal Chemistry. 3 (5): 505–23. doi:10.1016/0968-0896(95)00041-E. PMID 7648200.
- Ghosh D, Pletnev VZ, Zhu DW, Wawrzak Z, Duax WL, Pangborn W, Labrie F, Lin SX (May 1995). "Structure of human estrogenic 17 beta-hydroxysteroid dehydrogenase at 2.20 A resolution". Structure. 3 (5): 503–13. doi:10.1016/S0969-2126(01)00183-6. PMID 7663947.
- Sawetawan C, Milewich L, Word RA, Carr BR, Rainey WE (Mar 1994). "Compartmentalization of type I 17 beta-hydroxysteroid oxidoreductase in the human ovary". Molecular and Cellular Endocrinology. 99 (2): 161–8. doi:10.1016/0303-7207(94)90004-3. PMID 8206323. S2CID 54331976.
- Normand T, Narod S, Labrie F, Simard J (Apr 1993). "Detection of polymorphisms in the estradiol 17 beta-hydroxysteroid dehydrogenase II gene at the EDH17B2 locus on 17q11-q21". Human Molecular Genetics. 2 (4): 479–83. doi:10.1093/hmg/2.4.479. PMID 8389226.
- Zhao Z, Yazdani A, Shen Y, Sun Z, Bailey J, Caskey CT, Lee CC (Sep 1996). "Molecular dissection of a cosmid from a gene-rich region in 17q21 and characterization of a candidate gene for alpha-N-acetylglucosaminidase with two cDNA isoforms". Mammalian Genome. 7 (9): 686–90. doi:10.1007/s003359900206. PMID 8703123. S2CID 8692823.