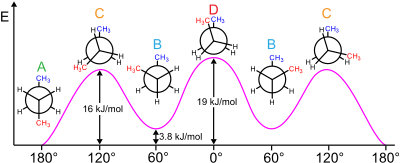
고슈 효과
Gauche effect
순응 이성질체론 연구에서 가우슈 효과는 거슈 순응(약 60°의 비틀림 각도로 분리된 집단)이 나타나는 비정상적인 상황이다.반순응(180°)[2]보다 안정적이다.
컨포머의 상대적 안정성에 영향을 미치는 강도와 전자적 효과가 모두 있다.일반적으로, 강직 효과는 큰 대체물을 서로 멀리 떨어뜨리는 경향이 있다.그러나, 일반적으로 매우 선택적인 특정 대체물에는 해당되지 않는다.대신에, 이러한 집단이 거슈가 되는 것을 전자적으로 선호하는 것이 있다.대표적인 연구 사례로는 1,2-디플루오로에탄(HFCCFH22), 에틸렌 글리콜, 비실리-디플루오로알킬 구조 등이 있다.
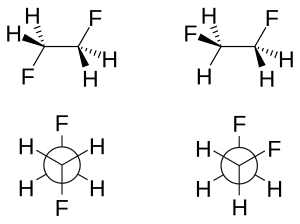 1,2-디플루로에탄(상단)과 해당 뉴먼 투영(하단)에서 반정응(왼쪽)이 거슈정응(오른쪽)보다 안정성이 떨어진다.
1,2-디플루로에탄(상단)과 해당 뉴먼 투영(하단)에서 반정응(왼쪽)이 거슈정응(오른쪽)보다 안정성이 떨어진다.
거슈 효과에 대한 두 가지 주요 설명이 있는데, 바로 초결합과 휨결합이다.초점화 모델에서는 C–H σ 본딩 궤도로부터 C–F σ* 항균 궤도까지의 전자 밀도의 기증은 거슈 이소체의 안정화의 근원으로 간주된다.불소의 전기성이 더 크기 때문에 C-H orbital 궤도보다 C-H orbital 궤도 공여가 더 나은 반면, C–F orbital* 궤도 공여가 C–H σ* 궤도보다 더 나은 전자 공여자가 된다.오직 거슈 순응만이 더 나은 기증자와 더 나은 수용자 사이에 좋은 중첩을 허용한다.
디플루오로에탄의 거슈 효과에 대한 휜 결합 설명의 핵심은 불소의 큰 전기성으로 인해 양쪽 C-F 결합의 p 궤도 문자 증가다.그 결과 전자 밀도는 중앙 C-C 결합의 좌우로 위아래로 쌓인다.결과적으로 감소된 궤도 오버랩은 거슈 준수를 가정할 때 부분적으로 보상될 수 있으며, 구부러진 결합을 형성한다.이 두 가지 모델 중, 하이퍼 콘주화는 일반적으로 디플루오로에탄의 거슈 효과 뒤에 있는 주요 원인으로 여겨진다.[5][6]
두 로타머의 분자 기하학은 실리코 작업에서 증강된 고해상도 적외선 분광법에 의해 실험적으로 얻을 수 있다.[2]위에서 설명한 모델에 따라, 탄소-탄소 결합 길이는 항로타머의 경우 더 길다(pm 151.4 pm 대 150).거슈 로타머 내 불소 원자들 사이의 강한 반발은 CCF 결합 각도 증가(3.2°)와 FCCF 이음각 증가(기본값 60° ~ 71°)를 유발한다.
관련 화합물 1,2-디플루오로-1,2-디페닐타인에서 threo 이소머(X선 회절 및 NMR 연결 상수)가 발견되어 두 페닐 그룹과 두 불소 그룹 사이에 반호환성을 가지며, 두 그룹에 대한 가우체 순응이 모두 에리스로 이소머에 대해 발견된다.[7]실리코 결과에 따르면 이 순응은 0.21 kcal/mol(880 J/mol)만큼 더 안정적이다.
4개의 연속 형광 투시 대체물의 올-시합 배열을 특징으로 하는 분자에 대해서도 가우슈 효과가 보고되었다.네 번째 제품을 설치하기 위한 반응은 입체적이다.[8]
거슈 효과는 또한 1,2-디메트호엑시테탄과[citation needed] 일부 비시날-디니트로알킬 화합물에서도 나타난다.
알켄 시스 효과는 특정 알켄의 유사한 비정형 안정화다.
외부 영향
거슈 효과는 두 컨포머의 극성 차이가 크기 때문에 용제 효과에 매우 민감하다.예를 들어 고형 상태의 2,3-디니트로-2,3-디메틸부탄은 벤젠 용액의 거슈 컨포머를 79:21의 비율로 선호하지만, 카본 테트라클로라이드에서는 58:42의 비율로 안티 컨포머를 선호한다.[9]또 다른 경우는 trans-1,2 difluorclohexane인데, 이것은 더 많은 극성 용매에서 항디아제 컨포머보다는 이등성 컨포머에 대한 선호도가 더 높다.[6]
참고 항목
참조
- ^ Floris Akkerman, Jürgen Buschmann, Dieter Lentz, Peter Luger, Eva Rödel (2003). "Crystal and molecular structure of 1,2-difluoroethane and 1,2-diiodoethane". Journal of Chemical Crystallography. 33: 969–975. doi:10.1023/A:1027494101785.
{{cite journal}}: CS1 maint: 작성자 매개변수 사용(링크) - ^ a b Gauche 효과 연구에 대한 기여. 1,2-디플루오로에탄 노만 C의 항로타머 완전구조크레이그, 앤서니 첸, 서기환, 스테판 클라이, 게오르크 C.멜라우, 브렌다 P.윈뉴시저, 맨프레드 윈뉴시저 J. Am. Chem. Soc.; 1997; 119(20) 페이지 4789–4790; (통신) doi:10.1021/ja963819e
- ^ J, McMurry (2012). Organic chemistry (8 ed.). Belmont, CA: Brooks/Cole. p. 98. ISBN 9780840054449.
- ^ Moss, GP (1996-01-01). "Basic terminology of stereochemistry (IUPAC Recommendations 1996)". Pure and Applied Chemistry. 68 (12): 2193–2222. doi:10.1351/pac199668122193. ISSN 1365-3075.
- ^ Goodman, L.; Gu, H.; Pophristic, V.가우슈 효과 1,2-디플루오로에탄.초동화, 벤트 본즈, 스테릭 리액션J. 체육 Chem. A. 2005, 109, 1223–1229. doi:10.1021/jp046290d
- ^ a b 데이비드 오하건오르가노플루오린 화학에 대한 이해.C-F 채권 소개.Chem. Soc. 2008년 개정판 doi:10.1039/b711844a
- ^ Vicinal difluoro 모티브: The synthesis and conformation of erythro- and threo- diastereoisomers of 1,2-difluorodiphenylethanes, 2,3-difluorosuccinic acids and their derivatives O'Hagan D, Rzepa H, Schuler M, Slawin A Beilstein Journal of Organic Chemistry, 2006 2:19 ( 2 October 2006 ) doi:10.1186/1860-5397-2-19
- ^ 루크 헌터, 데이비드 오하간, 알렉산드라 M. Z의 합성 4대 Vicinal Fluorine 모티브의 Enantoselective 합성.슬라윈 J. Am. Chem. Soc.; 2006; 128(51) 페이지 16422–16423; (통신) doi:10.1021/ja066188p
- ^ 스미스, 마이클B.; 3월 J. 3월의 첨단 유기화학, 제5판.2001년 와일리ISBN 0-471-58589-0