폴다머
Foldamer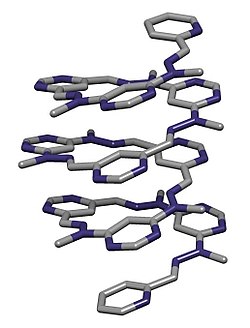
화학에서, 폴다머는 용액에서 순응적으로 순응된 상태로 접히는 이산 체인 분자 또는 올리고머이다.나선이나 β-시트와 같이 잘 정의된 순응으로 접히는 단백질, 핵산, 다당류의 능력을 모방한 인공 분자다.폴더머의 구조는 비인접 단층재 사이의 비균등 상호작용에 의해 안정화된다.[2][3]폴다머는 예측 가능한 구조로 큰 분자를 설계하는 것을 주요 목표로 연구된다.폴더머의 연구는 분자 자가 조립, 분자 인식, 숙주-게스트 화학의 주제와 관련이 있다.null
디자인
폴더머는 크기가 다양할 수 있지만, 비동치적, 비인접적 상호작용의 존재에 의해 정의된다.그들이 나선에 안정적으로 인접한 공유 결합 interactions.,[4]Foldamers으로 인해 접어서 이 정의 poly(isocyanates)(일반적으로(폴리우레탄으로 알려져))과 poly(prolines)에 큰 거시적 접기solvophobic 효과에 의해(소수성 붕괴)발생하는 역동적인 접기 반응[폅다 → 접],, 있어 분자들을 배제한다.t접힌 폴더머의 최종 에너지 상태는 비균등 상호작용에 기인한다.완전히 접히고 펴진 상태가 어느 부분 접힌 상태보다 안정적이기 때문에 이러한 상호작용은 가장 안정적인 3차 구조를 형성하기 위해 협력적으로 작용한다.[5]null
접힘 예측
폴더머의 구조는 종종 그것의 일차적인 순서에서 예측할 수 있다.이 과정은 다양한 조건에서 원자 수준에서 접히는 평형을 동적으로 시뮬레이션하는 것을 포함한다.이러한 유형의 분석은 작은 단백질에도 적용될 수 있지만 계산 기술은 가장 짧은 시퀀스를 제외하고는 모두 시뮬레이션할 수 없다.[6]null
폴더머의 접히는 경로는 다른 열역학 및 운동 조건에서 실험적으로 결정된 선호 구조로부터의 변화를 측정하여 결정할 수 있다.구조물의 변화는 선호 구조물의 백본 원자 위치에서 루트 평균 제곱 편차를 계산하여 측정한다.다른 조건에서 폴더머의 구조는 계산적으로 결정되고 실험적으로 검증될 수 있다.온도, 용제 점성, 압력, pH, 염분 농도의 변화는 모두 폴더머 구조에 대한 귀중한 정보를 산출할 수 있다.접힘 평형뿐 아니라 접힘의 운동학적 특성을 측정하면 접힘 구조에서 이러한 다양한 조건이 미치는 영향을 관찰할 수 있다.[6]null
용제는 종종 접히는 데 영향을 미친다.예를 들어 소수성 붕괴와 관련된 접이식 통로는 비극성 용매에서 다르게 접힐 수 있다.이러한 차이는 서로 다른 용제가 분자간 비균형 상호작용에 기초한 서로 다른 최종 폴더머 구조뿐만 아니라 접히는 경로의 서로 다른 중간체들을 안정화시키기 때문이다.[6]null
비동축 교호작용
비록 개별적으로 작지만, 비동분자간 상호작용은 화학반응을 주요한 방식으로 변화시킨다.아래에 열거된 것은 화학자들이 접이식 설계에 사용한 일반적인 분자간 힘이다.null
공통 디자인
폴더머는 펩티도미메틱 폴더머, 뉴클레오티도미메틱 폴더머, 아바이오틱 폴더머의 3가지 범주로 분류된다.펩티도미메틱 폴더머는 단백질 구조를 모방한 합성 분자인데 반해 뉴클레오티모틱 폴더머는 핵산에서의 상호작용을 기반으로 한다.비생물학적 폴더머는 일반적으로 자연에서 발견되지 않는 방향족과 전하 전달 상호작용에 의해 안정화된다.[2]아래에 설명된 세 가지 디자인은 나선형 폴더머를 제외한 폴더머에 대한 무어의 엄격한[3] 정의에서 벗어난다.null
펩티도미메틱스
펩티도미메틱 폴더머는 헬리컬 구조를 채택하는 경우가 많기 때문에 이전에 언급한 폴더머의 정의를 깨는 경우가 많다.그들은 디자인과 능력 때문에 폴더머 연구의 주요 랜드마크를 대표한다.[7][8]펩티도미메틱의 가장 큰 그룹은 β – 펩타이드, β – 펩타이드 및 Δ – 펩타이드로 구성되며, 가능한 단일 조합으로 구성된다.[8]이러한 펩타이드의 아미노산은 1(β), 2( two) 또는 3(Δ) 메틸렌 탄소에 의해서만 차이가 날 뿐 구조적인 변화는 심오했다.이러한 펩타이드 시퀀스는 시퀀스 제어가 신뢰성 있는 접힘 예측으로 이어지기 때문에 연구성이 높다.또한, 측면 펩타이드 결합의 카복실 및 아미노 종단 사이에 여러 개의 메틸렌 탄화수소를 사용하여 다양한 R 그룹 사이드 체인을 설계할 수 있다.β-펩타이드의 신기함을 보여주는 한 예는 라이저와 동료들의 연구 결과에서 볼 수 있다.[9]그들은 α-아미노산과 cis-β-아미노피아노프산(cis-β-ACCs)으로 구성된 이질화합물을 사용하여 과점기에서 7개의 잔류물만큼 짧은 헬리컬 시퀀스의 형성을 발견했으며 5개의 잔류물에서 정의했다. 즉, 순환 β-아미노산을 함유한 펩타이드 고유의 품질이다.[10][11][12][13]null
뉴클레오티도메틱
뉴클레오토미메틱스는 일반적으로 폴더머로 적합하지 않다.대부분은 특정하지 않게 DNA를 표적으로 삼기 위해 단일 DNA 염기, 뉴클레오시드 또는 뉴클레오티드를 모방하도록 설계되었다.[14][15][16]이것들은 항암제, 항바이러스제, 항풍구제 등의 여러 가지 다른 약용법을 가지고 있다.null
아바이오틱스
아바이오틱스 폴더머는 다시 동적 폴딩을 나타내도록 설계된 유기 분자다.그들은 그들의 설계에 의해 최적화된 것으로 알려진 하나 또는 몇 개의 알려진 주요 분자간 상호작용을 이용한다.한 예로 수소 결합을 통해 염화물과 같은 음이온을 결합하여 구성하는 올리고프로를 들 수 있다(그림 참조).음이온이 있는 곳에서 폴딩이 유도된다. 폴리피롤 그룹은 그렇지 않으면 순응적 제한이 거의 없다.[17][18]null
기타 예
- m-페닐렌 에틸렌 올로머는 솔보포비아력과 방향족 적층 상호작용에 의해 나선형 순응으로 이동한다.
- β-펩타이드들은 아민과 카복실산 사이에 추가 CH
2 단위를 포함하는 아미노산으로 구성된다.그것들은 효소 분해에 더 안정적이고 항균 활성이 입증되었다. - 펩타이드(Peptoids)는 N-대체 폴리글리신(N-대체 폴리글리신)으로, 폴리프로라인 I형 헬리컬 구조로 접힌다.[19]
- 소수성 및 방향족 적층 상호작용에 의해 구동되는 수용액에서 접히는 에다머.
- 향기로운 올리고아미드 폴다머 이러한 예들은 가장 크고 구조적으로 가장 잘 특징지어지는 폴다머들 중 하나이다.[20]
- 아릴라미드 폴다머([21]Brilacidin 등)
참조
- ^ Lehn, Jean-Marie; et al. (2003). "Helicity-Encoded Molecular Strands: Efficient Access by the Hydrazone Route and Structural Features". Helv. Chim. Acta. 86 (5): 1598–1624. doi:10.1002/hlca.200390137.
- ^ a b "폴더머: 구조, 속성, 응용 프로그램" 스테판 헤흐트, 이반 헉 에드스.Wiley-VCH, Weinheim, 2007.ISBN 9783527315635
- ^ a b Hill, D. J.; Mio, M. J.; Prince, R. B.; Hughes, T. S.; Moore, J. S. (2001). "A field guide to foldamers". Chem. Rev. 101 (12): 3893–4012. doi:10.1021/cr990120t. PMID 11740924.
- ^ Green, M. M.; Park, J.; Sato, T.; Teramoto, A.; Lifson, S.; Selinger, R. L. B.; Selinger, J. V. (1999). "The Macromolecular Route to Chiral Amplification". Angew. Chem. Int. Ed. 38 (21): 3138–3154. doi:10.1002/(SICI)1521-3773(19991102)38:21<3138::AID-ANIE3138>3.0.CO;2-C. PMID 10556885.
- ^ Gellman, S.H. (1998). "Foldamers: A Manifesto". Acc. Chem. Res. 31 (4): 173–180. doi:10.1021/ar960298r.
- ^ a b c van Gunsteren, Wilfred F. (2007). Foldamers: Structure, Properties, and Applications; Simulation of Folding Equilibria. Wiley-VCH Verlag GmbH & Co. KGaA. pp. 173–192. doi:10.1002/9783527611478.ch6.
- ^ 앤슬린과 더거티, 현대 물리 유기 화학, 대학 과학 도서, 2006, ISBN 978-1-891389-31-3
- ^ a b Martinek, T.A.; Fulop, F. (2012). "Peptidic foldamers: ramping up diversity". Chem. Soc. Rev. 41 (2): 687–702. doi:10.1039/C1CS15097A. PMID 21769415.
- ^ De Pol, S.; Zorn, C.; Klein, C.D.; Zerbe, O.; Reiser, O. (2004). "Surprisingly Stable Helical Conformations in alpha/beta-Peptides by Incorporation of cis-beta-Aminocyclopropate Carboxylic Acids". Angew. Chem. Int. Ed. 43 (4): 511–514. doi:10.1002/anie.200352267. PMID 14735548.
- ^ Seebach, D.; Beck, A.K.; Bierbaum, D. J.; Chem.바이오디브, 2004, 1, 1111-1239.
- ^ Seebach, D.; Beck, A.K.; Bierbaum, D.J. (2004). "Chemical and Biological Investigations of B-Oligoarginines". Chemistry & Biodiversity. 1 (1): 1111–1239. doi:10.1002/cbdv.200490014. PMID 17191776. S2CID 45258727.
- ^ Nizami, Bilal. "FoldamerDB: Database of foldamers". foldamerdb.ttk.hu. Retrieved 2020-07-06.
- ^ Nizami, Bilal; Bereczki-Szakál, Dorottya; Varró, Nikolett; el Battioui, Kamal; Nagaraj, Vignesh U.; Szigyártó, Imola Cs; Mándity, István; Beke-Somfai, Tamás (2020-01-08). "FoldamerDB: a database of peptidic foldamers". Nucleic Acids Research. 48 (D1): D1122–D1128. doi:10.1093/nar/gkz993. ISSN 0305-1048. PMC 7145536. PMID 31686102.
- ^ Longley, DB; Harkin DP; Johnston PG (May 2003). "5-fluorouracil: mechanisms of action and clinical strategies". Nat. Rev. Cancer. 3 (5): 330–338. doi:10.1038/nrc1074. PMID 12724731. S2CID 4357553.
- ^ Secrist, John (2005). "Nucleosides as anticancer agents: from concept to the clinic". Nucleic Acids Symposium Series. 49 (49): 15–16. doi:10.1093/nass/49.1.15. PMID 17150610.
- ^ Rapaport, E.; Fontaine J (1989). "Anticancer activities of adenine nucleotides in mice are mediated through expansion of erythrocyte ATP pools". Proc. Natl. Acad. Sci. USA. 86 (5): 1662–1666. Bibcode:1989PNAS...86.1662R. doi:10.1073/pnas.86.5.1662. PMC 286759. PMID 2922403.
- ^ Sessler, J.L.; Cyr, M.; Lynch, V. (1990). "Synthetic and structural studies of sapphyrin, a 22-.pi.-electron pentapyrrolic "expanded porphyrin"". J. Am. Chem. Soc. 112 (7): 2810. doi:10.1021/ja00163a059.
- ^ Juwarker, H.; Jeong, K-S. (2010). "Anion-controlled foldamers". Chem. Soc. Rev. 39 (10): 3664–3674. doi:10.1039/b926162c. PMID 20730154.
- ^ Angelici, G.; Bhattacharjee, N.; Roy, O.; Faure, S.; Didierjean, C.; Jouffret, L.; Jolibois, F.; Perrin, L.; Taillefumier, C. (2016). "Weak backbone CH⋯O=C and side chain tBu⋯tBu London interactions help promote helix folding of achiral NtBu peptoids". Chemical Communications. 52 (24): 4573–4576. doi:10.1039/C6CC00375C. hdl:11568/837881. PMID 26940758.
- ^ Delsuc, Nicolas; Massip, Stéphane; Léger, Jean-Michel; Kauffmann, Brice; Huc, Ivan (9 March 2011). "Relative Helix−Helix Conformations in Branched Aromatic Oligoamide Foldamers". Journal of the American Chemical Society. 133 (9): 3165–3172. doi:10.1021/ja110677a. PMID 21306159.
- ^ 순응적으로 억제된 항균 아릴라미드 폴더머의 노보 설계 및 생체내 활성.최. 2009년
추가 읽기
- Ivan Huc; Stefan Hecht (2007). Foldamers: Structure, Properties, and Applications. Weinheim: Wiley-VCH. ISBN 978-3-527-31563-5.
- Goodman CM, Choi S, Shandler S, DeGrado WF (2007). "Foldamers as versatile frameworks for the design and evolution of function". Nat. Chem. Biol. 3 (5): 252–62. doi:10.1038/nchembio876. PMC 3810020. PMID 17438550.
리뷰
- ^ Gellman, S.H. (1998). "Foldamers: a manifesto" (PDF). Acc. Chem. Res. 31 (4): 173–180. doi:10.1021/ar960298r. Archived from the original (PDF) on 2008-05-13.
- ^ Zhang DW, Zhao X, Hou JL, Li ZT (2012). "Aromatic Amide Foldamers: Structures, Properties, and Functions". Chem. Rev. 112 (10): 5271–5316. doi:10.1021/cr300116k. PMID 22871167.
- ^ Juwarker, H.; Jeong, K-S. (2010). "Anion-controlled foldamers". Chem. Soc. Rev. 39 (10): 3664–3674. doi:10.1039/b926162c. PMID 20730154.






