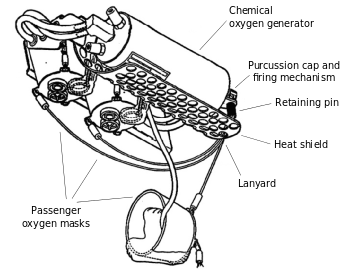
화학적 산소 발생기
Chemical oxygen generator화학적 산소 발생기는 화학 반응을 통해 산소를 방출하는 장치이다.산소 공급원은 보통 무기 과산화물,[1] 염소산염 또는 과염소산염입니다. 오조니드는 유망한 산소 공급원 그룹입니다.발전기는 보통 점화 핀에 의해 점화되며 화학반응은 보통 발열성이기 때문에 발전기는 화재의 위험이 있습니다.슈퍼옥시드 칼륨은 소련 우주 프로그램의 초기 승무원 임무, 비상 상황에서 사용하기 위한 잠수함, 소방관, 그리고 지뢰 구조에서 산소 공급원으로 사용되었다.
민간 여객기 내
민간 항공기는 기내 압력 상실 시 승객을 보호하기 위해 비상 산소를 공급한다.화학적 산소 발생기는 일반적으로 산소통이라고도 하는 압축 산소통을 사용하여 공급되는 조종석 승무원에게는 사용되지 않습니다.좁은 기내 여객기에는 좌석 열마다 머리 위 산소 마스크와 산소 발생기가 있었다.DC-10과 IL-96과 같은 일부 광체 여객기에서는 천장이 승객 위로 너무 높았기 때문에 캐니스터와 산소 마스크가 좌석 등받이의 상단에 장착되었습니다.감압이 발생하면 자동 압력 스위치 또는 수동 스위치로 패널을 열고 마스크를 풀었습니다.승객들이 마스크를 벗기자 고정 핀을 제거하고 산소 생성을 유발했습니다.
산화제 코어는 염소산나트륨(NaClO3)으로, 과산화바륨(BaO2)은 5% 미만이고 과염소산칼륨(KClO)4은 1% 미만입니다.퍼커션 캡에 있는 폭발물은 스티프네이트 납과 테트라젠 혼합물이다.화학 반응은 발열성이며 캐니스터의 외부 온도는 260°C(500°F)에 도달합니다.그것은 12분에서 22분 [2][3]동안 산소를 생산할 것이다.2-마스크 제너레이터의 직경은 약 63mm(2.5인치)이고 길이는 223mm(8.8인치)입니다.3마스크 제너레이터의 직경은 약 70mm(2.8인치)이고 길이는 250mm(9.8인치)입니다.
잘못 출하된 유효기간이 지난 발전기가 잘못 작동해 빈 발전기로 잘못 표시되면서 밸류젯 항공 592편이 추락해 [4]탑승자 전원이 사망했다.ATA DC-10 131편도 1986년 8월 10일 오헤어 공항에 주차되어 있던 중 파괴되었다.원인은 부서진 DC-10 시트의 뒷면에 들어있던 산소통이 실수로 작동하여 화물칸에 실려 수리소로 운송된 것입니다.불이 [5]났을 때 여객기에는 승객이 없었기 때문에 사망자나 부상자는 없었다.
산소초
염소산초 또는 산소초는 염소산나트륨과 철분말이 혼합된 원통형 화학 산소 발생기로, 약 600°C(1,112°F)에서 연소를 점화하면 염화나트륨, 산화철, 혼합물의 kg당 약 6.5 공시간의 고정 속도로 산소를 생성한다.이 혼합물은 적절히 보관하면 유통기한이 무기한입니다. 즉, 양초는 산소 배출량 감소 없이 20년 동안 보관되어 왔습니다.열분해는 산소를 방출한다.타는 쇠가 열을 공급한다.반응 온도를 유지하고 주변 장비를 보호하기 위해 양초를 단열재로 감싸야 합니다.주요 반응은 다음과 같습니다.[6]
- 23 NaClO → 2 NaCl + 3 O2
산소초에는 염소산칼륨과 리튬, 과염소산나트륨과 과염소산리튬도 사용할 수 있다.
2007년 [7]3월 21일, 이 촛불들 중 하나에 의한 폭발로 인해, 핵추진 잠수함인 HMS 타이어리스(S88)에서 두 명의 영국 해군 선원이 사망했다.그 양초는 유압유로 오염되었고, 이것은 혼합물을 [8]태우기 보다는 폭발하게 만들었다.
일부 우주선에 사용되는 Vika 산소 발생기에서 과염소산 리튬은 산소의 원천이다.400°C에서는 무게의 60%를 [9]산소로 방출합니다.
- LiClO4 → LiCl + 22 O
압력 스윙 흡착(PSA) 산소 발생기
기술의 진보로 공기가 공급되고 더 높은 농도의 산소가 필요한 곳에서 사용할 수 있는 산업용 산소 발생기 시스템이 제공되었습니다.압력 스윙 흡착(PSA)은 기체 분리를 위해 분자 체라고 불리는 물질을 포함합니다.산소 발생의 경우, 제올라이트 기반의 체는 [citation needed]질소에 대한 우선 흡착을 강제한다.깨끗하고 건조한 공기가 산소 발생기의 체층을 통과하여 산소가 풍부한 가스를 생성합니다.질소분리막장치도 사용한다.
사용하다
화학적 산소 발생기는 항공기, 소방관, 광산 구조대원, 잠수함, 그리고 저장 수명이 긴 소형 비상 산소 발생기가 필요한 모든 곳에 사용된다.그것들은 보통 이산화탄소의 흡수를 위한 장치, 때로는 수산화리튬으로 채워진 필터가 들어있다; LiOH 1킬로그램은 약 0.5킬로그램의 이산화탄소를2 흡수한다.
- 잠수함에는 자급식 산소 발생기(SCOG)가 사용된다.
- 지뢰로부터의 탈출을 용이하게 하기 위해 자급자족구조장치(SCSR)를 사용한다.
- 국제우주정거장에서는 화학산소발생기가 예비공급장치로 사용된다.각 통은 한 명의 승무원이 하루 [10]동안 충분한 산소를 생산할 수 있다.
「 」를 참조해 주세요.
레퍼런스
- ^ Hayyan M., Hashim M.A., AlNashef I.M., Superoxide Ion: Generation and Chemical Impactions, Chemical.개정판, 2016, 116(5), 페이지 3029–3085.DOI: 10.1021/acs.chemrev.5b00407
- ^ Yunchang Zhang; Girish Kshirsagar; James C. Cannon (1993). "Functions of Barium Peroxide in Sodium Chlorate Chemical Oxygen". Ind. Eng. Chem. Res. 32 (5): 966–969. doi:10.1021/ie00017a028.
- ^ William H. Schechter; R. R. Miller; Robert M. Bovard; C. B. Jackson; John R. Pappenheimer (1950). "Chlorate Candles as a Source of Oxygen". Industrial & Engineering Chemistry. 42 (11): 2348–2353. doi:10.1021/ie50491a045.
- ^ "Fire in the Hold". Mayday. Season 12. Episode 2. 10 August 2012.
- ^ Airliners.net, 사진, Dave Campbell
- ^ Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (2nd ed.). Butterworth-Heinemann. ISBN 978-0-08-037941-8.
- ^ Johnson, C. W. "Degraded Modes and the 'Culture of Coping' in Military Operations: An Analysis of a Fatal Incident on-board HMS Tireless on 20/21 March 2007" (PDF).
- ^ Page, Lewis (22 March 2007). "'Oxygen candle' caused explosion". The Register. Retrieved 2013-09-04.
- ^ M. M. Markowitz, D. A. Boryta, and Harvey Stewart Jr. (1964). "Lithium Perchlorate Oxygen Candle. Pyrochemical Source of Pure Oxygen". Ind. Eng. Chem. Prod. Res. Dev. 3 (4): 321–330. doi:10.1021/i360012a016.
{{cite journal}}: CS1 maint: 작성자 파라미터 사용(링크) - ^ Barry, Patrick (2000). "Breathing Easy on the Space Station". National Aeronautics and Space Administration. Retrieved 9 September 2012.