폴리인산염
Polyphosphate폴리인산염(Polyphosphate)은 산소 원자를 공유함으로써 서로 연결된 사면체 PO4(phosphate) 구조 단위로부터 형성되는 폴리머 옥시온의 염 또는 에스테르를 말한다. 폴리인산염은 선형 또는 순환 고리 구조를 채택할 수 있다. 생물학에서, 폴리인산 에스테르 ADP와 ATP는 에너지 저장과 관련되어 있다. 다양한 폴리인산염은 일반적으로 1에서 5ppm으로 나타나며, 도시 수역의 광물 분리 작용에 응용된다.[1] GTP, CTP, UTP도 각각 단백질 합성, 지질 합성, 탄수화물 대사에서 중요한 뉴클레오티드다. 폴리인산염은 E452로 표시된 식품 첨가물로도 사용된다.
구조
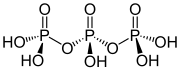
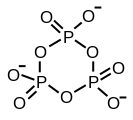
삼인산 구조는 다인산 구조를 정의하는 원리를 잘 보여준다. 산소 센터를 공유하여 서로 연결된 3개의 사면 PO4 단위로 구성된다. 선형 체인의 경우, 최종 인 그룹은 한 개의 산화물을 공유하고 다른 인 센터는 두 개의 산화물을 공유한다. 해당 인산염은 산성 양자의 상실에 의해 산과 관련된다. 주기적 트리머의 경우 각 사면체는 인접한 사면체와 두 개의 정점을 공유한다.
세 귀퉁이의 공유가 가능하다. 이 모티브는 선형 중합체의 교차 연결을 나타낸다. 교차 연결된 폴리인산염은 시트 구조 Phylosilate를 채택하지만 그러한 구조는 극한 조건에서만 발생한다.
형성 및 합성
폴리인산염은 인산 유도체의 중합에 의해 발생한다. 이 과정은 두 개의 인산염 단위가 응축 반응으로 결합하는 것으로 시작한다.
- 2 H(PO4)2− ⇌(PO27)4− + HO2
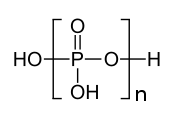
응결은 역반응인 가수분해도 가능하기 때문에 평형으로 나타난다. 프로세스는 단계별로 계속될 수 있으며, 각 단계에서 다른 (PO3)− 장치가 체인에 추가되며, 폴리인산 그림의 브래킷에 있는 부품으로 표시된다. PO는410 응축 반응의 최종 산물로 볼 수 있는데, 각 4면체는 다른 것과 세 모서리를 공유한다. 반대로 오산화 인에 소량의 물을 더하면 중합체의 복잡한 혼합물이 만들어진다.
산성기층 및 복합화 특성
폴리인산염은 약한 염기들이다. 산소 원자 위에 있는 한 쌍의 전자는 전형적인 루이스 산-루이스 염기 상호작용에서 수소 이온(프로톤)이나 금속 이온에 기증될 수 있다. 이것은 생물학에서 중대한 의미를 갖는다. 예를 들어, 아데노신 삼인산염은 pH 7에서 수용액에서 약 25% 양성이 된다.[2]
- ATP4− + H+ ⇌ ATPH3−, pKa 6.6
더 낮은 pH 값에서 추가 양성자가 발생한다.
"고에너지" 인산염 결합
ATP는 금속 이온으로 첼레이트 콤플렉스를 형성한다. 평형에 대한 안정성 상수
- ATP4− + Mg2+ ⇌ Mg ATP2−, 로그 β 4
특히 크다.[3] 마그네슘 복합체의 형성은 단자 인산염 그룹과 나머지 분자 사이의 연계를 약화시키기 때문에 ATP 가수분해 과정에서 중요한 원소다.[2][4]
ATP 가수분해에서 방출되는 에너지는
- ATP4− + H2O → ADP3− + Pi−
ΔG \\} -36.8 kJ−1 mol은 생물학적 표준으로 볼 때 크다. P는i 생물학적 pH로 양성된 무기인산염의 약자다. 그러나 무기질 기준으로는 크지 않다. "고에너지"란 생물계에서 발생할 수 있는 유기화학반응에서 방출되는 에너지의 양에 비례하여 높은 것을 말한다.
고분자 무기질 폴리인산염
높은 분자량 폴리인산염은 잘 알려져 있다.[5] 한 가지 파생상품은 유리(즉, 비정형) 그레이엄의 소금이다. 결정체 고분자 폴리인산염에는 쿠롤의 소금과 마드렐의 소금이 포함된다. 이 종들은 n이 2000년만큼 클 수 있는 [NaPO3][nNaPO3(OH)]2라는 공식을 가지고 있다. 구조 면에서 이들 중합체는 PO3− "모노머"로 구성되며, 체인은 양성자 인산염에 의해 종료된다.[6]
자연에서
1890년 L. Liberman에 의해 살아있는 유기체에서 고분자성 무기체 다인산염이 발견되었다. 이 화합물은 에너지가 풍부한 인산염 결합에 의해 연결된 몇 개에서 몇 백 개의 오토인산 잔류물을 함유한 선형 중합체다.
이전에는 '분자 화석' 또는 극한 조건에서 미생물의 생존을 제공하는 인과 에너지원으로만 여겨졌다. 이 화합물들은 이제 규제적 역할도 하고, 모든 살아있는 유기체의 왕국 대표들에게서 발생하며, 대사교정과 유전적, 효소적 수준 모두에 대한 통제에 참여한다고 알려져 있다. 다인산염은 박테리아의 기하급수적인 성장 단계의 유전 프로그램 특성을 정지 조건인 '느린 차선에서의 삶'에서 세포 생존 프로그램으로 전환하는 데 직접 관여한다. 그들은 박테리아에서 발생하는 많은 규제 메커니즘에 참여한다.
- 그들은 정지 성장 단계와 많은 스트레스를 받는 물질들의 조정에 관여하는 많은 유전자 그룹의 발현을 담당하는 RNA 폴리머아제 소단위인 rpoS의 유도에 참여한다.
- 그것들은 세포 운동성, 생체필름 형성 및 정력을 위해 중요하다.[clarification needed]
- 다인산염과 외인산염은 박테리아 세포의 두 번째 메신저인 구아노신 5'-디프인산염 3'-디프인산염(ppGpp)의 수위 조절에 참여한다.
- 폴리인산염은 살아있는 세포막을 가로지르는 채널 형성에 참여한다. Ca와2+ 함께 폴리인산염과 폴리-b-하이드록시부티이트에 의해 형성된 위의 채널은 다양한 유기체의 수송 과정에 관여한다.
- 미생물에서 폴리인산염의 중요한 기능인 prokaryotes와 하위 eukaryotes는 인산염과 에너지 비축량을 제공하여 변화하는 환경 조건을 처리하는 것이다. 다인산염은 동물 세포에 존재하며, 특히 뼈 조직과 뇌에서 발달과 세포 증식과 분화 과정에서의 규제 과정에 참여하는 것에 관한 많은 자료가 있다.
인간에서 다인산염은 혈액 응고에 중요한 역할을 하는 것으로 보인다. 혈소판에[7] 의해 생산되고 방출되는 혈소판들은 혈전 형성에 필수적인 혈액 응고 인자 XII를 활성화시킨다. 헤게만 인자라고도 불리는 인자 XII는 피브린 형성과 혈전 누출에 기여하는 소염 중재자 브래디키닌의 생성을 개시한다.[8][9] 박테리아에서 파생된 폴리인산염은 감염 시 숙주 면역 반응을 손상시키고 재조합성인성인산염을 대상으로 하는 것은 생쥐의 패혈증 생존을 향상시킨다.[10] 무기질 폴리인산염은 독성 중금속 양이온에 대한 효모세포의 내성에 결정적인 역할을 한다.[11]
식품첨가물로 사용
식품 첨가물로 폴리인산나트륨(E452(i)), 폴리인산칼륨(E452(ii), 폴리인산나트륨(E452(ii) 및 폴리인산칼슘(E452(iv)이 사용된다. 그것들은 일반적으로 다른 인산염 공급원(식품에서 자연적으로 발생하는 것 포함)에 기인하는 것 이외의 잠재적인 건강 위험을 제기하는 것으로 알려져 있지 않다. 고인산혈증은 물론 뼈와 심혈관 질환에 미치는 유해한 영향에 대한 우려가 제기됐지만, 이는 인산염 공급원의 과다 섭취에만 관련이 있는 것으로 보인다. 전체적으로 합리적인 소비량(하루 몸무게 kg당 최대 40mg의 인산염)은 건강상의 위험이 없는 것으로 보인다.[12][13]
참고 항목
참조
- ^ "The Phosphate Method For Producing Quality Drinking Water" (PDF). Carus Chemical Company. 2001. Archived from the original (PDF) on 2011-04-19. Retrieved 2011-04-20.
- ^ a b Storer A, Cornish-Bowden A (1976). "Concentration of MgATP2- and other ions in solution. Calculation of the true concentrations of species present in mixtures of associating ions". Biochem J. 159 (1): 1–5. doi:10.1042/bj1590001. PMC 1164030. PMID 11772.
- ^ Wilson J, Chin A (1991). "Chelation of divalent cations by ATP, studied by titration calorimetry". Anal Biochem. 193 (1): 16–9. doi:10.1016/0003-2697(91)90036-S. PMID 1645933.
- ^ Garfinkel L, Altschuld R, Garfinkel D (1986). "Magnesium in cardiac energy metabolism". J Mol Cell Cardiol. 18 (10): 1003–13. doi:10.1016/S0022-2828(86)80289-9. PMID 3537318.
- ^ Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (2nd ed.). Butterworth-Heinemann. ISBN 978-0-08-037941-8.
- ^ 클라우스 슈뢰터, 게르하르트 베르트만, 토마스 스태펠, 프리드리히 볼, 토마스 클라인, 토머스 호프만 "인산 및 인산" 2008년 울만 산업 화학 백과사전 Wiley-VCH, Weinheim의 "인산 및 인산". doi:10.1002/14356007.a19_465.pub3
- ^ Ruiz FA, Lea CR, Oldfield E, Docampo R (Oct 2004). "Human platelet dense granules contain polyphosphate and are similar to acidocalcisomes of bacteria and unicellular eukaryotes". J Biol Chem. 279 (43): 44250–7. doi:10.1074/jbc.M406261200. PMID 15308650.
- ^ Müller F, Mutch NJ, Schenk WA, Smith SA, Esterl L, Spronk HM, Schmidbauer S, Gahl WA, Morrissey JH, Renné T (Dec 2009). "Platelet polyphosphates are proinflammatory and procoagulant mediators in vivo". Cell. 139 (6): 1143–56. doi:10.1016/j.cell.2009.11.001. PMC 2796262. PMID 20005807.
- ^ "Newly discovered mechanism by which blood clots form". physorg.com. December 10, 2009. Retrieved 13 December 2009.
- ^ Roewe J, Stavrides G, Strueve M, Sharma A, Marini F, Mann A, Smith SA, Kaya Z, Strobl B, Mueller M, Reinhardt C, Morrissey JH, Bosmann M (August 2020). "Bacterial polyphosphates interfere with the innate host defense to infection". Nature Communications. 11 (1): 4035. Bibcode:2020NatCo..11.4035R. doi:10.1038/s41467-020-17639-x. PMC 7423913. PMID 32788578.
- ^ Andreeva N, Ryazanova L, Dmitriev V, Kulakovskaya T, Kulaev I (Aug 2013). "Adaptation of Saccharomyces cerevisiae to toxic manganese concentration triggers changes in inorganic polyphosphates". FEMS Yeast Res. 13 (5): 463–470. doi:10.1111/1567-1364.12049. PMID 23663411.
- ^ 식품첨가물 및 향료에 관한 EFSA 패널 (FAF), 유네스, M, 아쿨리나, G, 캐슬, L, 엥겔, K. H, 파울러, P, ...&메네스, W. (2019) 식품 첨가물로서의 인산-인산-인산-di –di –, 3- 및 폴리인산(E 338–341, E 343, E 450–452)의 재평가 및 제안된 사용 연장의 안전성. EFSA 저널, 17(6), e05674.
- ^ 리츠, E, 한, K, 케텔러, M, Khlmann, M. K, & Mann, J. (2012) 식품 내 인산염 첨가물—건강 위험. 독일인 아레스테블라트 인터내셔널, 109(4), 49.
외부 링크
- Pavlov E, Grimbly C, Diao CT, French RJ (September 2005). "A high-conductance mode of a poly-3-hydroxybutyrate/calcium/polyphosphate channel isolated from competent Escherichia coli cells". FEBS Lett. 579 (23): 5187–92. doi:10.1016/j.febslet.2005.08.032. PMID 16150446. S2CID 35616647.
- Kulaev I, Vagabov V, Kulakovskaya T (1999). "New aspects of inorganic polyphosphate metabolism and function". J. Biosci. Bioeng. 88 (2): 111–29. doi:10.1016/S1389-1723(99)80189-3. PMID 16232585.
- Kulaev I, Kulakovskaya T (2000). "Polyphosphate and phosphate pump". Annu. Rev. Microbiol. 54: 709–34. doi:10.1146/annurev.micro.54.1.709. PMID 11018142.