페놀 포름알데히드 수지
Phenol formaldehyde resin
 | |
| 식별자 | |
|---|---|
| |
| 켐스파이더 |
|
| ECHA InfoCard | 100.105.516 |
CompTox 대시보드 (EPA) | |
달리 명시된 경우를 제외하고, 표준 상태(25°C [77°F], 100 kPa)의 재료에 대한 데이터가 제공된다. | |
| Infobox 참조 자료 | |
페놀 포름알데히드 레진(PF) 또는 페놀 레진(흔히 페노플라스틱이라고도[1] 불림)은 페놀 또는 대체 페놀의 반응에 의해 포름알데히드로 얻은 합성 폴리머다. Bakelite의 기초로 사용된 PF는 최초의 상업용 합성수지(플라스틱)이다. 당구공, 실험실 조리대, 코팅제 및 접착제 등 곰팡이 제품 생산에 널리 사용되어 왔다. 그것들은 한때 회로 기판 생산에 사용된 주요 재료였지만, 내화성 FR-4 회로 기판 재료와 마찬가지로 에폭시 수지 및 섬유 유리 천으로 대체되었다.
생산방법은 크게 두 가지가 있다. 하나는 페놀과 포름알데히드를 직접 반응시켜 보온망 중합체를 생산하고, 다른 하나는 포름알데히드를 제한하여 노볼락으로 알려진 전합체를 생산하는데, 이는 포름알데히드와 열이 더해져 성형한 후 경화시킬 수 있다.[2][3] 특수 목적의 다양한 레진을 생산하기 위해 사용되는 생산 재료와 입력 재료 모두 많은 변화가 있다.
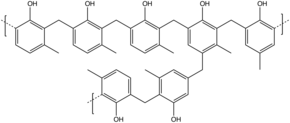
형성과 구조
페놀-포름알데히드 수지는 집단으로서 산이나 염기성분이 될 수 있는 단계 성장 중합반응에 의해 형성된다. 포름알데히드는 주로 메틸렌 글리콜 올리고머의 동적 평형으로서 용액에 존재하기 때문에 포름알데히드의 반응성 형태의 농도는 온도와 pH에 따라 달라진다.
페놀은 정형외과와 파라 부위(사이트 2, 4, 6)에서 포름알데히드와 반응해 최대 3단위의 포름알데히드가 링에 부착된다. 모든 경우에서 초기 반응은 히드록시메틸페놀의 형성을 포함한다.
- HOCH652 + CHO → HOCHCOH642
히드록시메틸 그룹은 다른 자유 정형외과 또는 파라 사이트 또는 다른 히드록시메틸 그룹과 반응할 수 있다. 첫 번째 반응은 메틸렌 다리를 주고, 두 번째 반응은 에테르 다리를 형성한다.
- 호치쵸우642 + 호치65 → (호치64)2CH2 + HO2
- 2 호치쇼642 → (호치642)2O + HO2
다이페놀(HOCH64)2CH2(때로는 "다이머"라고도 함)는 비스페놀 F라고 불리며, 에폭시 수지 생산에 있어 중요한 모노머다. 비스페놀-F는 3개 및 4개 이상의 페놀 과점 생성자를 추가로 연결할 수 있다.
노볼락스
노볼락(또는 노볼락)은 포름알데히드 대 페놀 어금니 비율이 1 미만인 페놀 포름알데히드 수지다. 페놀 그 자체 대신 크레졸(메틸페놀)에서 생산되는 경우가 많다. 중합은 황산, 옥살산, 염산과 같은 산-투석을 사용하여 완성되며, 드물게는 황산(sulfonic acid)[4]을 사용한다. 페놀 단위는 주로 메틸렌 및/또는 에테르 그룹에 의해 연결된다. 분자 중량은 약 10–20 페놀 단위에 해당하는 낮은 수천 단위에 있다. 획득된 폴리머는 열가소성 수지로 열가소성을 형성하기 위해 경화제 또는 경화제가 필요하다.
헥사메틸네테트라민은 크로스링크 노볼락에 첨가된 경화제다. 90 °C 이상의 온도에서 메틸렌과 디메틸렌 아미노 브리지를 형성한다. 분해능은 노볼락 레진을 위한 경화제(경화제)로도 사용할 수 있다. 어느 경우든 경화제는 노볼락 체인 사이의 다리를 제공하는 포름알데히드의 원천이며, 결국 시스템을 완전히 교차시킨다. [2]
노볼락은 타이어 태키퍼, 고온 레진, 탄소 결합 내화용 바인더, 탄소 브레이크, 포토레시스트 및 에폭시 레진용 경화제로서 여러 가지 용도가 있다.
리졸브
베이스 캐탈라이스 페놀 포름알데히드 레진은 포름알데히드 대 페놀 비율이 1(보통 1.5 정도) 이상이다. 이러한 수지를 Resolutions라고 부른다. 페놀, 포름알데히드, 물과 촉매가 형성되는 수지에 따라 원하는 양으로 혼합되어 가열된다. 반응의 첫 부분은 약 70°C에서 진한 적갈색 태키 소재를 형성하는데, 히드록시메틸과 벤질릭 에테르군이 풍부하다.
염기성 반응의 속도는 처음에는 pH와 함께 증가하며, 약 pH = 10으로 최대치에 도달한다. 반응성 종은 페놀의 감응에 의해 형성된 페노산화 음이온(CHO65−)이다. 음전하가 방향족 링 위에서 분해되어 사이트 2, 4, 6을 활성화하고 포름알데히드와 반응한다.
히드록시메틸페놀은 열분자 제거를 통해 메틸렌과 메틸에테르 다리를 형성하기 위해 약 120°C의 가열로 교차 연결된다. 이 시점에서 수지는 중합 페놀 수지의 대표적인 3차원 네트워크다. 높은 교차 연계는 이러한 유형의 페놀 수지의 경도, 우수한 열 안정성, 화학적 불침투성을 제공한다. 분해능은 '2단계' 수지인 노볼락과 달리 크로스 링커 없이 경화되면서 '1단계' 수지를 일컫는다.
리졸즈는 건축자재를 접착하고 접합하는 데 널리 사용되는 주요 고분자 수지 재료다. 외부 합판, 지향 스트랜드 보드(OSB), 엔지니어링된 적층 복합 목재(LCL)가 대표적인 응용 분야다.
교차 링크 및 포름알데히드/페놀 비
포름알데히드:페놀의 어금니 비율이 1에 도달하면 이론상 모든 페놀은 메틸렌 다리를 통해 서로 연결되어 하나의 분자를 생성하며, 시스템은 완전히 교차 연결된다. 노볼락(F:P <1)이 크로스링크제를 첨가하지 않고 경화되지 않는 이유, 그리고 F:P >1이라는 공식으로 해결되는 이유가 여기에 있다.
적용들
페놀 수지는 무수한 공산품에서 발견된다. 페놀 라미네이트는 종이, 섬유 유리 또는 면과 같은 하나 이상의 기본 물질 층을 페놀 수지로 담근 후 열과 압력 하에서 수지 포화 염기 물질을 라미네이트하여 만든다. 이 과정에서 수지는 열모셋 폴리머 매트릭스를 형성하는 완전 중합(고정)을 한다. 기본 재료 선택은 완제품의 의도된 용도에 따라 달라진다. 종이 페놀릭은 펀치 스루 보드, 가정용 라미네이트, 종이 복합 패널과 같은 전기 구성품을 제조하는 데 사용된다. 유리 페놀릭은 특히 고속 베어링 시장에서 사용하기에 적합하다. 페놀 마이크로 풍선은 밀도 조절에 사용된다. 일반(유기농) 브레이크 패드, 브레이크 슈 및 클러치 디스크의 결합제는 페놀 수지다. 페놀 수지와 종이로 만든 합성수지 보세지는 조리대를 만드는 데 사용된다. 페놀 수지의 또 다른 용도는 트라반트 자동차에 사용되는 듀로플라스트의 제작이다.
페놀 수지는 220°C(428°F) 이상의 온도 영역에서 녹는점이 없고 분해점만 있기 때문에 일반적으로 날씨와 끓는 방지(WBP) 합판으로 알려진 외부 합판을 만드는 데도 사용된다.
페놀 수지는 천으로 만들어진 확성기 드라이버 서스펜션 구성 요소에서 바인더로 사용된다.
더 비싼 당구공은 덜 비싼 세트에 사용되는 폴리머와는 반대로 페놀 레진으로 만들어진다.
때때로 사람들은 열팽창 계수가 초기 컴퓨터 시스템과[5] 듀라몰드에서와 같이 시스템의 다른 부분에 사용된 알루미늄과 밀접하게 일치하기 때문에 섬유 강화 페놀 수지 부품을 선택하기도 한다.
네덜란드의 한 반 메헤렌 화백은 완성된 캔버스를 굽기 전에 페놀 포름알데히드를 유화 물감과 섞어서 수세기에 걸쳐 페놀의 건조 상태를 위장했다.
상명
- 바켈라이트는 원래 페놀 수지와 나무 가루로 만들어졌다.
- 노보텍스트는 무작위 지향 섬유질을 사용하는 면 섬유 강화 페놀릭이다.
- 오아시스 플로럴 폼은 "물을 쉽게 흡수하는 오픈 셀 페놀 폼으로 꽃꽂이의 베이스로 사용된다"[6]고 설명했다.
- Paxolin은 많은 용도에서 섬유 유리 합성물로 대체되고 있지만 인쇄 회로 기판의 기본 재료로 오랫동안 사용되는 수지 접합 종이 제품이다.
- 투프놀(Tufnol)은 시트와 봉으로 사용할 수 있는 적층 플라스틱으로, 페놀 수지로 적신 후 열에 눌려 압착한 종이나 천을 겹겹이 쌓아 만든 것이다. 오일 및 용제에 대한 높은 저항성으로 인해 많은 엔지니어링 용도에 적합하게 되었다.[7]
- 에보놀(Ebonol)은 현악기와 목관악기의 에보니 목재를 대체하기 위해 고안된 종이로 채워진 페놀 수지다.
생물분해
페놀-포름알데히드는 흰색의 썩은 곰팡이 파네로차에테 번시스포륨에 의해 분해된다.[8]
참고 항목
참조
- ^ "Phenoplasts". polymerdatabase.com. Retrieved 13 June 2021.
- ^ a b A. Gardziella, L.A. Pilato, A. Knop, 페놀 레진스: 화학, 응용, 표준화, 안전 및 생태학, 제2판, 스프링거, 2000
- ^ 볼프강 헤세 "페놀릭 레진스" 2002년 울만 산업 화학 백과사전, Wiley-VCH, Weinheim. doi:10.1002/14356007.a19_371.
- ^ Ralph Dammel (1993). "Basic Chemistry of Novolaks". Diazonaphthoquinone-based Resists. Int. Soc. Optical Engineering. ISBN 9780819410191.
- ^ J. G. 퍼거슨, W. E. 그루츠너, D. C. 쾰러, R. S 스키너, M. T. 스쿠비악, D. H. Wetherll. 「1번 ESS 장비·장비」. 벨 시스템 기술 저널. 1964. 페이지 2417.
- ^ "Smithers Oasis Resource Center". Archived from the original on 7 April 2008. Retrieved 21 October 2010.
- ^ Godwin, R. (April 2015). "What is Tufnol?". ahistoryoftufnol.org.
- ^ Gusse AC; Miller PD; Volk TJ (July 2006). "White-rot fungi demonstrate first biodegradation of phenolic resin". Environmental Science and Technology. 40 (13): 4196–9. Bibcode:2006EnST...40.4196G. doi:10.1021/es060408h. PMID 16856735.