맨헤스-다비드 과정
Manhès–David process본 기사는 해당 기사에서 프랑스어로 번역된 텍스트로 전개될 수 있습니다. (2017년 8월) 중요 번역 지침은 [show]를 클릭해 주세요.
|
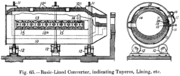
Manhés-David 공정은 1880년 프랑스 사업가 Pierre Manhés와 그의 엔지니어 Paul [fr] David에 의해 발명된 구리 매트의 정제 공정입니다.베세머 공정에서 영감을 얻어 변환기를 사용하여 무광에 포함된 바람직하지 않은 화학 원소(주로 철과 유황)를 공기로 산화시켜 구리로 변환합니다.
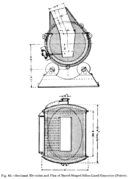
산화되는 원소의 양과 화학 반응에 의해 생성되는 낮은 열은 변환기의 플라스틱 변형을 초래합니다.Manhés와 David은 그것을 수평 실린더로 디자인했고, 한쪽 끝에서 다른 쪽 끝까지 노즐이 정렬되었다.몇 년 후, 미국인 기술자 윌리엄 H. 피어스와 엘리아스 안톤 카펠렌 스미스는 프랑스 발명가들이 사용한 것보다 훨씬 더 내구성이 좋은 기본적인 내화재들로 그것을 배열했다.이 개선으로 공정의 원칙이 바뀌지는 않지만, 널리 사용되기 쉬워져 영국에서 미국으로의 구리 생산 전환을 가속화할 수 있습니다.
21세기 초에 피어스-스미스 변환기는 [fr] 구리 매트의 90%를 정제하여 추출한 니켈의 60%에 사용됩니다.이 변환기는 순수한 산소의 첨가, 작동의 자동화, 연기 처리 및 도구의 크기 증가 등과 같이, 현대 도구들이 그들의 조상들과 거의 관련이 없는 경우에도 Manhés-David 공정의 내구성을 보장했습니다.
프로세스의 기원
Besemer 프로세스와의 관계
용광로에서 생산된 철이 다른 화학 원소와 합금되어 주철로 나오듯이, 광석에서 추출된 구리는 무광이라고 불리는 유황, 철 등과 합금이 됩니다.따라서 이 두 금속에 동일한 정제 과정을 적용하는 것이 타당하다.베세머 공정을 구리 야금에 적용하는 것이 제안되었고, 헨리 베세머가 발명된 지 10년 후인 1866년에 러시아 기술자 세메니코프에 [2]의해 그 원리가 검증되었습니다.
변환기에서 합금의 정교화는 바람직하지 않은 원소의 연소가 강하게 발열되기 때문에 가능합니다. 실리콘과 카본의 산화는 [3]각각 kg당 32.8 킬로줄과 10.3킬로줄을 생성합니다.한편 구리 무광에 철분과 황이 풍부하게 함유되어 있는 경우 산화([4][5]각각 5.9kJ/kg 생성)를 시작하기 전에 이들 원소를 분리(kg당 6.8킬로줄 소비)해야 한다.
첫 번째 시도
변환기에 의한 구리 합금의 첫 번째 정제 작업은 테네시 주 덕타운에서 이루어졌으며, 이 곳에서 A.Raht는 1866년부터 1875년까지 무광의 부분적인 정제 작업을 했다.1867년 러시아인 조사와 라틀린은 세메니코프의 연구를 실험적으로 검증하려고 했다.1870년에 그들은 구리 함량을 31%에서 72-80%[4]로 증가시키는 데 성공한 후 실험을 중단했다.
영국에서, 존 홀웨이는 [6][7]1878년까지 이러한 재판을 계속했다.전임자들과 마찬가지로, 그는 바람이 만족스럽게 불기 시작하면, 정제 작업이 진행되면서 점점 더 간헐적으로 불게 된다고 관찰했다.그가 마주친 장애물은 [2]수없이 많았다.
- 생산된 슬래그의 무게는 구리 무게와 같았으며 슬래그의 부피는 변환기의 부피보다 훨씬 더 컸습니다.따라서 정기적으로 응수할 필요가 있었다.
- 용융 금속의 밀도는 크게 변화했습니다(구리는 황철광의 3배 밀도가었습니다).
- 2시간에 이르는 공기 분사 시간은 큰 열 손실을 수반했습니다.
- 규소성 내화재는 슬래그에 흡수되어 플럭스 역할을 했습니다.
구리 공기 중 정제 반응의 열 균형은 철만큼 좋지 않았고,[5] 정제되기 전에 광택이 튜이어에 고화된 것 등 모든 어려움을 쉽게 해결할 수 없었습니다.베세머 변환기는 개조하더라도 철분과 [8]유황의 일부를 제거할 수 있습니다.홀웨이는 실패했지만, 그의 실험의 모든 세부사항을 발표함으로써,[9] 그는 본질적인 문제들을 밝혀냈다.
측두엽
1870년대에 프랑스 사업가 피에르 맨에스는 베덴에 있는 자신의 공장에서 50kg의 작고 평범한 베세메르 변환기로 첫 시도를 시작했고, 그 후 아비뇽 [5]근처에 있는 에길레에 있는 공장에서 그의 첫 시도를 시작했다.그는 이전에 도가니에 녹인 25~30%의 구리로 무광택을 정제하려고 했다.하지만 홀웨이와 마찬가지로, 그는 무광택을 완전히 다듬는 데 성공하지 못했다.바람직하지 않은 원소의 산화는 예상대로 일어났지만, 금속 [10]구리의 출현으로 인해 작동이 빠르게 중단되었다.이온 화합물인 무광은 슬래그와 용해된 금속과 함께 용해되지 않았습니다.후자는 밀도가 더 높았고copper(≈≈), 9), 변환기[11] 바닥으로 가서 관을 막았다.
피에르 맨에스는 그 후 산화 작용으로 막히지 않도록 충분한 열을 방출하는 첨가제의 사용 특허를 취득했다.결국, 해결책을 제안한 사람은 1880년 당시 그의 공장의 엔지니어였던 프랑스인 폴 데이비드였다.그는 변환기 바닥에서 충분한 거리에 수평 송곳니를 배치하여 구리가 그 아래로 모이고 공기가 지속적으로 무광으로 방출되도록 할 것을 제안했다.1881년까지, 그들의 변환기는 기술적으로 작동 가능하고 비용 효율적이었습니다.
1884년 가을,[6] 그 과정은 몬태나주 부트에 있는 패럿 실버 앤 구리 회사에 의해 미국에서 채택되었다.1912년 1톤에서 [2]8톤, [8]1920년에는 15톤으로 늘어나면서 두 종류가 점점 더 커졌다.
1920년 Anaconda Coopper의 Washoe 공장에서 Peirce-Smith가 변환합니다.용량은 구리 매트 65톤으로, 3시간(백금속) + 1시간 45분(블리스터)에 송풍됩니다.컨버터의 모양은 그레이트 폴스 타입입니다.
Peirce 및 Smith에 의한 개선
슬래그는 공기 중에 반응하는 동안 산화철로 농축되면 염기성이 되어 매우 [2]산성인 규소성 내화 라이닝과 결합합니다.기본적인 내화 라이닝은 반응하지 않기 때문에 생산 비용을 낮출 수 있습니다.1877년 시드니[12] 토마스와 퍼시 길크리스트가 개발한 안감의 채택은 1800년대 [2]초 홀웨이의 마지막 테스트에서 제안되었다.그러나 공기 송풍과 관련된 근본적인 문제가 내화성 [6]최적화보다 더 큰 문제였기 때문에 이 아이디어는 테스트되지 않았습니다.
1890년, 버트에 있는 패럿 제련소의 Manhés-David 컨버터 중 하나에 Herman A의 지시로 기본적인 내화 라이닝이 테스트되었습니다.켈러입니다.테스트 결과 라이닝은 산업용 [2]작동과 양립할 수 없었습니다.1906년, 여전히 몬태나에 있는 Ralph Baggaley는 여러 번의 테스트 끝에 피트몬트 제련소의 기본 코팅의 공업화에 성공했습니다. 피트몬트 제련소는 1908년 [9]그가 공장을 떠난 후 버려졌습니다.그 후 노르웨이 쿠센은 1908년 현재 술리트젤마 광산의 기초 도료를 사용하는 데 성공했다.그는 그곳에서 두 번의 블로우(blow)를 연속으로 수행했는데,[2] 처음에는 기본 코팅이 적용된 소형 컨버터, 다음에는 산성 코팅이 적용된 두 번째 기존 컨버터였습니다.
마침내 1909년 [13][14]볼티모어 구리 회사의 제련소에서 미국인 윌리엄 H. 피어스와 엘리아스 A.C.가 있었다.Smith는 기본 내화재의 주요 단점을 해결하는 데 성공했습니다. 기본 내화재는 더 취약했고 무엇보다도 산성 [2]내화물보다 더 많은 열을 방출했습니다.원통형 컨버터에 적합한 석재를 개발하고 용해로에 공급되는 금속의 양을 늘림으로써 나머지 [2]문제를 해결했습니다.
피어스와 스미스의 컨버터는 맨헤스와 데이빗의 컨버터보다 훨씬 유리했다.슬래그와 반응하지 않는 기본 내화물은 훨씬 더 오래 지속되었습니다.이러한 개선으로 변환기 교체, 석조 [2]설비 건설 및 변환기 교체의 필요성이 없어졌습니다(Anaconda[15] Copper에서는 1897년에 각 변환기마다 2개의 석조 변환기가 사용되었습니다).또한 내화물 [6]마모 제어 불량으로 인한 피어싱 위험도 감소했습니다.그러면 내화층이 얇아져 변환기의 용량이 증가할 수 있습니다.용량은 내화물 마모에 의존하지 않으므로 공장에서 [2]용해된 금속의 흐름 관리를 단순화할 수 있습니다.
내산성 내화물을 제조하는 데 사용되는 재료에 구리 또는 은 또는 금(흔히 금 함유 석영[16] 내 구리와 관련됨)이 포함되어 있는 경우, 이러한 금속은 라이닝이 제거될 때 무광 접합됩니다.따라서 내화물의 빠른 파괴를 고려할 때 산성 내화물의 소비량이 공정의 [2]가치를 높여야만 경제적 이점을 실현할 수 있습니다.그러나 이러한 상황은 다소 드물고, 비록 그렇다 하더라도, 귀금속이 풍부한 실리카는 경제적으로 실현 가능한 다른 방법으로 만들어질 수 있다.따라서 1921년에는 기본 내화물이 구리 [17]광석 추출 비용 절감의 주요 요인으로 간주되었습니다.어떤 경우에는 전환 비용이 15-20달러에서 4-5달러로 감소했다고 [18]보고되었다.
구리 야금에서의 변환
무광으로 불리는 구리와 황화철의 혼합물을 변환기로 처리하여 제1단에서는 철을 산화시키고, 제2단에서는 구리를 산화시킨다.1단계에서는 산소 농축 공기가 송풍관을 통해 금속 황화물을 부분적으로 산화물로 변환합니다.
- FeS + O2 → FeO + SO2
- CuS + O2 → CuO + SO2
철은 산소에 대한 친화력이 높기 때문에 생성된 산화동은 나머지 황화철과 반응합니다.
- CuO + FeS → CuS + FeO
산화구리 대부분은 다시 황화물 형태로 변한다.얻은 산화철을 분리하기 위해 변환기에 플럭스(주로 실리카)를 첨가한다.실리카는 산화철과 반응하여 가벼운 슬래그상을 생성합니다. 이 슬래그는 컨버터가 회전 축을 중심으로 기울어지면 후드를 통해 쏟아집니다.
- 2 FeO + SiO2 → FeSiO24 (2FeO·SiO2, 페야라이트라고도 함)
슬래그 제1부분을 컨버터에서 주입한 후 무광의 새로운 부분을 첨가하여 정제된 황화동기가 충전될 때까지 변환 동작을 여러 번 반복한다.변환기 슬래그는 일반적으로 이 부산물에 구리 함량이 높기 때문에 제련 단계로 재활용됩니다.변환기 가스는 이산화황의 10% 이상을 함유하고 있으며, 이는 보통 황산 생산을 위해 회수됩니다.
변환의 2단계는 황화구리상(정제1단계)을 산화시키는 것을 목적으로 하며, 물집동이를 생성한다.컨버터에서는 다음과 같은 반응이 발생합니다.
- CuS + O2 → Cu + SO2
얻어진 블리스터 구리 중 구리 함량은 일반적으로 95% 이상입니다.블리스터 구리는 변환의 최종 산물이다.
레퍼런스
- ^ Coleman, Arthur Philemon (1913). The nickel industry; with special reference to the Sudbury region, Ontario. Ottawa Government Printing Bureau. pp. 143–144.
- ^ a b c d e f g h i j k l Levy, Donald M. (1912). Modern copper smelting. Being lectures delivered at Birmingham university greatly extended and adapted, and with an introduction on the history, uses and properties of copper. University of California Libraries. London, C. Griffin & company, limited.
- ^ Ledebur, Adolf (1895). Manuel théorique et pratique de la métallurgie du fer (in French). Paris: Librairie polytechnique Baudry et Cie. p. 472. ISBN 1272776794.
- ^ a b Hofman, H. O. (Heinrich Oscar) (1914). Metallurgy of copper. New York Public Library. New York [etc.] McGraw-Hill book company, inc.
- ^ a b c Paul Weiss (1894). Le cuivre: origine, propriétés, applications (in French). University of California. J.B. Baillière & Fils.
- ^ a b c d Peters, Edward Dyer (1905). Modern copper smelting. University of California Libraries. New York, London : Engineering and mining journal.
- ^ US 234129, Holway, John, "황, 구리-매트, &c.의 생산, 황철광으로부터의 생산", 1880-11-09 출판
- ^ a b Société de l'industrie minérale (France) (1855). Bulletin (in French). Harvard University. Saint-Étienne [etc.
- ^ a b Southwick, Larry M. (2008). "William Peirce and E.A. Cappelen Smith and their amazing copper converting machine". JOM. 60 (10): 24–34. Bibcode:2008JOM....60j..24S. doi:10.1007/s11837-008-0131-y. ISSN 1047-4838. S2CID 110248998.
- ^ Ouvrard, Léon Victor René (1896), Le Nickel, Gauthier-Villars et fils, Masson et Cie, pp. 56–117, retrieved 8 December 2020
- ^ "Pyrométallurgie". Techniques de l'Ingénieur (in French). Retrieved 8 December 2020.
- ^ Wedding, Hermann (1891). Wedding's Basic Bessemer Process. Wedding's Basische Bessemer oder Thomas process.English. Translated by Phillips, William; Prochaska, Ernst. New York Scientific Publishing Company. hdl:2027/wu.89074785106.
- ^ Bustos, Alejandro Alberto (1984). Injection phenomena and heat transfer in copper converters (Thesis). University of British Columbia.
- ^ US 942346, Peirce, William H. & Smith, Elias A. C., "구리의 무광택을 맞춤화하는 방법 및 변환기 용기", 1909-12-07년 발행
- ^ Anaconda Company (1897). Catalogue no. 1, presented by the Anaconda Copper Mining Co., foundry department, manufacturers of mining, milling, concentrating and smelting machinery. Anaconda Copper Mining Co., foundry department. Anaconda, Montana: The Company.
- ^ "Analysis of Jawbone Flats Mine Dump Samples". people.wou.edu. Retrieved 9 December 2020.
- ^ Mueller, W. A. (November 1921). "Progressive Steps In the Metallurgy of Copper". Ohio State Engineer. 5: 11–13, 21.
- ^ Bjork, Kenneth O. (1947). Saga in Steel and Concrete: Norwegian Engineers in America. Norwegian-American Historical Association. ISBN 9780877320289.