HBTU
HBTU | |
| 이름 | |
|---|---|
| IUPAC 이름 3-[비스(디메틸아미노)메틸리아실]-3H-벤조트리아졸-1-옥시드헥사플루오로인산 | |
| 기타 이름 HBTU | |
| 식별자 | |
3D 모델(JSmol) | |
| 켐스파이더 | |
| ECHA 정보 카드 | 100.133.815 |
| EC 번호 |
|
PubChem CID | |
| 유니 | |
CompTox 대시보드 (EPA ) | |
| |
| |
| 특성. | |
| C11H16F6N5OP | |
| 몰 질량 | 379.247 g/120−1 |
| 외모 | 백색 결정 |
| 녹는점 | 200 °C (392 °F, 473 K) |
| 위험[1] 요소 | |
| 산업안전보건(OHS/OSH): | |
주요 위험 요소 | 자극성 |
| GHS 라벨링: | |
 | |
| 경고 | |
| H315, H319, H335 | |
| P210, , , , , , , , , , , , , , , , | |
달리 명시되지 않은 한 표준 상태(25°C[77°F], 100kPa)의 재료에 대한 데이터가 제공됩니다. | |
HBTU(2-(1H-벤조트리아졸-1-일)-1,1,3,3-테트라메틸루늄헥사플루오로인산벤조트리아졸테트라메틸우로늄)는 고체상펩타이드 합성에 사용되는 결합시약이다.1978년에 도입되어 라세미화에 [2][3]대한 저항을 나타내고 있다.가벼운 활성화 [4]특성 때문에 사용됩니다.
HOBt와 테트라메틸클로로늄염(TMUCl)의 반응으로 얻은 생성물은 우로늄형 구조에 할당되었으며, 아마도 포스포늄 잔기 대신 양의 탄소 원자를 가진 대응하는 포스포늄염과 유추하여 할당되었다.이후 X선 분석 결과 염분이 해당 우로늄염이 [5][6]아닌 아미늄으로 결정되는 것으로 나타났다.
메커니즘
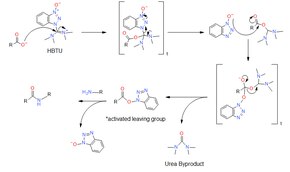
HBTU는 안정화 HOBt(Hydroxybenzotriazole) 이탈기를 형성하여 카르본산을 활성화한다.아미노분해 중에 아민에 의해 공격된 활성 중간 종은 HOBt 에스테르이다.
HOBt에스테르를 생성하기 위해 산의 카르복실기가 HBTU의 이미드 카르보닐 탄소를 공격하고 이어서 치환된 음이온성 벤조트리아졸 N-옥시드를 공격하여 테트라메틸 요소 부산물과 활성 에스테르를 얻는다.아미노분해는 벤조트리아졸 N-옥시드를 치환하여 원하는 아미드를 [7]형성한다.
「 」를 참조해 주세요.
레퍼런스
- ^ "2-(1h-Benzotriazole-1-yl)-1,1,3,3-tetramethyluronium hexafluorophosphate". pubchem.ncbi.nlm.nih.gov.
- ^ Dourtoglou, Vassilis. (April 1978). "L'hexafluorophosphate de O-benzotriazolyl-N,N-tetramethyluronium: Un reactif de couplage peptidique nouveau et efficace". Tetrahedron Letters. 19 (15): 1269–1272. doi:10.1016/0040-4039(78)80103-8.
- ^ Knorr, R.; Trzeciak, A.; Bannwarth, W.; Gillessen, D. (1989). "New coupling reagents in peptide chemistry". Tetrahedron Letters. 30 (15): 1927–1930. doi:10.1016/S0040-4039(00)99616-3.
- ^ Solange, A. (1992). "HBTU: a mild activating agent of muramic acid". Bioorganic & Medicinal Chemistry Letters. 2 (6): 571–574. doi:10.1016/S0960-894X(01)81199-9.
- ^ Carpino, L.; Imazumi, H.; El-Faham, A.; Ferrer, F.; Zhang, C.; Lee, Y.; Foxman, B.; Henklein, P.; Hanay, C.; Mügge, C.; Wenschuh, H.; Klose, J.; Beyermann, M.; Bienert, M. (2002). "The uronium/guanidinium peptide coupling reagents: Finally the true uronium salts". Angewandte Chemie International Edition. 41 (3): 441–445. doi:10.1002/1521-3773(20020201)41:3<441::AID-ANIE441>3.0.CO;2-N. PMID 12491372.
- ^ Abdelmoty, I.; Albericio, F.; Carpino, L.; Foxman, B.; Kates, S. (1994). "Structural studies of reagents for peptide bond formation: Crystal and molecular structures of HBTU and HATU". Letters in Peptide Science. 1 (2): 57–67. doi:10.1007/BF00126274. S2CID 38746650.
- ^ Bradley, Mark; Valeur, Eric (2009-01-26). "Amide bond formation: beyond the myth of coupling reagents". Chemical Society Reviews. 38 (2): 606–631. doi:10.1039/B701677H. ISSN 1460-4744. PMID 19169468.