컬리
Curli| 컬리 분비 통로 | |||||||
|---|---|---|---|---|---|---|---|
 | |||||||
| 식별자 | |||||||
| 유기체 | |||||||
| 기호 | CsgG | ||||||
| 엔트레스 | 945619 | ||||||
| PDB | 3X2R | ||||||
| RefSeq(mRNA) | NC_000913.3 | ||||||
| RefSeq(프로토콜) | NP_415555.1 | ||||||
| 유니프로트 | P0AEA2 | ||||||
| 기타자료 | |||||||
| 염색체 | 게놈어: 1.1 - 1.1Mb | ||||||
| |||||||
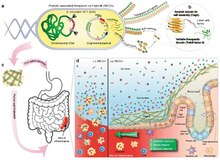
컬리 단백질은 특정 종류의 엔토박테리아에 의해 생산되는 아밀로이드 섬유질의 일종이다. 대장균이나 살모넬라 같은 박테리아에 위치한 세포외 섬유다.[2] 이 섬유들은 세포외 매트릭스에서 바이오필름 형성을 통해 세포 공동체 행동을 촉진하는 역할을 한다. 아밀로이드는 알츠하이머병과 같은 인간의 신경퇴행성 질환과 관련이 있다.[3] 컬리에 대한 연구는 부적절한 아밀로이드 섬유 형성으로 인해 발생하는 인간의 질병을 이해하는 데 도움이 될 수 있다.[2] 컬리필리는 일반적으로 세포외 핵/초기화 경로를 통해 조립된다.[4]
유전자 조절
컬리 섬유, 즉 컬리 단백질은 두 개의 연산자인 csgB에 의해 코딩된다.AC와 csgDEFG 피연산자, 총 7개의 유전자를 포함하고 있다.[5][6] csgBAC 피연산자는 세 가지 단백질 CsgB, CsgA 및 CsgC의 코딩을 담당하며, 모두 컬리 섬유 내 주요 서브 유닛 형성을 담당하거나 이를 억제한다.[6] 컬리 단백질의 조립, 변환 및 조절을 담당하는 CsgD, CsgE, CsgF 및 CsgG 단백질에 대한 CsgDEFG 피연산자 코드.[6]
CsgD는 CsgBA 피연산자의 양전사 조절기다. CsgD 단백질은 전사 조절기로서 CsgBA 피연산자를 긍정적으로 조절하지만 그 자체의 표현을 조절하지는 않는다. CsgBA 피연산자는 핵분열기 단백질 CsgB뿐만 아니라 Curli의 주요 구조 하위 단위인 CsgA를 인코딩한다. CsgD 표현이나 활동을 자극하는 것이 무엇인지를 알기 위해서는 추가 연구가 여전히 진행되어야 하지만, 일부 증거는 단백질의 활성화가 N-단자 수신기 영역의 아스파르트산 잔류물의 인산화 때문에 발생한다는 것을 뒷받침한다. CsgD는 CsgBA 추진자 활동을 위해 존재해야 하므로, 따라서 CsgD 표현 규제자들은 CsgBA의 표현에도 영향을 미친다는 것이 보여진다.[2]
많은 환경적인 단서들이 컬리 유전자 발현에 역할을 한다. 섭씨 30도 이하의 온도에서 성장하면 컬리 유전자 발현이 촉진된다.[2] 또한 질소, 인산염, 철분 등 염분과 영양소가 부족할 때 컬리 유전자 발현이 자극된다.[2]
함수
아밀로이드는 알츠하이머, 파킨슨병, 헌팅턴병, 루푸스와 같은 질병과 연관되어 있다.[7][8] 덧붙여 컬리 단백질은 PAMP(병원성 관련 분자 패턴)로 간주되어 컬리의 베타 시트 구조가 선천적인 면역체계에 작용하여 TLR2(톨라이크 수용체 2)를 활성화시킨다.[7] 그 후, 소염증 시토카인과 화학물질을 개시 및 염증 반응을 위해 모집하는 소염 반응을 생성하여 다운스트림 반응을 일으킨다.[7]
그러나 컬리는 대장균, 살모넬라 등 그램 음성 박테리아에 의해 생성되는 바이오필름의 주요 성분이 되는 등 다른 기능('기능성 아밀로이드'[8]로 만들어진다)을 갖고 있다.[9][7][8] 이러한 바이오필름들은 그램 음성 박테리아가 주어진 환경에서 더 잘 식민지화하여 산화 스트레스와 탈수로부터 그들을 보호해준다.[9][7] 그러나 이 생물 영화들은 많은 우려를 필요로 한다. 이러한 바이오필름은 박테리아가 환경 내에서 화학적, 물리적 스트레스 요인을 견뎌낼 수 있도록 해주기 때문에 공유기기를 사용할 때 환자가 감염되기 쉽도록 만들 뿐만 아니라 Curli와 다른 바이오필름은 감염된 개개인의 면역반응과 항균작용을 감소시키는 것을 보여주었다.[9] 컬리 단백질과 바이오필름 모두 컬리가 도데실황산나트륨(SDS)에서 분해하거나 용해되기 위해서는 보다 강력한 전처리가 필요할 정도로 화학적 스트레스 요인에 대한 내성이 매우 강하다.[9]
구조
컬리 단백질의 주요 성분(하위닛)은 CsgA와 CsgB 단백질로 구성된다.
CsgA
CsgA는 13.1킬로달튼의 컬리 단백질의 주요 서브단위다. 이 단백질은 아밀로이드 섬유질, 단일 펩타이드, 22개의 아미노산 N 단자 염기서열(분비에 사용) 및 C-단자 염기서열에서 아밀로이드 코어 도메인을 형성하는 경향이 있는 3개의 영역으로 구성되어 있다.[9][8] 또한 아밀로이드 코어 영역은 시퀀스를 중심으로 회전하는 5개의 반복(정확하지 않은) 시퀀스, 즉 Ser-X-Gln-X-Gly-Asn-Ala-X-Gln으로53 구성된다.[8] 이 반복 시퀀스는 집계 가능한 β-시트를 구성하는 특성 서브 유닛이다.[8]
CsgB
CsgB는, 마이너 서브 유닛으로도 알려져 있으며, 세포 표면의 컬리 섬유로 CsgA의 핵화 및 조직화를 위해 필요하다.[7] CsgB는 5개의 반복 시퀀스 중 하나가 Lys133, Arg140, Arg14, Arg151로 알려진 추가 아미노산을 포함하고 있다는 예상과 함께 CsgA와 매우 유사한 반복 시퀀스를 가지고 있다.[9] 최종 서브 유닛(R5 서브 유닛으로 알려져 있음)의 이러한 변경이 필요하다. R5 서브유닛의 존재 또는 서브유닛 내부의 변화가 없으면 CsgA는 세포 표면에서 적절하게 형성될 수 없다.[9][8]
CsgC
CsgC 서브유닛은 최근에야 CsgA 단백질의 집적과 중합화를 방지하기 위해 발견되었다. 그것이 없다면, 아밀로이드 피브릴 형성과 궁극적인 세포 사망의 가능성이 있다.[7] CsgC를 CsgA 및 CsgB 하위 유닛에서 분리하는 여러 실험은 CsgA가 섬유질로 응집하도록 유발하며, 따라서 알츠하이머병과 같은 질병에 대한 다운스트림 효과로 이어질 수 있다.[9] CsgC가 CsgA를 억제하는 데 필요한 어금니 비율은 1:500이므로, 500 CsgA 단백질이 아밀로이드 피브릴 구조를 형성하는 것을 억제하는 데는 1 CsgC 단백질만 필요하다.[9][10] 따라서 CsgC는 더 이상의 CsgA 핵화를 방지하고 오히려 CsgA가 집적하는 대신 적절한 구조로 형성되도록 하기 때문에 CsgC를 보호자로 간주한다는 가설이 있다.[9]
참조
- ^ Praveschotinunt P, Duraj-Thatte AM, Gelfat I, Bahl F, Chou DB, Joshi NS (December 2019). "Engineered E. coli Nissle 1917 for the delivery of matrix-tethered therapeutic domains to the gut". Nature Communications. 10 (1): 5580. doi:10.1038/s41467-019-13336-6. PMC 6898321. PMID 31811125.
- ^ a b c d e Barnhart MM, Chapman MR (2006). "Curli biogenesis and function". Annual Review of Microbiology. 60: 131–47. doi:10.1146/annurev.micro.60.080805.142106. PMC 2838481. PMID 16704339.
- ^ Chapman MR, Robinson LS, Pinkner JS, Roth R, Heuser J, Hammar M, et al. (February 2002). "Role of Escherichia coli curli operons in directing amyloid fiber formation". Science. 295 (5556): 851–5. Bibcode:2002Sci...295..851C. doi:10.1126/science.1067484. PMC 2838482. PMID 11823641.
- ^ Hammar M, Bian Z, Normark S (June 1996). "Nucleator-dependent intercellular assembly of adhesive curli organelles in Escherichia coli". Proceedings of the National Academy of Sciences of the United States of America. 93 (13): 6562–6. doi:10.1073/pnas.93.13.6562. PMC 39064. PMID 8692856.
- ^ Van Gerven N, Klein RD, Hultgren SJ, Remaut H (November 2015). "Bacterial amyloid formation: structural insights into curli biogensis". Trends in Microbiology. 23 (11): 693–706. doi:10.1016/j.tim.2015.07.010. PMC 4636965. PMID 26439293.
- ^ a b c Tursi SA, Tükel Ç (December 2018). "Curli-Containing Enteric Biofilms Inside and Out: Matrix Composition, Immune Recognition, and Disease Implications". Microbiology and Molecular Biology Reviews. 82 (4): e00028–18, /mmbr/82/4/e00028–18.atom. doi:10.1128/MMBR.00028-18. PMC 6298610. PMID 30305312.
- ^ a b c d e f g Tursi SA, Tükel Ç (December 2018). "Curli-Containing Enteric Biofilms Inside and Out: Matrix Composition, Immune Recognition, and Disease Implications". Microbiology and Molecular Biology Reviews. 82 (4): e00028–18, /mmbr/82/4/e00028–18.atom. doi:10.1128/MMBR.00028-18. PMC 6298610. PMID 30305312.
- ^ a b c d e f g Evans ML, Chapman MR (August 2014). "Curli biogenesis: order out of disorder". Biochimica et Biophysica Acta (BBA) - Molecular Cell Research. 1843 (8): 1551–8. doi:10.1016/j.bbamcr.2013.09.010. PMC 4243835. PMID 24080089.
- ^ a b c d e f g h i j Van Gerven N, Klein RD, Hultgren SJ, Remaut H (November 2015). "Bacterial amyloid formation: structural insights into curli biogensis". Trends in Microbiology. 23 (11): 693–706. doi:10.1016/j.tim.2015.07.010. PMC 4636965. PMID 26439293.
- ^ Evans ML, Chorell E, Taylor JD, Åden J, Götheson A, Li F, et al. (February 2015). "The bacterial curli system possesses a potent and selective inhibitor of amyloid formation". Molecular Cell. 57 (3): 445–55. doi:10.1016/j.molcel.2014.12.025. PMC 4320674. PMID 25620560.
추가 읽기
- Dema B, Charles N (January 2016). "Autoantibodies in SLE: Specificities, Isotypes and Receptors". Antibodies. 5 (1): 2. doi:10.3390/antib5010002. PMC 6698872. PMID 31557984.
- Gallo PM, Rapsinski GJ, Wilson RP, Oppong GO, Sriram U, Goulian M, et al. (June 2015). "Amyloid-DNA Composites of Bacterial Biofilms Stimulate Autoimmunity". Immunity. 42 (6): 1171–84. doi:10.1016/j.immuni.2015.06.002. PMC 4500125. PMID 26084027.
- Kono DH, Baccala R, Theofilopoulos AN (December 2013). "TLRs and interferons: a central paradigm in autoimmunity". Current Opinion in Immunology. 25 (6): 720–7. doi:10.1016/j.coi.2013.10.006. PMC 4309276. PMID 24246388.
- Tursi SA, Lee EY, Medeiros NJ, Lee MH, Nicastro LK, Buttaro B, et al. (April 2017). "Bacterial amyloid curli acts as a carrier for DNA to elicit an autoimmune response via TLR2 and TLR9". PLOS Pathogens. 13 (4): e1006315. doi:10.1371/journal.ppat.1006315. PMC 5406031. PMID 28410407.