폴리셀레니드
Polyselenide화학에서 폴리셀렌화물은 보통 공식(Sen)의 음이온을 가리키는데,2- 여기서 세는 셀레늄 원소의 원자 기호다.많은 주요 그룹과 전이 금속은 폴리셀렌화 음이온과 함께 콤플렉스를 형성한다.[1]
준비
개념적으로 폴리셀렌화물은 탈화폴리셀렌즈 HSe에2n 의해 유도되지만, 그러한 종은 드물거나 불안정하다.대신에 많은 진틀 이온의 준비와 유사하게 폴리셀렌화물은 알칼리 금속으로 원소 세의 감소에 의해 생성된다.이러한 반응은 고체의 혼합물을 가열하거나 알칼리 금속의 아민 용액에 세 금속을 용해하는 방법으로 수행될 수 있다.합성은 또한 DMF, HMPA, NMP와 같은 고화질 극성의 무화합 용매에서도 수행될 수 있다.[2] 이러한 반응은 알칼리 금속 셀레니드의 초기 포뮬레이션에 의해 진행되며, 셀레늄이 추가된 후 후자의 반응에 따라 다음과 같이 나타난다.
- 2 Na + Se → NaSe2
- NaSe2 + n Se → NaSe2n+1
알칼리 금속 폴리셀렌화물은 일단 생성되면 암호화된 리간드를 처리하거나 쿼트염과 이온 교환을 통해 지방질 염으로 변환할 수 있다.[3]
- NaSe2n + 2 RNCl4 → (RN4)2Sen + 2 NaCl
구조물들
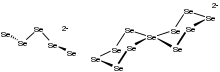
폴리셀렌화물의 염분은 종종 X선 결정술로 특징지어진다.폴리셀레니데스 염은 일반적으로 지그재그 순응을 채택하는 오픈 체인을 특징으로 한다.드물지만, 평방형 평면 세 중심이 특징인 LiSe에서와25 같이 순환 구조가 관찰된다.[NMe4]2의6 고해상도 솔리드 스테이트 Se NMR 스펙트럼 세 가지 셀레늄 부지를 보여준다.두 염류의 단결정 X선 구조 결정은 NMR 데이터를 지원한다.[4]
반응도
폴리셀렌화물은 공기에 노출될 때 분해되기 쉬우며, 이 경우 다시 원소 셀레늄으로 산화된다.
- SE2−
n + 2H+ +1⁄22 O → n Se + HO2
조정 콤플렉스에서 리간드처럼 폴리셀레니드는 일반적으로 바이덴산이다.펜타-, 테트라-, 트리셀레니드 리간드의 복합체가 알려져 있다.한 예는 스피로사이클릭 [Zn(Se4)]22-[5]이다.
추가 읽기
- Graf, Christian; Assoud, Abdeljalil; Mayasree, Oottil; Kleinke, Holger (2009). "Solid State Polyselenides and Polytellurides: A Large Variety of Se–Se and Te–Te Interactions". Molecules. 14 (9): 3115–3131. doi:10.3390/molecules14093115. PMC 6255372. PMID 19783911.
- Sheldrick, William S. (2012). "Polychalcogenide Anions: Structural Diversity and Ligand Versatility". Zeitschrift für Anorganische und Allgemeine Chemie. 638 (15): 2401–2424. doi:10.1002/zaac.201200241.
참고 항목
참조
- ^ Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (2nd ed.). Butterworth-Heinemann. p. 763-765. ISBN 978-0-08-037941-8.
- ^ Thompson, D.; Boudjouk, P. A (1988). "Convenient Synthesis of Alkali Metal Selenides and Diselenides in Tetrahydrofuran and the Reactivity Differences Exhibited By These Salts Toward Organic Bromides". Journal of Organic Chemistry. 53: 2109-2112. doi:10.1021/jo00244a051.
- ^ Kolis, J. "폴리찰코겐 음이온과 전이 금속 카보닐의 조정 화학" 1990, 105, 페이지 195-219. 도이:10.1016/0010-8545(90)80023-M
- ^ 배리, P. J.; 클라크, R. J. H.; 셀레늄 고체-상태 NMR 분광법과 테트라메틸람모늄 펜타셀레니드 및 헥사셀레니드 복합체의 구조Inorg. Chem, 1995, 34, 4299–4304 DOI: 10.1021/ic00121a006
- ^ Kanatzidis, Mercouri G. (1990). "Soluble Polychalcogenides of the Late Transition and Main Group Elements". Comments on Inorganic Chemistry. 10 (4–5): 161–195. doi:10.1080/02603599008048650.