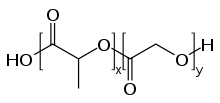
PLGA
PLGAPLGA, PLG 또는 폴리(lactic-co-glycolic acid)는 생분해성과 생체적합성 때문에 식품의약국(FDA) 승인 치료기기의 숙주에 사용되는 복합제다.PLGA는 글리콜산과 젖산의 주기적 디머(1,4-dioxane-2,5-diones)인 두 모노머의 고리 개방 공동 폴리머화를 통해 합성된다.폴리머는 무작위 또는 블록 복합체로 합성될 수 있으므로 추가적인 폴리머 특성을 부여할 수 있다.이 폴리머의 조제에 사용되는 공통 촉매에는 주석()이 포함된다.II) 2-에틸헥사노산염, 주석(II) 알코산화물 또는 이소프로산화 알루미늄.중합 시 PLGA에서 (글리콜산 또는 젖산의) 연속적인 단조 단위는 에스테르 링크에 의해 서로 연결되므로, 제품으로서 선형, 편광 폴리에스테르가 생성된다.[1]
코폴리머
중합에 사용되는 글라이콜라이드 대비 유당화 비율에 따라 다른 형태의 PLGA를 얻을 수 있다. 이러한 PLGA는 일반적으로 사용된 단량체의 어금니 비율과 관련하여 식별된다(예: PLGA 75:25는 유산과 25% 글리콜산 성분인 복합체를 나타낸다).PLGA의 결정성은 블록 구조와 어금니 비율에 따라 완전 비정형에서 완전 결정체까지 다양하다.PLGA는 일반적으로 40~60°C 범위에서 유리 전환 온도를 나타낸다.PLGA는 조성에 따라 광범위한 용매에 의해 용해될 수 있다.높은 유당 중합체는 염소 처리된 용제를 사용하여 용해될 수 있는 반면, 높은 글리콜리드 물질은 HFIP와 같은 불소 처리된 용제를 사용해야 한다.
PLGA는 물이 있는 곳에서 에스테르 연동을 가수 분해하여 분해한다.PLGA의 분해에 필요한 시간은 생산에 사용되는 단량체의 비율과 관련이 있는 것으로 나타났으며, 글리콜라이드 단위의 함량이 높을수록 유당화 물질에 비해 분해에 필요한 시간이 낮은 것으로 나타났다.이 규칙의 예외는 50:50의 모노머 비율을 가진 복합체로서 더 빠른 성능 저하(약 2개월)를 나타낸다.또한 에스테르(무료 카복실산과는 대조적으로)로 엔드캡을 받은 폴리머는 반감기 분해 시간이 더 길다는 것을 보여준다.[2]이러한 성능 저하 유연성은 이식, 봉합, 임플란트, 보철 장치, 외과용 실란트 필름, 마이크로 및 나노 입자와 같은 많은 의료기기의 제작에 편리해졌다.[3]
PLGA는 원래 모노머인 젖산과 글리콜산을 생산하기 위해 체내에서 가수분해를 겪는다.정상적인 생리적 조건 하에서 이 두 단조체는 체내의 다양한 대사 경로의 부산물이다.젖산은 트리카복실산 사이클에서 대사되며 이산화탄소와 물을 통해 제거된다.글리콜산은 같은 방식으로 대사되며, 또한 신장을 통해 배설된다.[4]신체는 두 개의 모노머를 대사시킬 수 있기 때문에, 생체 재료 용도에 PLGA를 사용하는 것과 관련된 전신 독성은 거의 없다.그러나 PLGA의 산성저하로 인해 국소 pH가 충분히 낮아져 자기분석적인 환경이 조성되는 것으로 보고되었다.[5]마이크로스피어 내부의 pH는 pH 1.5만큼 산성이 될 수 있다는 것이 밝혀졌다.[6]
예
PLGA 사용의 구체적인 예는 다음과 같다.
- PLGA를 이용해 상업적으로 구할 수 있는 약물전달장치는 전립선암 전립선암 치료를 위한 루프론 디포다.
- 뇌수술[7][8] 후 뇌 표면에 항생제 반코마이신을 바르면 중추신경계로 예방적으로 전달한다.
참고 항목
참조
- ^ Astete, C. E. & Sabliov, C. M. (2006). "Synthesis and characterization of PLGA nanoparticles". Journal of Biomaterials Science, Polymer Edition. 17 (3): 247–289. doi:10.1163/156856206775997322. PMID 16689015.
- ^ Samadi, N.; Abbadessa, A.; Di Stefano, A.; van Nostrum, C. F.; Vermonden, T.; Rahimian, S.; Teunissen, E. A.; van Steenbergen, M. J.; Amidi, M. & Hennink, W. E. (2013). "The effect of lauryl capping group on protein release and degradation of poly(D,L-lactic-co-glycolic acid) particles". Journal of Controlled Release. 172 (2): 436–443. doi:10.1016/j.jconrel.2013.05.034. PMID 23751568.
- ^ Pavot, V; Berthet, M; Rességuier, J; Legaz, S; Handké, N; Gilbert, SC; Paul, S; Verrier, B (December 2014). "Poly(lactic acid) and poly(lactic-co-glycolic acid) particles as versatile carrier platforms for vaccine delivery". Nanomedicine (Lond.). 9 (17): 2703–18. doi:10.2217/nnm.14.156. PMID 25529572.
- ^ Crotts, G (2 July 1998). "Protein delivery from poly(lactic-co-glycolic acid) biodegradable microspheres: Release kinetics and stability issues". Journal of Microencapsulation. 15 (6): 699–713. doi:10.3109/02652049809008253. PMID 9818948.
- ^ Zolnik, Banu; Burgess, Diane (2007). "Effect of acidic pH on PLGA microsphere degradation and release". JCR. 122 (3): 338–44. doi:10.1016/j.jconrel.2007.05.034. PMID 17644208.
- ^ Karen, Fu; Pack, Daniel; Alexander, Klibanov; Langer, Robert (2000). "Visual Evidence of Acidic Environment Within Degrading Poly(lactic-co-glycolic acid) (PLGA) Microspheres". Pharm Res. 17 (1): 100–106. doi:10.1023/A:1007582911958. PMID 10714616.
- ^ "Dissolvable Plastic Nanofibers could Treat Brain Infections". Scientific Computing. Advantage Business Media. August 28, 2013. Retrieved September 3, 2013.
- ^ "PLGA 50 50". Scientific Computing. Advantage Business Media. August 28, 2013. Retrieved September 3, 2013.
외부 링크
 Wikimedia Commons의 PLGA 관련 미디어
Wikimedia Commons의 PLGA 관련 미디어