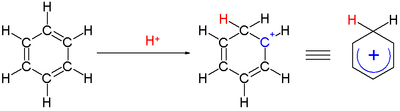
아레늄 이온
Arenium ion
유기화학에서 아레늄 이온은 전기영양 방향족 치환에서 반응성 매개체로 나타나는 사이클로헥사디엔아닐 양이온이다.[1] 역사적인 이유로 이 콤플렉스는 미국의 화학자 조지 윌러드 윌랜드(1907–1976)의 이름을 따서 윌랜드 중간체라고도 불린다.[2] 시그마 콤플렉스라고도 한다.[3] 가장 작은 아레늄 이온은 양성 벤젠인 벤젠 이온(CH
6+
7)이다.
하나의 탄소에 결합된 두 개의 수소 원자가 벤젠 고리에 수직인 평면에 놓여 있다.[4] 아레늄 이온은 더 이상 방향족은 아니지만, 탈색현상으로 인해 비교적 안정적이다: 양극 전하가 다음의 공명 구조에서 설명한 바와 같이 파이 시스템에 의해 3개의 탄소 원자에 걸쳐 분산된다.
복잡한 전기영동은 아레늄 이온의 안정성에 기여할 수 있다.
벤젠 이온의 염분은 카르보레인 초산화물 H(CBH(11CH3)5Br6)에 의해 벤젠이 양성될 때 격리될 수 있다.[5] 벤제늄 소금은 최대 150 °C의 열 안정성을 가진 결정체다. X선 결정학에서 추론된 결합 길이는 사이클로헥사디아닐 양이온 구조와 일치한다.
한 연구에서 메틸렌 아레늄 이온은 금속 복합화에 의해 안정화된다.[6]
이 반응 시퀀스에서 TMEDA에 의해 안정화된 R-Pd(II)-Br 출발 복합체 1은 dppe를 통해 금속 복합체 2로 변환된다. (X선 결정학에 근거한) 양의 전하를 방향족 파라 위치에 두고 링의 평면 밖으로 6° 나가는 메틸렌 그룹과 함께 메틸렌 삼불산염 이온 3의 전기적 공격. 먼저 물로 반응한 다음 트리에틸아민으로 반응하면 에테르 그룹이 가수분해된다.
참고 항목
- 아릴 래디컬
- 사이클로펜타디엔닐 음이온
- 핵포함 방향족 대체의 아날로그 중간형인 마이젠하이머 콤플렉스
- 트로필리움 계통
일부 역사적 언급
- Olah, G. A. (1972). "Stable carbocations. CXVIII. General concept and structure of carbocations based on differentiation of trivalent (classical) carbenium ions from three-center bound penta- or tetracoordinated (nonclassical) carbonium ions. Role of carbocations in electrophilic reactions". J. Am. Chem. Soc. 94 (3): 808–820. doi:10.1021/ja00758a020.
- Wheland, G. W. (1942). "A Quantum Mechanical Investigation of the Orientation of Substituents in Aromatic Molecules". J. Am. Chem. Soc. 64 (4): 900–908. doi:10.1021/ja01256a047.
참조
- ^ Smith, Michael B.; March, Jerry (2007), Advanced Organic Chemistry: Reactions, Mechanisms, and Structure (6th ed.), New York: Wiley-Interscience, p. 658, ISBN 978-0-471-72091-1
- ^ Smith, Michael B. (18 October 2010). Organic Chemistry: An Acid—Base Approach. CRC Press. ISBN 9781439894620 – via Google Books.
- ^ 더 흔히, 시그마 콤플렉스는 보통 유기농 콤플렉스의 한 유형을 가리킨다.
- ^ Sykes, Peter. A Guidebook to Mechanism in Organic Chemistry. p. 130–133.[ISBN 누락]
- ^ Reed, C. A.; Kim, K.; Stoyanov, E. S.; Stasko, D.; Tham, F. S.; Mueller, L. J.; Boyd, P. D. W. (2003). "Isolating Benzenium Ion Salts". J. Am. Chem. Soc. 125 (7): 1796–804. doi:10.1021/ja027336o. PMID 12580605.
- ^ Poverenov, E.; Leitus, G.; Milstein, D. (2006). "Synthesis and Reactivity of the Methylene Arenium Form of a Benzyl Cation, Stabilized by Complexation". J. Am. Chem. Soc. (Communication). 128 (51): 16450–1. doi:10.1021/ja067298z. PMID 17177364.