T자형 분자 기하학
T-shaped molecular geometry| T자형 분자 기하학 | |
|---|---|
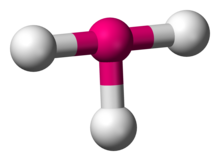 | |
| 예 | CLF3 |
| 점군 | C2v |
| 조정번호 | 3 |
| 본드 각도 | 90°, 180° |
| μ(극성) | >0 |

T자형 조정기하를 갖는 화합물의 예인 3불화염소의 구조.
화학에서 T자 모양의 분자 기하학은 중심 원자가 3개의 리간드를 갖는 일부 분자의 구조를 설명한다.일반적으로 세 개의 조정된 화합물은 삼각 평면 또는 피라미드 기하학을 채택한다.T형 분자의 예로는 ClF와3 같은 할로겐 3불화합물이 있다.[1]
VSEPR 이론에 따르면, T자 형상은 AXE로32 표기된 AXE 표기법으로 쓰여진 3개의 리간드와 2개의 한 쌍의 전자가 중심 원자에 결합될 때 발생한다.T자 형상은 적도 3개와 축간지 2개를 가진 AX5 분자에 대한 삼각형 쌍곡선 분자 형상과 관련이 있다.AXE32 분자에서는 두 개의 외로운 쌍이 두 개의 적도 위치를 차지하고, 세 개의 리간드 원자가 두 개의 축 위치뿐만 아니라 한 개의 적도 위치를 차지하고 있다.세 개의 원자는 중심 원자의 한 면에 90° 각도로 결합하여 T 형상을 만들어 낸다.[2]
삼불화산염(trifluoroxenate).II) 음이온, XeF는−
3 AXE33 분자의 가능한 첫 번째 예로서 조사되었으며, VSEPR 추론에 의해 3개의 단독 쌍과 3개의 리간드를 모두 8개의 면으로 배열한 상태에서 메리 또는 T자 방향으로 6개의 전자 쌍을 가질 것으로 예상할 수 있다.[3]비록 이 음이온이 가스 단계에서 검출되었지만, 용액에서의 합성 시도와 실험 구조 결정에는 성공하지 못했다.컴퓨터 화학 연구에서는 T자 형상과 같이 90°가 아니라 69°에 해당하는 F-Xe-F 접합 각도가 가장 작은 평면 Y자 형상이 왜곡된 것으로 나타났다.[3]
참고 항목
참조
- ^ Greenwood, N. N.; Earnshaw, A. (1997). Chemistry of the Elements (2nd ed.). Oxford: Butterworth-Heinemann. ISBN 978-0-7506-3365-9.
- ^ Housecroft, C. E.; Sharpe, A. G. (2004). Inorganic Chemistry (2nd ed.). Prentice Hall. p. 47. ISBN 978-0-13-039913-7.
- ^ a b Vasdev, Neil; Moran, Matthew D.; Tuononen, Heikki M.; Chirakal, Raman; Suontamo, Reijo J.; Bain, Alex D.; Schrobilgen, Gary J. (2010). "NMR Spectroscopic Evidence for the Intermediacy of XeF−
3 in XeF2/F− Exchange, Attempted Syntheses and Thermochemistry of XeF−
3 Salts, and Theoretical Studies of the XeF−
3 Anion". Inorg. Chem. 49 (19): 8997–9004. doi:10.1021/ic101275m. PMID 20799721.


